Trong phân tử oxygen, số oxi hóa của nguyên tử oxygen là
Phân tử O2 là đơn chất số oxi hóa của nguyên tử oxygen là 0.
Trong phân tử oxygen, số oxi hóa của nguyên tử oxygen là
Phân tử O2 là đơn chất số oxi hóa của nguyên tử oxygen là 0.
Cho quá trình Mn+7 + 5e → Mn+2, đây là quá trình
Quá trình oxi hóa (sự oxi hóa) là quá trình nhường electron.
Quá trình khử (sự khử) là quá trình thu electron.
Quá trình Mn+7 + 5e → Mn+2 là quá trình khử
Số oxi hóa của S trong phân tử K2SO4 là
Trong hợp chất, số oxi hóa của K là +1, số oxi hóa của O là –2.
Số oxi hóa của từng nguyên tử:
Ta có: (+1).2 + x + (–2).4 = 0 x = +6.
Cho phản ứng sau:
KMnO4 + FeSO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
Hệ số của chất oxi hóa và chất khử trong phản ứng trên lần lượt là
Phương trình phản ứng:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Chất oxi hóa là KMnO4
Chất khử là FeSO4
Hệ số cân bằng (là các số nguyên, tối giản) của Cu2S và HNO3 trong phản ứng: Cu2S + HNO3 → Cu(NO3)2 + H2SO4 + NO + H2O là
Sự thay đổi số oxi hóa của các nguyên tố:
Phương trình phản ứng:
3Cu2S + 22HNO3 → 6Cu(NO3)2 + 3H2SO4 + 10NO + 8H2O
Vậy hệ số cân bằng của Cu2S và HNO3 trong phản ứng là 3 và 22
Cho sơ đồ phản ứng sau: Al + HNO3 → Al(NO3)3 + N2 + H2O. Hệ số cân bằng của phản ứng lần lượt là:
Xác định vai trò của từng chất tham gia phản ứng và nêu sự oxi hóa, sự khử:
Al0 + H+5NO3loãng → Al+3(NO3)3+ N02+ H2O
Số oxi hóa của Al tăng từ 0 lên +3 ⇒ Al là chất khử
Số oxi hóa của N giảm từ +5 xuống 0 ⇒ HNO3 là chất oxi hóa
Sự oxi hóa: Al → Al+3 + 3e
Sự khử: 2N+5 + 10e → N2
b) Cân bằng phản ứng trên theo phương pháp thăng bằng electron.
0Al + H+5NO3 loãng → Al+3(NO3)3+ 0N2 + H2O
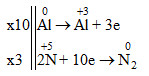
Phương trình phản ứng
10Al + 36HNO3 loãng → 10Al(NO3)3 + 3N2 + 18H2O
Số oxi hóa của sulfur (lưu huỳnh) trong H2SO3 là:
Số oxi hóa của H là + 1 và O là -2, gọi số oxi hóa của S là x, ta có:
2.1 + 3.(-2) + x = 0 ⇒ x = +4.
Cho 8,1 gam Al tác dụng với dung dịch HNO3 thu được 2,2311 lít khí X (không có sản phẩm khử khác). Khí X là:
TH1: khí tạo ra chỉ có 1 N trong công thức
Quá trình nhường nhận electron:
Al → Al+3 + 3e
N+5 + (5 - x) e→ N+x
Theo định luật bảo toàn electron:
0,3.3 = 0,09.x
x = 10 (loại vì x < 5)
TH2: khí tạo ra có 2 N
Quá trình nhường nhận electron:
Al → Al+3 + 3e
2N+5 + 2(5 - x)e → 2N+x
0,3.3 = 0,09.2.(5-x)
x = 0
Vậy N có số oxi hóa 0 trong khí X do đó X là khí N2.
Dựa vào các công thức ion giả định, những nguyên tử nào lần lượt có số oxi hóa âm trong các hợp chất CH4, F2O?
Dựa vào các công thức ion giả định, ta có:
Trong phân tử, khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các
Trong phân tử, khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các lưỡng cực tạm thời.
Trong phân tử NH4NO3 thì số oxi hóa của 2 nguyên tử nitơ là :
NH4NO3 tạo bởi NH4+ và ion NO3-.Gọi số oxi hóa của N bằng x.
Trong NH4+: x.1 + (+1).4 = +1 ⇒ x = -3
NO3-: x .1 + (-2).3 = -1 ⇒ x = +5.
Cho phản ứng hoá học: aAl + bHNO3 → cAl(NO3)3 + dNO + eH2O. Tổng hệ số (a + b) là
Xác định số oxi hóa của các nguyên tố thay đổi
1x 1x | Al0 → Al+3 + 3e N+5 + 3e → N+2 |
Vậy ta có phương trình:
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
Tổng hệ số a + b = 1 + 4 = 5
Số oxi hoá của carbon và oxygen trong C2O42- lần lượt là:
Ta có số oxi hóa của oxygen trong C2O42– là –2:
Gọi số oxi hóa của C là x thì:
2.x + 4.(–2) = –2 ⇒ x = +3.
Trong đơn chất, số oxi hóa của nguyên tử bằng
Trong đơn chất, số oxi hóa của nguyên tử bằng 0.
VD:
Số oxi hóa của một nguyên tử một nguyên tố trong hợp chất là
Số oxi hóa của một nguyên tử một nguyên tố trong hợp chất là điện tích của nguyên tử nguyên tố đó với giả định đây là hợp chất ion.
Trong phản ứng sau: 2FeCl3 + H2S → 2FeCl2 + S + 2HCl. Vai trò của FeCl3 là:
Số oxi hóa của Fe giảm từ +3 xuống +2. Vậy FeCl3 đóng vai trò là chất khử.
Cho phản ứng hóa học: Fe + CuSO4 → FeSO4 + Cu. Trong phản ứng trên xảy ra
Cho phản ứng hóa học: Fe + CuSO4 → FeSO4 + Cu. Trong phản ứng trên xảy ra sự oxi hóa Fe và sự khử Cu2+
Sự oxi hóa: Fe0 → Fe+2 + 2e
Sự khử: Cu+2 + 2e → Cu0
Điều nào đúng khi nói về vai trò của các chất tham gia sơ đồ phản ứng oxi hóa khử sau?
KMnO4 + HCl KCl + MnCl2 + Cl2 + H2O
Chất khử (chất bị oxi hóa) là chất nhường electron
Chất oxi hóa (chất bị khử) là chất nhận electron
Quá trình oxi hóa (sự oxi hóa) là quá trình nhường electron
Quá trình khử (sự khử) là quá trình thu electron
Xác định sự thay đổi số oxi hóa của các nguyên tố
HCl là chất khử
KMnO4 là chất oxi hóa
|
x5 x2 |
|
⇒ 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O.
Số oxi hóa của Fe trong FexOy là:
Số oxi hóa của O là -2, gọi số oxi hóa của Fe là a, ta có:
x.a + y.(-2) = 0 ⇒ a =
Trong các phản ứng sau phản ứng nào là phản ứng oxi hóa - khử:
Phương trình phản ứng oxi hóa khử là
2CH3COOH + Mg → (CH3COO)2Mg + H2
