Cho phản ứng 3O2 → 2O3. Ban đầu nồng độ oxygen là 0,022 mol/L. Sau 4s thì nồng độ của oxygen là 0,02 mol/L. Tốc độ phản ứng trên tính theo oxygen là:
Tốc độ phản ứng trung bình:
Cho phản ứng 3O2 → 2O3. Ban đầu nồng độ oxygen là 0,022 mol/L. Sau 4s thì nồng độ của oxygen là 0,02 mol/L. Tốc độ phản ứng trên tính theo oxygen là:
Tốc độ phản ứng trung bình:
Cho 1,5 g bột Mg (dư) vào 100 mL dung dịch HCl 1M, sau khi phản ứng hoàn toàn, nhiệt độ dung dịch tăng lên 8,3oC. Biết nhiệt dung riêng của H2O là 4,2 J/g.K. Nhiệt lượng của phản ứng là:
Phản ứng xảy ra:
Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g)
Số mol HCl = 0,1 mol
Q = m.c.∆T = 100.4,2.8,3 = 3486 (J)
0,1 mol HCl phản ứng tỏa ra nhiệt lượng là 3486 (J)
2 mol HCl phản ứng tỏa ra nhiệt lượng là:
⇒
Cho dung dịch chứa 6,03 gam hỗn hợp gồm hai muối NaX và NaY (X, Y là hai nguyên tố có trong tự nhiên) ở hai chu kì liên tiếp thuộc nhóm VIIA, số hiệu nguyên tử ZX < ZY) vào dung dịch AgNO3 (dư), thu được 8,61 gam kết tủa. Phần trăm khối lượng của NaX trong hỗn hợp ban đầu là
X, Y ở hai chu kì liên tiếp thuộc nhóm VIIA
⇒ X, Y là nguyên tố halogen.
TH1: Cả 2 muối hhalide đều tạo kết tủa
Gọi halogen trung bình là R ⇒ muối là NaR (MX < MR < MY)
NaR + AgNO3 → AgR↓ + NaNO3
⇒ MR = 175,66
⇒ Halogen là I và At (At không có trong tự nhiên ⇒loại
TH2: Chỉ có 1 muối halide tạo kết tủa ⇒ 2 muối là NaF và NaCl
NaCl + AgNO3 → AgCl + NaNO3
⇒ nNaCl = 0,06 mol ⇒ mNaCl = 3,51 gam
⇒ mNaF = 6,03 – 3,51 = 2,52 gam
Hệ số cân bằng của H2 trong phản ứng: Fe2O3 + H2 ⟶ Fe + H2O là
Bước 1:
Bước 2:
Bước 3:
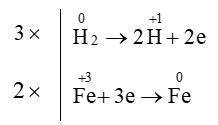
Bước 4: Fe2O3 + 3H2⟶ 2Fe + 3H2O
Chất A là muối calcium halide. Cho dung dịch chứa 0,2 gam A tác dụng với lượng dư dung dịch silver nitrate thì thu được 0,376 gam kết tủa. Hãy xác định công thức chất A.
Phương trình hóa học:
CaX2 + 2AgNO3 → Ca(NO3)2 + 2AgX (X là halogen)
Áp dụng phương pháp tăng giảm khối lượng:
Theo phương trình cứ 1 mol CaX2 tham gia phản ứng tạo 2 mol AgX.
Khối lượng AgX tăng so với khối lượng CaX2 là:
(2.108 + 2MX) – (40 – 2MX) = 176
Theo đề bài, số mol CaX2 tham gia phản ứng là:
MCaX2 = 0,2/0,001 = 200 (g/mol)
40 + 2MX = 200
MX = 80
Vậy X là Brom (Br). Công thức của chất A là CaBr2
Halogen nào sau đây dùng để khử trùng nước sinh hoạt?
Halogen được dùng để khử trùng nước sinh hoạt là Cl2.
Trong phản ứng 2KMnO4 + 6KI + 4H2O → 2MnO2 + 3I2 + 8KOH, ion bị oxi hóa là:
Trong phản ứng:
2KMnO4 + 6KI + 4H2O → 2MnO2 + 3I2 + 8KOH, ion bị oxi hóa là I-, số oxi hóa của ion này tăng từ -1 lên 0 trong đơn chất I2.
Trong phân tử oxygen, số oxi hóa của nguyên tử oxygen là
Phân tử O2 là đơn chất số oxi hóa của nguyên tử oxygen là 0.
Phản ứng nào sau đây là phản ứng tỏa nhiệt?
Dấu của biến thiên enthalpy cho biết phản ứng tỏa nhiệt hay thu nhiệt:
∆rH0298 > 0: phản ứng thu nhiệt.
∆rH0298 < 0: phản ứng tỏa nhiệt.
Xét phản ứng
C4H10 (g) + 13O2 8CO2 (g) + 10H2O (l)
∆rH0298 = -5316,0 kJ < 0 phản ứng tỏa nhiệt.
Phát biểu nào sau đây sai?
Phản ứng tỏa nhiệt thì năng lượng của hệ chất phản ứng cao hơn hơn năng lượng của hệ sản phẩm.
Phản ứng không đúng là: HF + NaCl → NaF + HCl
Do phản ứng này không xảy ra.
Những hydrogen halide có thể thu được khi cho H2SO4 đặc lần lượt tác dụng với các muối NaF, NaCl, NaBr, NaI là:
Hydrogen halide có thể là HF và HCl.
Không thể là HBr và HI vì khí HBr và HI sinh ra phản ứng được với H2SO4 đặc nóng.
Phản ứng nào dưới đây không là phản ứng oxi hoá - khử?
Nhận thấy số oxi hóa của các nguyên tử trong các phân tử không thay đổi số oxi hóa
Không phải phản ứng oxi hóa khử.
Số oxi hóa của nguyên tố hydrogen trong hydrogen chloride bằng:
Số oxi hóa của hydrogen trong HCl là +1
Nguyên tố R có cấu hình electron: 1s22s22p3. Công thức hợp chất oxide ứng với hóa trị cao nhất của R và hydride (hợp chất của R với hydrogen) tương ứng là
Nguyên tố R có cấu hình electron: 1s22s22p3
⇒ Thuộc nhóm VA trong bảng tuần hoàn.
⇒ Hóa trị cao nhất trong hợp chất oxide là V và hydride là III.
⇒ Công thức hợp chất oxide ứng với hóa trị cao nhất của R và hydride (hợp chất của R với hydrogen) tương ứng là R2O5 và RH3.
Trong y tế đơn chất halogen nào hòa tan trong rượu được dùng làm chất sát trùng?
Trong y tế, I2 được hòa tan trong ethanol để dùng làm chất sát trùng vết thương.
Cho phương trình nhiệt hoá học của phản ứng:
2H2(g) + O2(g) → 2H2O(l) ![]() = - 571,68 kJ
= - 571,68 kJ
Phản ứng trên là phản ứng
Ta có: = - 571,68 kJ < 0
Phản ứng là phản ứng tỏa nhiệt, có sự giải phóng nhiệt ra ngoài môi trường.
Cho 1,12 gam một kim loại X tác dụng với khí chlorine dư thu được 3,25 gam muối. Kim loại đó là
Gọi X là n.
Áp dụng định luật bảo toàn khối lượng ta có:
mX + mCl2 = mXCln 1,12 + mCl2 = 3,25
mCl2 = 2,13 g
Phương trình phản ứng:
2X + nCl2 → 2XCln
n = 3 X = 56 (Fe)
X được dùng làm chất bán dẫn trong kĩ thuật vô tuyến điện, chế tạo pin mặt trời. Nguyên tử của nguyên tố X có 3 lớp electron. Lớp ngoài cùng có 4 electron. Số hiệu nguyên tử của X là
Nguyên tử của nguyên tố X có 3 lớp electron và lớp ngoài cùng có 4 electron
⇒ Cấu hình electron của X là: 1s22s22p63s23p2
⇒ Số hiệu nguyên tử của X là: Z = P = E = 14
Giản đồ biến thiên enthalpy chuẩn của phản ứng giữa methane và oxygen được biểu diễn ở hình dưới đây:
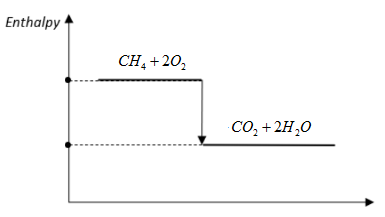
Phát biểu nào sau đây không đúng khi nói về phản ứng trong hình?
Theo đề bài thì chất đầu là CH4 và O2, sản phẩm là CO2 và H2O.
Có phản ứng toả nhiệt (ΔH < 0) có sơ đồ biến thiên enthalpy như sau:
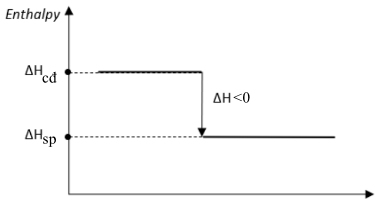
⇒ Phản ứng giữa methane và oxygen là phản ứng toả nhiệt.
Phosphine (PH3) là một chất khí không màu, nhẹ hơn không khí, rất độc và dễ cháy. Khí này thường thoát ra từ xác động vật thối rữa, khi có mặt diphosphine (P2H4) thường tự bốc cháy trong không khí, đặc biệt ở thời tiết mưa phùn, tạo hiện tượng “ma trơi” ngoài nghĩa địa.
Phản ứng cháy phosphine: 2PH3(g) + 4O2(g) → P2O5(s) + 3H2O(l)
Biết nhiệt tạo thành chuẩn của các chất cho trong bảng sau:
| Chất | PH3(g) | P2O5(s) | H2O(l) |
| 5,4 | –365,8 | –285,8 |
Tính biến thiên enthalpy chuẩn của phản ứng trên?
=
(P2O5) + 3.
(H2O) – 2.
(PH3) –
(O2)
⇒ = [–365,8 + 3.(–285,8)] – 2.5,4 – 4.0 = –1234 (kJ)
Dãy acid nào sau đây sắp xếp đúng theo thứ tự giảm dần tính acid?
Dãy acid được sắp xếp đúng theo thứ tự giảm dần tính acid là HI > HBr > HCl > HF.
Tốc độ của phản ứng hoá học là đại lượng mô tả mức độ nhanh hay chậm của chất phản ứng được sử dụng hoặc sản phẩm được tạo thành.
a) Trong cùng một phản ứng hoá học, tốc độ tiêu thụ các chất phản ứng khác nhau sẽ như nhau nếu chúng được lấy với cùng một nồng độ. Sai||Đúng
b) Tốc độ của phản ứng hoá học không thể xác định được từ sự thay đổi nồng độ chất sản phẩm tạo thành theo thời gian. Đúng||Sai
c) Tốc độ của phản ứng hoá học có thể có giá trị âm hoặc dương. Sai||Đúng
d) Hằng số tốc độ phản ứng có giá trị đúng bằng tốc độ phản ứng khi nồng độ các chất phản ứng bằng nhau và bằng 1 M. Đúng||Sai
Tốc độ của phản ứng hoá học là đại lượng mô tả mức độ nhanh hay chậm của chất phản ứng được sử dụng hoặc sản phẩm được tạo thành.
a) Trong cùng một phản ứng hoá học, tốc độ tiêu thụ các chất phản ứng khác nhau sẽ như nhau nếu chúng được lấy với cùng một nồng độ. Sai||Đúng
b) Tốc độ của phản ứng hoá học không thể xác định được từ sự thay đổi nồng độ chất sản phẩm tạo thành theo thời gian. Đúng||Sai
c) Tốc độ của phản ứng hoá học có thể có giá trị âm hoặc dương. Sai||Đúng
d) Hằng số tốc độ phản ứng có giá trị đúng bằng tốc độ phản ứng khi nồng độ các chất phản ứng bằng nhau và bằng 1 M. Đúng||Sai
a) Sai:
Vì trong cùng một phản ứng hoá học, tốc độ tiêu thụ của các chất phản ứng khác nhau là khác nhau, tuỳ thuộc vào hệ số cân bằng của chúng trong phương trình hoá học.
b) Đúng
c) Sai:
Vì tốc độ phản ứng có giá trị dương.
d) Đúng.
Hoà tan hoàn toàn 16,2 gam kim loại R hóa trị I vào dung dịch HNO3 dư thu được 1,12 lít khí NO ở đktc (sản phẩm khử duy nhất) và dung dịch muối nitrat của R. R là kim loại nào dưới đây?
nNO = 0,05 mol
Gọi x là số mol của kim loại R hóa trị I.
Quá trình nhường e R0 → R+1 + 1e x → x | Quá trình nhận e N+5 + 3e → N+2 0,15 ← 0,05 |
Áp dụng định luật bảo toàn e ta có
x = 0,15 mol
=> MR = 16,2/0,05 = 108 (Ag)
Than đá được nghiền nhỏ dùng trong quá trình luyện kim loại. Cho biết yếu tố chính ảnh hưởng đến tốc độ phản ứng trong quá trình trên:
Yếu tố chính ảnh hưởng đến tốc độ phản ứng trong quá trình trên bề mặt tiếp xúc.
Rót 3 mL dung dịch HCl 1 M vào 2 mL dung dịch NaOH 1 M, cho quỳ tím vào dung dịch sau phản ứng, mẩu quỳ tím sẽ:
nHCl = 0,003 mol, nNaOH = 0,002 (mol)
Phương trình phản ứng:
HCl + NaOH → NaCl + H2O
mol: 0,002 ← 0,002
⇒ Sau phản ứng HCl dư ⇒ mẩu quỳ tím sẽ hóa màu đỏ.
Cho các phản ứng:
(1) SiO2 + dung dịch HF →
(2) F2 + H2O ![]()
(3) AgBr ![]()
(4) Br2 + NaI (dư) →
Trong các phản ứng trên, những phản ứng có tạo ra đơn chất là
(1) SiO2 + HF → SiF4 + 2H2O
(2) F2 + H2O 4HF + O2↑
(3) AgBr 2Ag + Br2
(4) Br2 + NaI (dư) → NaBr + I2
Các phản ứng tạo ra đơn chất là: (1); (2); (4).
Liên kết hydrogen không được hình thành giữa hai phân tử nào sau đây?
Liên kết hydrogen là liên kết yếu được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron riêng. Các nguyên tử có độ âm điện lớn thường gặp trong liên kết hydrogen là N, O, F…
Nguyên tử H của phân tử H2O không tạo được liên kết hydrogen với nguyên tử C của C2H6 vì nguyên tử C của phân tử C2H6 không còn cặp electron riêng.
Nguyên tử nguyên tố nitrogen (N) có 7 proton. Công thức oxide cao nhất và tính chất của oxide đó là
Nguyên tử nguyên tố nitrogen (N) có 7 proton ⇒ Z = 16
Cấu hình electron của N: 1s22s22p3 ⇒ chu kì 2, nhóm VA
Hóa trị cao nhất của N = số thứ tự nhóm VA = VI
⇒ Công thức oxide cao nhất là: N2O5
N có 5 electron lớp ngoài cùng ⇒ N là nguyên tố phi kim
⇒ Oxide có tính acid oxide.
Tốc độ phản ứng tính theo định luật tác dụng khối lượng là
Tốc độ phản ứng tính theo định luật tác dụng khối lượng là tốc độ tức thời của phản ứng tại một thời điểm.
Đơn vị của nhiệt tạo thành chuẩn là
Phản ứng tạo NaCl từ Na và Cl2 có ΔH = -98,25 kcal/mol. Nếu tiến hành phản ứng giữa 46 gam Na với 71 gam Cl2 trong bình kín bằng thép, đặt chìm trong một bể chứa 10 lít nước ở 25oC thì sau phản ứng hoàn toàn nhiệt độ của nước trong bể là (biết nhiệt dung riêng của nước là 4,186 J/g.K và nhiệt lượng sinh ra truyền hết cho nước)
mH2O = V.D = 10.1 = 10 kg
Nhiệt tỏa ra khi cho 2 mol Na tác dụng với 1 mol Cl2 là:
Q = 98,25. 2 = 196,5 (kcal)
Q = mC(T2 - T1) = 10.1 (T2 - T1) = 196,5
⇒ T2 - T1 = 19,65
⇒T2 = 19,65 + 25 = 44,65 oC
Nước muối sinh lý có tác dụng diệt khuẩn, sát trùng trong y học là dung dịch có nồng độ của muối nào sau đây?
Nước muối sinh lý có tác dụng diệt khuẩn, sát trùng trong y học là dung dịch có nồng độ của NaCl.
Trong phản ứng 6KI + 2KMnO4 +4H2O → 3I2 + 2MnO2 + 8KOH, chất bị oxi hóa là
6KI-1 + 2KMnO4 + 4H2O → 3I02 + 2MnO2 + 8KOH.
Số oxi hóa của I trong KI tăng lên
→ I- là chất khử (chất bị oxi hóa).
X, Y là hai nguyên tố thuộc cùng một nhóm A, ở hai chu kỳ liên tiếp. Cho biết tổng số electron trong anion XY32− là 42. Liên kết giữa X và Y trong ion XY32- thuộc loại liên kết nào?
Tổng số electron: pX + 3pY + 2 = 42
- Nếu pX – pY = 8 ⇒ pX = 16, pY = 8. Ion là SO32-
- Nếu pY – pX = 8 ⇒ pX = 4, pY = 12, loại vì Be và Mg không tạo ion dạng MgBe32-
⇒ Liên kết giữa S và O là liên kết cộng hóa trị phân cực.
Để chứng minh Cl2 vừa có tính khử vừa có tính oxi hóa, người ta cho Cl2 tác dụng với
Để chứng minh Cl2 vừa có tính khử vừa có tính oxi hóa, người ta cho Cl2 tác dụng với dung dịch NaOH loãng:
Chất nào sau đây được ứng dụng dùng để tráng phim ảnh?
Silver bromide (AgBr) là chất nhạy với ánh sáng, dùng để tráng phim ảnh.
Cho m gam Mg tác dụng vừa đủ với dung dịch H2SO4 đặc đến khi phản ứng xảy ra hoàn toàn thu được dung dịch X và 2,479 lít khí SO2 (sản phẩm khử duy nhất S+6, ở đkc). Giá trị của m là
nSO2 = 0,1 (mol)
Quá trình nhường electron:
Quá trình nhận electron:
Áp dụng bảo toàn electron:
2nMg = 2nSO2 ⇒ nMg = nSO2 = 0,1 mol
⇒ mMg = 0,1.24 = 2,4 gam
Khi đun nóng, Cl2 phản ứng với dung dịch potassium hydroxide tạo thành muối X. Biết X là chất oxi hóa mạnh, được sử dụng chế tạo thuốc nổ, hỗn hợp đầu que diêm, … Công thức hóa học của X là
Khi đun nóng, Cl2 phản ứng với dung dịch potassium hydroxide tạo thành muối chlorate (KClO3).
3Cl2 + 6KOH 5KCl + KClO3 + 3H2O
Potassium chorate là chất oxi hóa mạnh, được sử dụng chế tạo thuốc nổ, hỗn hợp đầu que diêm, …
Trong các phản ứng hoá học, để chuyển thành anion, nguyên tử của các nguyên tố halogen đã nhận hay nhường bao nhiêu electron?
Để chuyển thành anion, nguyên tử của các nguyên tố halogen đã nhận thêm 1 electron:
X + 1e X-
