Các liên kết trong phân tử nitrogen được tạo thành do sự xen phủ của các
Các liên kết trong phân tử nitrogen được tạo thành do sự xen phủ của 3 orbital p giống nhau về hình dạng và kích thước, chỉ khác nhau về sự định hướng trong không gian.
Các liên kết trong phân tử nitrogen được tạo thành do sự xen phủ của các
Các liên kết trong phân tử nitrogen được tạo thành do sự xen phủ của 3 orbital p giống nhau về hình dạng và kích thước, chỉ khác nhau về sự định hướng trong không gian.
Dãy các chất nào dưới đây mà tất cả các phân tử đều có liên kết ion?
Loại các đáp án có chứa các phân tử H2, HCl, NH3, F2, HI, CO2, N2, CH4 chỉ chứa liên kết cộng hóa trị.
Vậy dãy các chất mà tất cả các phân tử đều có liên kết ion là: KCl, Al2O3, NaF, Ba(OH)2.
Mô tả sự hình thành ion của nguyên tử Na (Z = 11) theo quy tắc octet là?
Na (Z= 11) có cấu hình electron: 1s22s22p63s1 → có 1 electron lớp ngoài cùng.
Khí hiếm gần nhất là: Ne (Z = 10): 1s22s22p6
Do đó, Na có xu hướng nhường 1 electron lớp ngoài cùng để trở thành ion mang điện tích dương.
Na → Na+ + 1e.
Phát biểu nào sau đây không đúng?
Hợp chất NaNO3 tạo nên bởi các ion đơn nguyên tử (Na+) và đa nguyên tử (NO3-)
Na+ + NO3- → NaNO3
Phát biểu nào sau đây sai?
Trong các phản ứng hóa học, chỉ có các electron thuộc lớp ngoài cùng và phân lớp sát lớp ngoài cùng tham gia vào quá trình tạo thành liên kết (electron hóa trị).
Hợp chất nào sau đây là hợp chất cộng hóa trị?
- Các hợp chất CaO, NaCl, KCl là các hợp chất ion được hình thành từ kim loại điển hình và phi kim điển hình Là hợp chất ion.
- HCl là hợp chất cộng hóa trị. Nguyên tử hydrogen liên kết với nguyên tử chlorine bằng cách mỗi nguyên tử góp chung 1 electron tạo thành 1 cặp electron dùng chung trong phân tử HCl.
Trong các phân tử sau, phân tử nào có nguyên tử trung tâm không có cấu hình electron bền của khí hiếm?
Quy tắc octet chỉ đúng cho sự tạo thành liên kết hoá học giữa các nguyên tử của các nguyên tố thuộc chu kì 2 của bảng tuần hoàn và một số nguyên tử của các nguyên tố có tính kim loại, phi kim điển hình. Ngoài ra có các ngoại lệ.
Trong phân tử PCl5, lớp ngoài cùng của P có 10 electron.
Cho các phát biểu sau phát biểu nào là đúng khi nói về các loại liên kết?
a, Liên kết hydrogen yếu hơn liên kết ion và liên kết cộng hóa trị.
b, Liên kết hydrogen mạnh hơn liên kết ion và liên kết cộng hóa trị
c, Tương tác van der Waals yếu hơn liên kết hydrogen.
d, Tương tác van der Waals mạnh hơn liên kết hydrogen.
Các phát biểu đúng là: a và c.
H2O có nhiệt độ sôi và độ tan trong nước tốt hơn CH4 vì lí do nào sau đây?
H2O có nhiệt độ sôi và độ tan trong nước tốt hơn CH4 vì H2O có liên kết hydrogen, còn CH4 thì không có.
Liên kết cộng hóa trị là liên kết
Liên kết cộng hóa trị là liên kết được tạo thành giữa 2 nguyên tử bằng một hay nhiều cặp electron chung.
Phát biểu nào sau đây không đúng?
Liên kết ion thường được tạo thành từ các nguyên tử kim loại điển hình và phim kim điển hình.
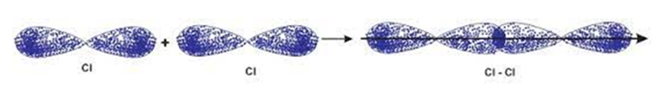
Liên kết hóa học trong phân tử nào sau đây được hình thành từ sự xen phủ trục p – p?
Liên kết trong phân tử Cl 2 được hình thành nhờ sự xen phủ bên p – p.
Sodium chloride là một hợp chất có thể tan trong nước lạnh và có nhiệt độ nóng chảy cao (801oC). Liên kết trong phân tử sodium chloride là
Liên kết trong phân tử sodium chloride là liên kết ion
Cho ion Al3+ và SO42-. Công thức của hợp chất ion được tạo thành từ 2 ion đã cho là
Công thức của hợp chất ion được tạo thành từ 2 ion đã cho có dạng: Alx(SO4)y
Tổng điện tích của các ion trong hợp chất bằng 0 nên ta có:
3x + (-2).y = 0
⇒ 3x = 2y
⇒
⇒ Lấy x = 2; y = 3
Vậy công thức là: Al2(SO4)3
Độ âm điện của các phi kim giảm dần theo thứ tự F, Cl, Br, H. Lực kéo electron về phía nguyên tử nitrogen mạnh nhất ở liên kết nào dưới đây?
Do nguyên tử H có độ âm điện nhỏ nhất nên lực kéo electron về phía nguyên tử nitrogen mạnh nhất ở liên kết N – H.
Nếu giữa các phân tử chất tan và dung môi có thể tạo thành liên kết hydrogen hoặc tương tác van der waals càng mạnh với nhau thì tan càng tốt vào nhau. Lí do nào sau đây phù hợp để giải thích dầu hỏa (thành phần chính là hydrocacbon) không tan vào nước?
Dầu hoả (thành phần chính là hydrocarbon) không tan trong nước do nước là phân tử phân cực và dầu là không/ ít phân cực.
Liên kết ion là loại liên kết phổ biến trong
Liên kết ion là loại liên kết phổ biến trong các hợp chất được tạo nên từ kim loại điển hình và phi kim điển hình.
Ví dụ: Khi kim loại potasssium kết hợp với phi kim oxygen, tạo thành các ion Ba2+ và O2–, các ion này có điện tích trái dấu sẽ hút nhau tạo thành liên kết ion
Phát biểu nào sau đây sai về các liên kết được tạo thành bởi sự xen phủ các orbital nguyên tử
Liên kết ba gồm một liên kết σ và hai liên kết π
M thuộc nhóm IIA, X thuộc nhóm VIA. Trong oxit cao nhất M chiếm 71,43% khối lượng, còn X chiếm 40% khối lượng. Liên kết giữa X và M trong hợp chất thuộc loại liên kết nào sau đây?
M thuộc nhóm IIA oxit cao nhất của M có dạng MO.
⇒ MM = 40 (Ca)
Oxit của X có dạng XO3
Tương tự, ta có:
⇒ Công thức hóa học của hợp chất tạo bởi M và X là: CaS
⇒ Hợp chất có liên kết ion .
Giữa H2O và C2H5OH có thể tạo ra bao nhiêu kiểu liên kết hydrogen?
Giữa H2O và C2H5OH có thể tạo ra 4 kiểu liên kết hydrogen
H2O và H2O
H2O và C2H5OH
C2H5OH và C2H5OH
C2H5OH và H2O.
