Oxi hóa FeS bằng axit HNO3 thu được sản phẩm là Fe(NO3)3, H2SO4, NO2. Vậy một phân tử FeS sẽ
Xác định số sự thay đổi số oxi hóa của FeS
FeS → Fe+3 + S+6 + 9e
Vậy một phân tử FeS nhường 9 electron.
Oxi hóa FeS bằng axit HNO3 thu được sản phẩm là Fe(NO3)3, H2SO4, NO2. Vậy một phân tử FeS sẽ
Xác định số sự thay đổi số oxi hóa của FeS
FeS → Fe+3 + S+6 + 9e
Vậy một phân tử FeS nhường 9 electron.
Cho quá trình: Mn+7 +5e → Mn+2 đây là quá trình?
Mn+7 +5e → Mn+2 đây là quá trình quá trình nhận e
→ Đây là quá trình khử.
Cho phương trình phản ứng:
a Al + b H2SO4 → c Al2(SO4)3 + d SO2 + e H2O.
Tỉ lệ a:b là:
2Al + 6H2SO4 → Al2(SO4)3 + 3SO2 + 6H2O.
Tỉ lệ a : b = 2 : 6 = 1 : 3.
Phản ứng hoá học mà SO2 không giữ là chất oxi hoá, cũng không là chất khử là phản ứng nào?
Phản ứng SO2 + 2KOH → K2SO3 + H2O. SO2 không giữ là chất oxi hoá, cũng không là chất khử vì S trong hợp chất không có sự thay đổi số oxi hóa
S+4O2 + 2KOH → K2S+4O3 + H2O
Trong phản ứng: 2NO2 + 2NaOH → NaNO3 + NaNO2 + H2O. NO2 đóng vai trò là:
Sự thay đổi số oxi hóa các chất trong phản ứng:
2N+4O2 + 2NaOH → NaN+5O3 + NaN+3O2 + H2O
⇒ NO2 vừa là chất oxi hóa, vừa là chất khử
Chất nào sau đây chỉ có tính khử?
Chất chỉ có tính khử khi chỉ có khả năng nhường eletcron.
⇒ Fe là chất chỉ có tính khử.
Phản ứng nào sau đây có thể tự xảy ra ở điều kiện thường?
Phản ứng giữa Mg và dung dịch H2SO4 loãng xảy ra ở nhiệt độ thường
Mg + H2SO4 → MgSO4 + H2
Dấu hiệu để nhận ra một phản ứng oxi hóa - khử là
Dấu hiệu để nhận ra một phản ứng oxi hóa - khử là có sự thay đổi số oxi hóa của một hay một số nguyên tố.
Cho sơ đồ phản ứng : Fe3O4 + HNO3 → Fe(NO3)3 + NO + H2O
Sau khi cân bằng, hệ số lần lượt của các chất là phương án nào sau đây?
Sự thay đổi số oxi hóa của các nguyên tử nguyên tố trước và sau phản ứng:
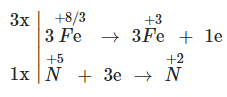
Cân bằng: 3Fe3O4 + 28HNO3 → 9Fe(NO3)3 + NO + 14H2O
Hệ số cân bằng của các phân tử là: 3, 28, 9, 1, 14
Số oxi hóa của nguyên tố hydrogen trong hydrogen chloride bằng:
Số oxi hóa của hydrogen trong HCl là +1
Hãy cho biết dãy nào sau đây số oxi hóa của nguyên tố hydrogen luôn là +1?
Dãy có số oxi hóa của nguyên tố hydrogen luôn là +1 là HF, H2O2, C2H2, NH3
Số oxy hóa của nguyên tử sulfur trong các ion sau: S2-, HSO4- lần lượt là:
S2- là ion đơn nguyên tử có điện tích là 2- ⇒ Số oxi hóa của ion S trong S2- là -2
HSO4-: gọi số oxi hóa của S trong ion là x.
Ta có: (+1).1 + x.1 + (-2).4 = -1
⇒ x = +6
Xét phản ứng: 4NH3 + 5O2 → 4NO + 6H2O. Cần trộn 1 thể tích khí ammonia với bao nhiêu thể tích không khí để thực hiện phản ứng trên? Biết không khí chứa 21% thể tích oxygen và các thể tích khí đo ở cùng điều kiện về nhiệt độ và áp suất.
Phương trình hóa học: 4NH3 + 5O2 → 4NO + 6H2O.
Theo phương trình hóa học:
Không khí chứa 21% thể tích oxygen.
Thể tích không khí là:
Quá trình oxi hóa là quá trình
Quá trình oxi hóa (sự oxi hóa) là quá trình nhường electron.
Cho 16,2 gam Aluminium tác dụng vừa đủ với 3,8 lít dung dịch HNO3, phản ứng tạo ra muối nhôm và một hỗn hợp khí gồm NO và N2O (là sản phẩm khử, ngoài ra không còn sản phẩm khử nào khác). Tính nồng độ mol của dung dịch HNO3. Biết rằng tỉ khối của hỗn hợp khí đối với hydrogen bằng 19,2. (cho biết NTK của N = 14, O = 16; Al = 27, H =1)
Cho 16,2 gam Aluminium tác dụng vừa đủ với 3,8 lít dung dịch HNO3, phản ứng tạo ra muối nhôm và một hỗn hợp khí gồm NO và N2O (là sản phẩm khử, ngoài ra không còn sản phẩm khử nào khác). Tính nồng độ mol của dung dịch HNO3. Biết rằng tỉ khối của hỗn hợp khí đối với hydrogen bằng 19,2. (cho biết NTK của N = 14, O = 16; Al = 27, H =1)
Gọi x, y lần lượt là số mol của NO và N2O
Ta có: nAl = 16,2 : 27 = 0,6 (mol)
Bảo toàn electron ta có:
3nAl = 3nNO + 8nN2O
⇔ 3.0,6 = 3x + 8y (1)
Phương trình khối lượng mol.
Giải hệ phương trình (1) và (2) ta được: x = 0,12; y = 0,18 mol
Áp dụng công thức tính nhanh ta có
nHNO3 = 4nNO + 10nN2O = 4.0,12 + 10.0,18 = 2,28 (mol)
CM = n:V = 2,28 : 3,8 = 0,6M
Hợp chất sắt đóng vai trò chất oxi hóa trong phản ứng:
Fe+2SO4 + Mg → MgSO4 + Fe0. (META)
Số oxi hóa Fe trong hợp chất từ +2 xuống 0. Nên FeSO4 đóng vai trò là chất oxi hóa
Dựa vào số oxi hóa của nguyên tử Cl hay S, chất nào dưới đây chỉ có tính oxi hoá?
Trong hợp chất HClO4, nguyên tử Cl có số oxi hóa +7 là lớn nhất ⇒ Hợp chất chỉ có tính oxi hóa.
Xét phản ứng: SO2 + Br2 + H2O → 2HBr + H2SO4. Vai trò của SO2 trong phản ứng là
Br từ số oxi hóa 0 xuống -1 → Br2 là chất oxi hóa; S từ +4 lên S+6 → SO2 là chất khử.
Xét phản ứng: MnO2 + 4HCl ![]() MnCl2 + Cl2 + H2O
MnCl2 + Cl2 + H2O
Phát biểu nào sau đây không đúng?
Cứ 4 phân tử HCl tham gia phản ứng thì 2 phân tử đóng vai trò là chất khử, hai phân tử đóng vai trò là chất tạo môi trường.
Trong phân tử NH4NO3 thì số oxi hóa của 2 nguyên tử nitrogen là :
Áp dụng quy tắc xác định số oxi hóa của các nguyên tử trong phân tử ta có:
