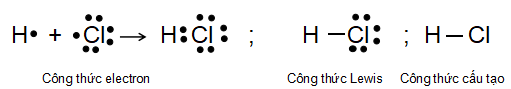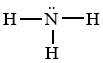Cho biết năng lượng liên kết của H–F là 565 KJ mol-1; H–Cl là 431 kJ mol-1; H–Br là 364 kJ mol-1; H–I là 297 kJ mol-1.
a) HF, HCl, HBr, HI tạo được liên kết hydrogen với các phân tử cùng loại. Sai||Đúng
b) Khi đun nóng, HI bị phân hủy (thành H2và I2) ở nhiệt độ thấp hơn so với HBr (thành H2và Br2). Đúng||Sai
c) Liên kết H – I là bền vững hơn so với liên kết H – Br. Sai||Đúng
d) Độ dài liên kết của H-Cl lớn hơn của H-Br. Sai||Đúng
Đáp án là:
Cho biết năng lượng liên kết của H–F là 565 KJ mol-1; H–Cl là 431 kJ mol-1; H–Br là 364 kJ mol-1; H–I là 297 kJ mol-1.
a) HF, HCl, HBr, HI tạo được liên kết hydrogen với các phân tử cùng loại. Sai||Đúng
b) Khi đun nóng, HI bị phân hủy (thành H2và I2) ở nhiệt độ thấp hơn so với HBr (thành H2và Br2). Đúng||Sai
c) Liên kết H – I là bền vững hơn so với liên kết H – Br. Sai||Đúng
d) Độ dài liên kết của H-Cl lớn hơn của H-Br. Sai||Đúng
a) Sai vì
Chỉ có HF mới tạo được liên kết hydrogen với các phân tử cùng loại; còn HCl, HI, HBr, thì không.
b) Đúng.
c) Sai vì
Giá trị năng lượng liên kết là thức đo độ bền liên kết nên năng lượng liên kết càng lớn thì liên kết càng bền.
→ So sánh độ bền liên kết: H–F > H–Cl > H–Br > H–I.
d) Sai vì
Liên kết càng bền thì độ dài liên kết càng ngắn
Độ dài liên kết HCl ngắn hơn của HBr.
eA + 3.eB + 2 = 42
pA + 3.pB = 40
nA = pA ; nB = pB
pA = 16 (S) và pB = 8 (O) vì hạt nhân S và O có số p = số n
hợp chất C là SO2
Liên kết trong C là liên kết cộng hóa trị có cực.