Trong thực tế, người ta sử dụng chất nào sau dây trong đèn xì để hàn, cắt kim loại?
Đốt cháy C2H2 sinh ra lượng nhiệt rất lớn, ứng dụng trong đèn xì để hàn cắt kim loại:
C2H2(g) + 5/2 O2(g) → 2CO2(g) + H2O = -1300,2 kJ
Trong thực tế, người ta sử dụng chất nào sau dây trong đèn xì để hàn, cắt kim loại?
Đốt cháy C2H2 sinh ra lượng nhiệt rất lớn, ứng dụng trong đèn xì để hàn cắt kim loại:
C2H2(g) + 5/2 O2(g) → 2CO2(g) + H2O = -1300,2 kJ
Nung KNO3 lên 550oC xảy ra phản ứng:
KNO3(s) ![]() KNO2(s) +
KNO2(s) + ![]() O2(g)
O2(g) ![]()
Phản ứng nhiệt phân KNO3 là
Phản ứng cần cung cấp nhiệt và luôn duy trì mới xảy ra
Phản ứng thu nhiệt có
> 0.
Ở mỗi ý a), b), c), d) hãy chọn đúng hoặc sai.
NaHCO3 (Baking soda) có trong thành phần của thuốc trị đau dạ dày Nabica, xét phản ứng nhiệt phân NaHCO3 xảy ra như sau:
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l) có ![]() = +91,6 kJ
= +91,6 kJ
a) Cần tránh để bột nở ở nơi có nhiệt độ cao. Đúng || Sai
b) Phản ứng trên thu vào một lượng nhiệt bằng 91,6 kJ. Đúng || Sai
c) Nếu thay đổi trạng thái của H2O(l) bằng H2O(g) thì giá trị ![]() vẫn không đổi. Sai || Đúng
vẫn không đổi. Sai || Đúng
d) Phản ứng trên có ![]() (cđ) <
(cđ) < ![]() (sp). Đúng || Sai
(sp). Đúng || Sai
Ở mỗi ý a), b), c), d) hãy chọn đúng hoặc sai.
NaHCO3 (Baking soda) có trong thành phần của thuốc trị đau dạ dày Nabica, xét phản ứng nhiệt phân NaHCO3 xảy ra như sau:
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l) có = +91,6 kJ
a) Cần tránh để bột nở ở nơi có nhiệt độ cao. Đúng || Sai
b) Phản ứng trên thu vào một lượng nhiệt bằng 91,6 kJ. Đúng || Sai
c) Nếu thay đổi trạng thái của H2O(l) bằng H2O(g) thì giá trị vẫn không đổi. Sai || Đúng
d) Phản ứng trên có (cđ) <
(sp). Đúng || Sai
a) đúng. Do = +91,6 kJ > 0 nên phản ứng này thu nhiệt, khi gặp nhiệt độ cao bột nở NaHCO3 dễ dàng bị phân hủy.
b) đúng.
c) sai. của H2O(l) và H2O(g) có giá trị khác nhau ⇒ nếu thay đổi trạng thái của H2O(l) bằng H2O(g) thì giá trị
thay đổi.
d) đúng.
Ta có:
=
(sp) –
(cđ) ⇒
(sp) –
(cđ) > 0
⇒ (sp) >
(cđ)
Đâu là phản ứng toả nhiệt dưới đây?
Nước đóng băng, cần tỏa nhiệt ra môi trường, để giảm nhiệt độ và chuyển sang thể rắn.
Số lượng mỗi loại liên kết trong phân tử C2H4 là:
Công thức cấu tạo của C2H4 là:
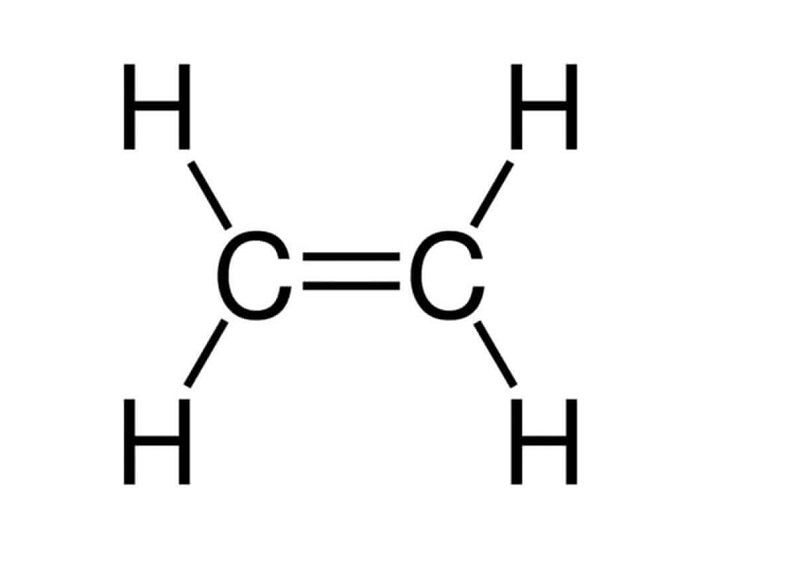
Số lượng mỗi loại liên kết trong phân tử C2H4 là: 4 liên kết C - H, 1 liên kết C = C.
Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
Cho các chất sau, chất nào có ![]() ≠0?
≠0?
Hợp chất có ≠0.
Enthalpy tạo thành của một chất (ΔfH) là nhiệt kèm theo phản ứng tạo thành
Enthalpy tạo thành của một chất (ΔfH) là nhiệt kèm theo phản ứng tạo thành 1 mol chất đó từ các đơn chất bền nhất.
Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết khi các chất ở trạng thái nào?
Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết khi các chất đều ở thể khí.
Cho phản ứng sau: CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (g). Công thức tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành chuẩn của các chất là
Phản ứng: CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (g)
Biến thiên enthalpy của phản ứng tính theo nhiệt tạo thành chuẩn:
Nhiệt tạo thành chuẩn (![]() ) của các đơn chất ở dạng bền vững nhất là
) của các đơn chất ở dạng bền vững nhất là
Nhiệt tạo thành chuẩn ( ) của các đơn chất ở dạng bền vững nhất là 0 kJ/mol.
Cho phương trình nhiệt hoá học của phản ứng:
2FeS(s) + 7/2O2(g) → Fe2O3(s) + 2SO2(g) ![]() = –1219,4 kJ.
= –1219,4 kJ.
Phản ứng trên là phản ứng
Phản ứng có = –1219,4 kJ < 0
⇒ Phản ứng là phản ứng tỏa nhiệt.
Phản ứng thu nhiệt là gì?
Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt
Một bình gas (khí hoá lỏng) chứa hỗn hợp propane và butane với tỉ lệ số mol 1 : 2. Cho biết các phản ứng:
C3H8(g) + 5O2(g) ⟶ 3CO2(g) + 4H2O(g) ![]() = –2220 kJ
= –2220 kJ
C4H10(g) + O2(g) ⟶ 4CO2(g) + 5H2O(g) ![]() = –2874 kJ
= –2874 kJ
Trung bình mỗi ngày, một hộ gia đình cần đốt gas để cung cấp 10 000 kJ nhiệt (hiệu suất hấp thụ nhiệt là 80%). Sau bao nhiêu ngày hộ gia đình trên sẽ sử dụng hết bình gas 12 kg?
Gọi a là số mol của propane trong bình gas ⇒ 2a là số mol của butane trong bình gas.
Theo bài, ta có:
44a + 58.2a = 12.1000 ⇒ a = 75 mol
Tổng nhiệt lượng tỏa ra khi đốt cháy hoàn toàn một bình gas là:
75.2220 + 2.75.2874 = 597600 kJ
Số ngày mà hộ gia đình sử dụng hết bình gas là:
Phản ứng đốt cháy 2 mol khí hydrogen bằng 1 mol khí oxygen, tạo thành 2 mol nước ở trạng thái lỏng được biểu diễn như sau:
2H2(g) + O2(g) → 2H2O(l) ![]()
Nhận xét nào sau đây là đúng?
2H2(g) + O2(g) → 2H2O(l)
Ta thấy
phản ứng tỏa nhiệt.
Vậy phản ứng trên tỏa ra nhiệt lượng là 571,6 kJ.
Điều chế NH3 từ N2(g) và H2(g) làm nguồn chất tải nhiệt, nguồn để điều chế nitric acid và sản xuất phân urea. Xác định nhiệt tạo thành chuẩn của NH3, biết khi sử dụng 7 gam khí N2 sinh ra 22,95 kJ nhiệt.
nN2 = 0,25 (mol)
N2(g) + 3H2(g) → 2NH3(g)
Ta có: 0,25 mol N2 phản ứng sinh ra 22,95 kJ nhiệt.
⇒ 1 mol N2 phản ứng sinh ra = 91,8 kJ nhiệt.
⇒ Cứ 2 mol NH3 tạo thành sinh ra 91,8 kJ nhiệt.
Vậy: 1 mol NH3 tạo thành sinh ra = 45,9 kJ nhiệt.
Phản ứng tỏa nhiệt nên: = –45,9 kJ.
Cho các phản ứng sau đâu là phản ứng không tỏa nhiệt?
Phản ứng không tỏa nhiệt là: Fe + 2HCl → FeCl2 + H2
Để làm nóng khẩu phần ăn, người ta dùng phản ứng giữa CaO với H2O:
CaO(s) + H2O(l) → Ca(OH)2(aq) ∆H = -105 kJ
Số gam CaO vào 250g H2O để nâng nhiệt độ từ 20oC lên 80oC?
Q = m.c. ∆T = 250.4,2.(80 – 20) = 63 000 J = 63 (kJ)
(Với 4,2 (J/g.K) là nhiệt dung riêng của nước)
1 mol CaO tương đương 56 gam CaO phản ứng tỏa ra nhiệt lượng là 105 kJ
Số gam CaO cần để tỏa ra nhiệt lượng 63 kJ là
Phương trình hóa học nào dưới đây biểu thị enthalpy tạo thành chuẩn của CO(g)?
Enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) của một chất là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất dạng bền nhất trong điều kiện chuẩn.
Vậy phương trình biểu thị enthalpy tạo thành chuẩn của CO(g) là:
C(than chì) + O2(g) → CO(g).
Nung nóng hai ống nghiệm chứa NaHCO3 và P, xảy ra các phản ứng sau:
2NaHCO3(s) → Na2CO3(s) + CO2(g) +H2O(g) (1)
4P(s) + 5O2(g) → 2P2O5(s) (2)
Khi ngừng đun nóng, phản ứng (1) dừng lại còn phản ứng (2) tiếp tục xảy ra, chứng tỏ
Khi ngừng đun nóng, phản ứng (1) dừng lại ⇒ Phản ứng (1) là phản ứng thu nhiệt.
Khi ngừng đun nóng, phản ứng (2) tiếp tục xảy ra ⇒ Phản ứng (2 là phản ứng tỏa nhiệt.
