Trong quy trình sản xuất benzene từ hexane, hiệu suất 50%, để sản xuất 19,5 kg benzene cần lượng hexane là:
Sơ đồ phản ứng:
C6H14 → C6H6
86kg → 78kg
Trong quy trình sản xuất benzene từ hexane, hiệu suất 50%, để sản xuất 19,5 kg benzene cần lượng hexane là:
Sơ đồ phản ứng:
C6H14 → C6H6
86kg → 78kg
Trong các phát biểu sau, hãy chọn đúng hoặc sai.
(1) Toluene (C6H5CH3) không tác dụng được với nước bromine, dung dịch thuốc tím ở điều kiện thường. Đúng||Sai
(2) Styrene (C6H5CH=CH2) tác dụng được với nước bromine, làm mất màu dung dịch thuốc tím ở điều kiện thường. Đúng||Sai
(3) Ethylbenzene (C6H5CH2CH3) không tác dụng được với nước bromine, làm mất màu dung dịch thuốc tím ở điều kiện thường. Sai||Đúng
(4) Naphthalene (C10H8) tác dụng được với nước bromine, làm mất màu dung dịch thuốc tím ở điều kiện thường. Sai||Đúng
Trong các phát biểu sau, hãy chọn đúng hoặc sai.
(1) Toluene (C6H5CH3) không tác dụng được với nước bromine, dung dịch thuốc tím ở điều kiện thường. Đúng||Sai
(2) Styrene (C6H5CH=CH2) tác dụng được với nước bromine, làm mất màu dung dịch thuốc tím ở điều kiện thường. Đúng||Sai
(3) Ethylbenzene (C6H5CH2CH3) không tác dụng được với nước bromine, làm mất màu dung dịch thuốc tím ở điều kiện thường. Sai||Đúng
(4) Naphthalene (C10H8) tác dụng được với nước bromine, làm mất màu dung dịch thuốc tím ở điều kiện thường. Sai||Đúng
(1) đúng.
(2) đúng.
(3) sai. Ethylbenzene (C6H5CH2CH3) không tác dụng được với nước bromine, làm mất màu dung dịch thuốc tím khi đun nóng.
(4) sai. Naphthalene (C10H8) không tác dụng được với nước bromine và không làm mất màu dung dịch thuốc tím ở điều kiện thường.
Cho các chất sau: (1) benzene; (2) toluene; (3) cyclohexane; (4) hex-5-triene; (5) xylene; (6) cumene. Dãy gồm các hydrocarbon thơm là:
Các hydrocarbon thơm là: (1) benzene; (2) toluene; (5) xylene; (6) cumene
Hỗn hợp X gồm C2H2 và H2 có cùng số mol. Lấy một lượng hỗn hợp X cho qua chất xúc tác, nung nóng thu được hỗn hợp Y gồm C2H2, C2H6, C2H4 và H2 dư. Dẫn Y qua bình nước bromine dư, thấy bình tăng 10,8 gam và thoát ra 4,48 lít hỗn hợp khí Z (đktc) có tỉ khối so với H2 bằng 8. Thể tích O2 (đktc) cần để đốt cháy hoàn toàn hỗn hợp Y trên là:
Gọi số mol C2H2 và số mol H2 ban đầu là a:
Bảo toàn khối lượng: mX = mY = mbình bromine tăng + m khí thoát ra
⇒ 26a + 2a = 10,8 + 0,2.8.2
⇒ a = 0,5 mol
Đốt X và Y tiêu tốn lượng O2 bằng nhau nên:
C2H2 + 5/2O2 2CO2 + H2O
H2 + 1/2O2 H2O
⇒ nO2 = 2,5a + 0,5a = 1,5 mol
⇒ V = 33,6 lít
Phản ứng nào sau đây không phải là phản ứng đặc trưng của hydrocarbon không no?
Phản ứng thế không phải là phản ứng đặc trưng của hydrocarbon không no.
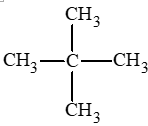
Alkane X có công thức phân tử C5H12. Xác định tên gọi của X, biết X chỉ có thể tạo ra một dẫn xuất monochloro duy nhất.
X chỉ có thể tạo ra một dẫn xuất monochloro duy nhất do đó chỉ có thể là:
2,2 – dimethylpropane.
Ứng với công thức C5H8 có bao nhiêu đồng phân alkyne?
Các đồng phân alkyne C5H8 là:
CH≡C−CH2−CH2−CH3
CH3−C≡C−CH2−CH3
CH≡C−CH(CH3)−CH3
Tính chất nào sau đây không phải đặc trưng của alkene.
Alkene không tan hoặc rất ít tan trong nước, tan trong một số dung môi hữu cơ
Đốt cháy hoàn toàn V lít (đktc) một ankin thu được 16,2 gam H2O. Tất cả sản phẩm cháy cho hấp thụ hết vào bình nước vôi trong thấy khối lượng bình tăng 69 gam. V có giá trị là:
nH2O = 0,9 mol
Bình nước vôi trong hấp thụ CO2 và nước nên:
mtăng = 69 gam = mCO2 + mH2O
nankin = nCO2 – nH2O = 1,2 – 0,9 = 0,3 mol
→ V = 0,3.22,4 = 6,72 lít
Một alkanen A có tỉ khối hơi so với không khí bằng 2, alkane đó là:
Gọi công thức phân tử của ankan là CnH2n+2
Ta có:
12n + 2n + 2 = 58
n = 4. (C4H10)
Chất nào sau đây có đồng phân hình học:
Chất có đồng phân hình học là: CH3 – CH = CH – CH3
Công thức nào sau đây là công thức tổng quát của hydrocarbon no không có mạch vòng?
Công thức nào sau đây là công thức tổng quát của hydrocarbon no không có mạch vòng CnH2n+2.
Alkane X có chứa 82,76% carbon theo khối lượng. Số nguyên tử hydrogen trong một phân tử X là
Gọi công thức phân tử của X là CnH2n+2:
(C4H10)
Vậy X có 10 nguyên tử H trong phân tử
Số đồng phân alkene ứng với công thức C5H10 là:
CH2 = CH – CH2 – CH2 – CH3
CH3 – CH= CH – CH2 – CH3
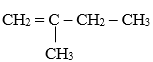
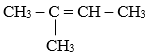
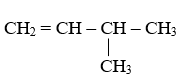
CH3–CH=CH–CH2–CH3: pent-2-ene có đồng phân hình học:
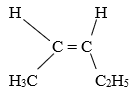
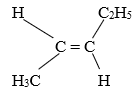
(CH3)2CH-CH3 có tên theo danh pháp thay thế là

(CH3)2CH-CH3 có tên theo danh pháp thay thế là 2-methylpropane.
Nitro hóa benzene bằng hỗn hợp HNO3 đặc và H2SO4 đặc ở nhiệt độ không quá 50oC, tạo thành chất hữu cơ X. Phát biểu nào sau đây về X không đúng?
X là nitrobenzene lỏng có màu vàng, sánh như dầu không tan trong nước.
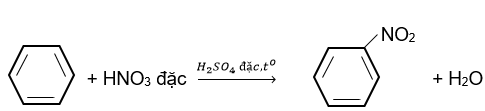
Ở các nước Mỹ, Úc và một số quốc gia khác, khí hoá lỏng (LPG – Liquefied Petroleum Gas) được sử dụng nhiều làm nhiên liệu là propane hoá lỏng, Em hãy tính xem một bình khí hoá lỏng chứa 12 kg propane có thể cung cấp bao nhiêu lít khí propane ở 25°C, 1 bar.
Ở các nước Mỹ, Úc và một số quốc gia khác, khí hoá lỏng (LPG – Liquefied Petroleum Gas) được sử dụng nhiều làm nhiên liệu là propane hoá lỏng, Em hãy tính xem một bình khí hoá lỏng chứa 12 kg propane có thể cung cấp bao nhiêu lít khí propane ở 25°C, 1 bar.
Công thức phân tử propane là C3H8
nC3H8 = 12.1000 : 44 = 3000/11 (mol)
VC3H8 = 3000:11 x 24,79 = 6761 L
Khi điều chế ethylene trong phòng thí nghiệm từ ethyl alcohol với xúc tác sulfuric acid đặc ở nhiệt độ trên 170oC thì khí ethylene thu được thường có lẫn các oxide như CO2 và SO2. Để làm sạch ethylene phải dùng hoá chất nào dưới đây?
NaOH có tính kiềm mạnh nên hấp thụ rất tốt những oxide acid như CO2 và SO2.
Ở nội dung câu hỏi này không phải là phân biệt CO2 và SO2 nên ta không dung Br2 và KMnO4.
Cho phản ứng: C2H2 + H2O ![]() X
X
X là chất nào dưới đây
C2H2 + H2O [CH2=CHOH] → CH3CHO.
Dãy nào sau đây chỉ gồm các chất thuộc dãy đồng đẳng của methane?
Dãy chất chỉ gồm các chất thuộc dãy đồng đẳng của methane có công thức phân tử CnH2n – 2 (n ≥ 2):
Dãy chất thỏa mãn là: CH4, C2H6, C4H10, C5H12.
