Cho dãy chất: C3H6, C2H6, C2H4, C3H8, CH2=CH-Cl. Số chất tham gia phản ứng trùng hợp là?
Các chất có liên kết đôi có thể tham gia phản ứng trùng hợp:
C3H6, C2H4, CH2=CH-Cl.
Cho dãy chất: C3H6, C2H6, C2H4, C3H8, CH2=CH-Cl. Số chất tham gia phản ứng trùng hợp là?
Các chất có liên kết đôi có thể tham gia phản ứng trùng hợp:
C3H6, C2H4, CH2=CH-Cl.
Cho các chất sau: CH2=CH–CH2–CH2–CH=CH2; CH2=CH–CH=CH–CH2–CH3; CH3–C(CH3)=CH–CH3; CH2=CH–CH2–CH=CH2. Số chất có đồng phân hình học là:
Điều kiện để alkene có đồng phân hình học: Mỗi nguyên tử carbon ở liên kết đôi liên kết với 2 nguyên tử hoặc nhóm nguyên tử khác nhau.
Chất có đồng phân hình học là: CH2=CH–CH=CH–CH2–CH3.
Công thức cấu tạo CH3CH(CH3)CH2CH2CH3 ứng với tên gọi nào sau đây?
Tên theo danh pháp tháy thế của alkane mạch phân nhánh:
Vị trí nhóm thế alkyl - tên của nhóm thế alkyl tên alkane mạch chính
Tên alkane: 2-methylpentane.
Số đồng phân alkene ứng với công thức C5H10 là:
CH2 = CH – CH2 – CH2 – CH3
CH3 – CH= CH – CH2 – CH3
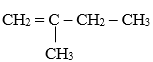
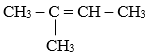
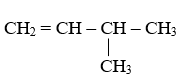
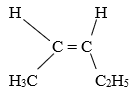
CH3–CH=CH–CH2–CH3: pent-2-ene có đồng phân hình học:
Cho sơ đồ phản ứng sau :
CH3–C≡CH + AgNO3/NH3 → X + NH4NO3
X có công thức cấu tạo là?
Phương trình phản ứng:
CH3–C≡CH + AgNO3/NH3 → CH3-C≡C-Ag + NH4NO3
Đốt cháy hoàn toàn hỗn hợp M gồm một alkane X và một alkyne Y, thu được số mol CO2 bằng số mol H2O. thành phần phần trăm về số mol của X và Y trong hỗn hợp m lần lượt là
Đốt cháy alkane: nalkane = nH2O – nCO2 (1)
Đốt cháy alkyne: nalkyne = nCO2 – nH2O (2)
Lấy (1) - (2) ta có:
nalkane - nalkyne = 2(nH2O – nCO2) mà nH2O = nCO2
nalkane = nalkyne = 50%
Alkene X hợp nước tạo thành 3-ethylpentan-3-ol. Tên của X là
Phương trình phản ứng:
CH3CH=C(C2H5)CH2CH3 + H2O CH3CH2C(OH)(C2H5)CH2CH3
(3-ethylpent-2-ene)
Craking 50 lít n-butane thu được 82,5 lít hỗn hợp A gồm H2, CH4, C2H4, C2H6, C3H6, C4H8 và một phần n-butane dư. Các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất. Giả sử chỉ có các phản ứng tạo ra các sản phẩm trên. Hiệu suất phản ứng tạo hỗn hợp A là:
Các khí ở cùng điều kiện nhiệt độ, áp suất nên:
VC4H10 phản ứng = Vkhí tăng = VA – VC4H10 bđ = 32,5 lít.
Chất (CH3)2CH–C6H5 có tên gọi là
Chất (CH3)2CH–C6H5 có tên gọi là iso-propylbenzene hay còn gọi là cumene.
Hai alkane X và Y kế tiếp nhau trong dãy đồng đẳng, có tổng khối lượng phân tử bằng 74. X và Y lần lượt là
Ta có:
MX + MY = 74 MX + (MX + 14) = 74
MX = 30 (C2H6)
MY = 44 (C3H8)
Vậy 2 alkane là ethane và propane.
Dẫn từ từ 6,72 lít (đktc) hỗn hợp X gồm ethene và propene vào dung dịch bromine, thấy dung dịch bromine bị nhạt màu và không có khí thoát ra. Khối lượng dung dịch sau phản ứng 9,8 gam. Thành phần phần trăm theo thể tích của ethene trong X là
nhh = 0,3 mol
Gọi số mol của C2H4 là x mol và C3H6 là y mol
⇒ x + y = 0,3 (1)
Khối lượng dung dịch sau phản ứng tăng là khối lượng của X:
⇒ 28x + 42y = 9,8 (2)
Từ (1) và (2) ⇒ x = 0,2 mol; y = 0,1 mol
Hợp chất hữu cơ nào sau đây thuộc dãy đồng đẳng alkane?
Dãy đồng đẳng của alkane có công thức chung CnH2n+2 (n 1).
C10H22 thuộc dãy đồng đẳng của alkane.
Cracking hoàn toàn 6,6 gam propane thu được 2 hydrocarbon X, Y. Cho toàn bộ hỗn hợp gồm X, Y qua 100 gam dung dịch Br2 thấy dung dịch mất màu. Khí bay ra có tỷ khối so với H2 là 9,5. Nồng độ % của Br2 là
nC3H8 = 6,6/44 = 0,15 mol
C3H8 CH4 + C2H4
0,15 → 0,15 → 0,15
Cho X, Y đi qua dung dịch bromine khí bay ra gồm 0,15 mol CH4 và 1 phần C2H4 dư (x mol)
⇒ x = 0,05
⇒ nBr2 = nC2H4 phản ứng = 0,15 – 0,05 = 0,1
Một hỗn hợp X gồm 0,12 mol C2H2 và 0,18 mol H2. Cho X đi qua Ni nung nóng, sau một thời gian thu được hỗn hợp khí Y. Cho Y vào bình đựng bromine dư, thấy bình bromine tăng m gam và thoát ra khí Z. Đốt cháy hết Z và cho toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư thấy có 5 gam kết tủa xuất hiện và thấy khối lượng dung dịch giảm 1,36 gam. Giá trị của m là:
Đốt cháy Z thu được sản phẩm gồm: CO2, H2O
Dẫn sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư:
nCO2 = nCaCO3 = 5/100 = 0,05 mol
Khối lượng dung dịch giảm 5 gam nên:
mdd↓ = mCaCO3 − (mCO2 + mH2O)
⇒ mH2O = 5 − 0,05.44 − 1,36 = 1,44 gam
⇒ nH2O = 0,08 mol
Bảo toàn C: nC = nCO2 = 0,05 mol
Bảo toàn H: nH = 2nH2O = 2.0,08 = 0,16 mol
Z được tạo bởi hai nguyên tố C và H nên:
mZ = mC + mH = 0,05.12 + 0,08.2 = 0,76 gam
Bảo toàn khối lượng:
mX = m + mZ
⇒ m = 0,12.26 + 0,18.2 − 0,76 = 2,72 gam.
Hydrocarbon nào sau đây khi phản ứng với dung dịch bromine thu được 1,2-dibromobutane?
1,2-dibromobutane là CH2Br-CHBr-CH2-CH3
Phương trình phản ứng:
CH2=CH-CH2 -CH3 + Br2 → CH2Br-CHBr-CH2-CH3
Nhựa PS được chế tạo từ
Nguyên liệu cho chế tạo nhựa PS (polystyrene) là styrene:
n-C6H5-CH=CH2 → (-CH2-CH(C6H5)-)n (tº, xt, p)
(Polystyrene- PS)
Cho 2,2 gam C3H8 tác dụng với 3,55 gam Cl2 thu được 2 sản phẩm thế monochloro X và dichloro Y với khối lượng mX = 1,3894mY. Sau khi cho hỗn hợp khí còn lại sau phản ứng (không chứa X, Y) đi qua dung dịch NaOH dư, còn lại 0,448 lít khí thoát ra (đktc). Khối lượng của X, Y lần lượt là:
Ta có: nC3H8ban đầu = 2,2/44 = 0,05 mol
nCl2 = 3,55/71 = 0,05 mol
C3H8 + Cl2 C3H7Cl + HCl
a a a a
C3H8 + 2Cl2 C3H6Cl2 + 2HCl
b 2b b 2b
Theo đề bài: mX = 1,3894mY
⇔ 78,5a = 1,3894.113b
⇔ a = 2b (1)
Khí còn lại đi ra khỏi dung dịch NaOH dư là C3H8
nC3H8dư = 0,448/22,4 = 0,02 mol
nC3H8pứ = nC3H8 ban đầu − nC3H8 dư
= 0,05 - 0,02 = 0,03 mol
a + b = 0,03 (2)
Từ (1) và (2) ta có: a = 0,02; b = 0,01.
nC3H7Cl = 0,02.78,5 = 1,57 gam
nC3H6Cl2 = 0,0.113 = 1,13 gam.
Chất có công thức cấu tạo: CH3-C(CH3)=CH-C≡CH có tên gọi là:
CH3-C(CH3)=CH-C≡CH có tên gọi là 4-methylhex-3-ene-1-yne.
Hỗn hợp X gồm H2 và C2H4 có tỷ khối so với H2 là 7,5. Dẫn X qua Ni nung nóng, thu được hỗn hợp Y có tỉ khối so với H2 là 12,5. Hiệu suất của phản ứng hydrogen hóa là
Gọi nX = x, nY = y.
Ta có: MX = 15 ⇒ 28x + 2y = 15(x+y)
⇒ x = y. (Hiệu suất tính theo một trong hai chất)
Giả sử: nX = 2 mol ⇒ nH2 = 1 mol; nC2H4 = 1 mol
⇒ mX = 28.1 + 2.1 = 30 gam
MY = 25 ⇒ 30/nY = 25 ⇒ nY = 1,2 mol
⇒ số mol giảm = nH2 pư = nalkene pư = 0,8 mol.
Styrene có công thức phân tử C8H8 và có công thức cấu tạo: C6H5–CH=CH2. Câu nào đúng khi nói về styrene?
Styrene là hydrocarbon thơm.
