Cồn 70° là dung dịch ethyl alcohol, được dùng để sát trùng vết thương. Mô tả nào sau đây về cồn 70° là đúng?
Cồn 70° là 100 mL dung dịch có 70 mL ethyl alcohol nguyên chất.
Cồn 70° là dung dịch ethyl alcohol, được dùng để sát trùng vết thương. Mô tả nào sau đây về cồn 70° là đúng?
Cồn 70° là 100 mL dung dịch có 70 mL ethyl alcohol nguyên chất.
Cho 68,913 gam 1 alcohol hai chức Z phản ứng hết với Na thu được 24,8976 lít H2 (đktc). Vậy Z là:
Phương trình phản ứng:
R(OH)2 + 2Na → R(ONa)2 + H2
nalcohol = nH2 = 1,1115 mol
Malcohol = 62 = 14n + 2 + 32
n = 2
Z là C2H6O2.
Dẫn xuất halogen bậc II có tên phù hợp là:
Cl–CH2–CH2–Cl: 1,2-dichloroethane
Bậc I.
CH3–CHl–CH3: 2-iodopropane.
Bậc II
CH3–CH(CH3)–CH2–Br: 1-bromo-2-methylpropane.
Bậc I.
FC(CH3)3: 2-fluoro-2-methylpropane
Bậc III
Khi đun nóng hỗn hợp methyl alcohol và ethyl alcohol với H2SO4 đặc ở 140oC có thể thu được số ether tối đa là
Ta có 2 alcohol khác nhau nên số ether tạo ra:
Các ether có thể thu được là: CH3OC2H5; C2H5OC2H5 và CH3OCH3
Cho các chất: C2H4(OH)2, CH2OH-CH2-CH2OH, CH3CH2CH2OH, C3H5(OH)3, C2H5OH. Có bao nhiêu chất phản ứng được với Cu(OH)2
Các polyalcohol có các nhóm -OH liền kề như ethylene glycol, glycol có thể tác dụng với Cu(OH)2 tạo dung dịch màu xanh lam đậm.
Vậy số chất phản ứng được với Cu(OH)2 ở nhiệt độ thường là 2: C3H5(OH)3, C2H4(OH)2
Cặp chất nào sau đây là đồng phân?
o-cresol: o-CH3-C6H4-OH
Benzyl alcohol: C6H5-CH2OH
Cả 2 chất đều có công thức phân tử là C7H8O nên là đồng phân của nhau.
Cho 30,8 gam hỗn hợp m-cresol và ethanol tác dụng với sodium dư thu được m gam muối và 0,2 mol khí H2 (đktc). Giá trị của m là
Đặt công thức tổng quát của hỗn hợp là ROH.
ROH + Na → RONa + 1/2H2.
0,4 ← 0,2 mol
Áp dụng định luật bảo toàn khối lượng ta có:
mROH + mNa = mmuối + mH2
⇔ 30,8 + 0,4.23 = mmuối + 0,2. 2
→ mmuối = 39,6 gam
M là hỗn hợp gồm 3 alcohol đơn chức X, Y, Z có số nguyên tử carbon liên tiếp nhau, đều mạch hở (MX < MY < MZ); X và Y no, Z không no (có 1 liên kết đôi C=C). Chia M thành 3 phần bằng nhau.
- Đốt cháy hoàn toàn phần 1 thu được 49,828 lít khí CO2 (đkc) và 46,44 gam H2O
- Phần 2 làm mất màu vừa đủ dung dịch chứa 16 gam Br2
- Đun nóng phần 3 với H2SO4 đặc ở 140oC thu được 18,752 gam hỗn hợp 6 ether (T). Đốt cháy hoàn toàn T thu được 1,106 mol CO2 và 1,252 mol H2O.
Hiệu suất tạo ether của X, Y, Z lần lượt là
Đốt phần 1 thu được: nCO2 = 2,01 mol và nH2O = 2,58 mol
Vì Z chứa 1 liên kết đôi đốt cháy Z thu được nH2O = nCO2
nX + nY = nH2O nCO2 = 0,57 mol
nM = 0,67
số C = 3
Vậy M chứa:
X là C2H5OH: 0,1 mol
Y là C3H7OH: 0,47 mol
Z là C4H7OH: 0,1 mol
(số C = 3 nên nX = nZ)
Đặt x, y, z là số mol X, Y, Z đã phản ứng:
Bảo toàn khối lượng: mX + mY + mZ = mether + mH2O
46x + 60y + 72z = 18,752 + 18.(x+y+z)/2 (1)
Đốt T thu được:
nCO2 = 2x + 3y + 4z = 1,106 (2)
nH2O = 3x + 4y + 4z −
Giải hệ (1), (2), (3) x = 0,05; y = 0,282; z = 0,04
H(X) = 50%; H(Y) = 60%; H(Z) = 40%
Công thức tổng quát của dẫn xuất monochlorine no, mạch hở là:
Công thức tổng quát của dẫn xuất monochlorine no, mạch hở là CnH2n+1Cl.
Đâu là alcohol thơm?
Alcohol là những hợp chất hữu cơ mà phân tử có nhóm –OH liên kết trực tiếp với nguyên tử C no (C no là C liên kết với các nguyên tử khác bằng liên kết đơn)
Alcohol thơm là alcohol có vòng benzene nhưng –OH không liên kết trực tiếp với vòng benzene.
Hydrate hóa 2 alkene chỉ tạo thành 2 alcohol. Hai alkene đó là
2 alkene có cấu tạo đối xứng khi hydrate hóa sẽ chỉ tạo thành 2 alcohol:
Ethene:
CH2=CH2 + H2O CH3-CH2-OH
But-2-ene:
CH3-CH=CH-CH3 + H2O CH3-CH2-CH(OH)-CH3
Cả phenol và ethyl alcohol đều phản ứng được với:
Cho các dung dịch sau: CH3COOH, C2H5ONa và H2O. Chỉ dùng một hóa chất nào sau đây có thể nhận biết được cả 3 chất ở trên:
Sử dụng quỳ tím để nhận biết 3 chất:
- CH3COOH làm quỳ tím hóa đỏ
- Trong dung dịch C2H5ONa thủy phân tạo ra môi trường bazo mạnh, làm quỳ tím hóa xanh.
C2H5ONa + H2O → C2H5OH + NaOH
- Nước không làm quỳ tím chuyển màu
X là dẫn xuất chlorine của ethane. Đun nóng X trong NaOH dư thu được chất hữu cơ Y vừa tác dụng với Na vừa tác dụng với Cu(OH)2 ở nhiệt độ thường. Vậy X là
Ta có Y vừa tác dụng với Na vừa tác dụng với Cu(OH)2 ở nhiệt độ thường nên:
Y có 2 nhóm -OH trong phân tử, Y là CH2OH-CH2OH
X là: CH2Cl-CH2Cl (1,2-dichloroethane)
CH2ClCH2Cl CH2OHCH2OH
CH2OHCH2OH CH2ONaCH2ONa
CH2OHCH2OH Cu(C2H5O2)2
Khử hợp chất hữu cơ X bằng LiAlH4, thu được (CH3)2CH-CH2-CH2OH. Chất X có tên là
Phương trình phản ứng
(CH3)2CH−CH2−CHO + 2[H] (CH3)2CH−CH2−CH2OH
Chất X là (CH3)2CH-CH2-CHO; có tên 3-methylbutanal.
Ứng dụng nào sau đây không còn được sử dụng?
Phân tích nguyên tố hợp chất hữu cơ X cho thấy phần trăm khối lượng ba nguyên tố C, H và O lần lượt là 64,86%; 13,51% và 21,63%. Phổ MS của X được cho như sau:
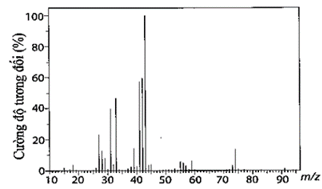
Phổ hồng ngoại của X có tín hiệu hấp thụ trong vùng 3650 - 3200 cm−1. Tính số công thức cấu tạo có thể có của X.
Gọi công thức đơn giản nhất của X là CxHyOz:
Theo bài ra ta có:
= 4 : 10 : 1
⇒ Công thức đơn giản nhất của X là C4H10O, công thức phân tử của X là (C4H10O)n.
Từ phổ MS của X cho thấy X có phân tử khối bằng 74.
⇒ 74n = 74 ⇒ n = 1. Vậy công thức phân tử của X là C4H10O.
Do trên phổ IR của X có tín hiệu ở vùng 3650 – 3200 cm−1 nên X là một alcohol.
Công thức cấu tạo có thể có của X là: CH3–CH2–CH2–CH2–OH, CH3–CH(OH)–CH2–CH3, (CH3)2CH–CH2–OH và (CH3)3–C–OH.
Phản ứng nào dưới đây là đúng?
Phản ứng đúng là: C6H5OH + NaOH → C6H5ONa + H2O.
Các phản ứng còn lại sai vì:
C2H5OH + NaOH → không xảy ra
C6H5ONa + CO2 + H2O → C6H5OH + NaHCO3
C6H5OH + HCl → không xảy ra
Phenol có thể phản ứng với dung dịch NaOH, chứng tỏ
Phenol có thể phản ứng với dung dịch NaOH, chứng tỏ phenol có tính acid.
Cho 54,5 g một alkyl chloride X tác dụng với dung dịch KOH trong C2H5OH đun nóng nhẹ, thu được V lít khí Y và 7,45 g muối Z. Xác định alkyl chloride X và thể tích khí thoát ra.
nKCl = 0,1 mol
Gọi công thức phân tử của alkyl chloride là CnH2n+1Cl
Phương trình hóa học:
CnH2n+1Cl + KOH CnH2n + KCl + H2O
0,1 ← 0,1 ← 0,1
Malkyl chloride = 5,45/0,1 = 54,5 (g/mol)
⇒ Công thức của X là C2H5Cl.
Thể tích khí thu được là:
VC2H4 = 0,1.24,79 = 2,479 lít
