Nguyên tố Sulfur có Z = 16. Sulfur là
Cấu hình electron của nguyên tử phosphorus (Z = 16): 1s22s22p63s23p4.
Số electron ở lớp ngoài cùng bằng 6.
⇒ Sulfur là nguyên tố phi kim.
Nguyên tố Sulfur có Z = 16. Sulfur là
Cấu hình electron của nguyên tử phosphorus (Z = 16): 1s22s22p63s23p4.
Số electron ở lớp ngoài cùng bằng 6.
⇒ Sulfur là nguyên tố phi kim.
Trong bảng tuần hoàn các nguyên tố, nguyên tố có tính phi kim mạnh nhất là
Trong bảng tuần hoàn các nguyên tố, nguyên tố có tính phi kim mạnh nhất là fluorine.
Cho các nguyên tố X (Z = 19); Y (Z = 8).
Viết cấu hình electron và xác định vị trí của X, Y trong bảng tuần hoàn (có giải thích); Chúng là nguyên tố phi kim, kim loại hay khí hiếm?
Cho các nguyên tố X (Z = 19); Y (Z = 8).
Viết cấu hình electron và xác định vị trí của X, Y trong bảng tuần hoàn (có giải thích); Chúng là nguyên tố phi kim, kim loại hay khí hiếm?
Cấu hình electron:
- X: 1s22s22p63s23p64s1
- Y: 1s22s22p4
Vị trí:
- X thuộc ô số 19, X có 1 e ở lớp ngoài cùng nên thuộc nhóm IA, X có 4 lớp electron nên thuộc chu kì 4.
- Tương tự, Y thuộc ô số 8, nhóm VIA, chu kì 2.
X có 1 electron lớp ngoài cùng ⇒ X là kim loại, Y có 6 electron lớp ngoài cùng ⇒ Y là phi kim.
Tính kim loại giảm dần trong dãy :
Trong cùng 1 nhóm tính kim loại tăng dần theo chiều tăng của điện tích hạt nhân do đó tính kim loại B < Al.
Trong cùng 1 chu kỳ tính kim loại giảm dần theo chiều tăng của điện tích hạt nhân do đó tính kim loại B > C, Mg > Al.
Tính kim loại giảm dần trong dãy: Mg, Al, B, C.
Ion R+ có tổng số hạt cơ bản là 57 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 17 hạt. Vị trí của R trong bảng tuần hoàn là
Theo bài ra R+ có:
p + (e – 1) + n = 57 R có 2p + n = 57 + 1 = 58
Trong R+ có : p + (e – 1) = n + 17 2p – n = 18
p = 19 và n = 20
R thuộc ô 19, chu kì 4, nhóm IA.
Nguyên tố X thuộc chu kì 3, nhóm IIIA. Nguyên tử của nguyên tố X có cấu hình electron là
X thuộc chu kì 3, nhóm IIIA nên có 3 lớp electron, lớp ngoài cùng có 3 electron.
Cấu hình electron của X là: 1s22s22p63s23p1.
Trong một chu kì, bán kính nguyên tử các nguyên tố
Trong một chu kì, bán kính nguyên tử các nguyên tố giảm theo chiều tăng dần của điện tích hạt nhân.
Nguyên tố Y có cấu hình electron lớp ngoài cùng 4s1 thuộc chu kì:
Nguyên tố Y có cấu hình electron lớp ngoài cùng 4s1 thuộc chu kì 4
X và Y là hai nguyên tố kế tiếp nhau trong cùng một nhóm A của bảng tuần hoàn. Biết rằng tổng số electron trong nguyên tử X và Y là 30, số electron của X nhỏ hơn số electron của Y. Phát biểu nào sau đây là sai?
Ta tính được eX = 9 và eY = 19
Cấu hình electron nguyên tử của X: 1s22s22p63s1
Cấu hình electron nguyên tử của Y: 1s22s22p63s23p64s1
X có 2 lớp electron bão hòa, Y có 3 lớp electron bão hòa.
Nguyên tử X có cấu hình electron [Ne]3s23p5. Vị trí của X trong bảng hệ thống tuần hoàn là
Cấu hình của nguyên tử X: 1s22s22p63s23p5
ZX = 17 X có số thứ tự 17.
X có 3 lớp electron ⇒ X ở chu kì 3;
X là nguyên tố p, có 7 electron lớp ngoài cùng ⇒ X ở nhóm VIIA;
Vị trí của X trong bảng tuần hoàn là ô thứ 17, chu kì 3, nhóm VIIA.
Nguyên tố magnesium thuộc ô số 12, chu kì 3, nhóm IIA. Viết cấu hình electron của magnesium
Nguyên tố magnesium (Mg) ở ô số 12, chu kì 3, nhóm IIA.
Suy ra:
Số hiệu nguyên tử Z = 12 = Số electron.
Số lớp electron = Số thứ tự chu kì = 3.
Số electron lớp ngoài cùng = Số thứ tự nhóm A = 2.
⇒ Cấu hình electron của nguyên tử magnesium (Mg): 1s22s22p63s2
Đại lượng nào của nguyên tố hóa học biến thiên tuần hoàn?
Số electron ở lớp ngoài cùng của nguyên tử biến thiên tuần hoàn.
Nguyên tử R có cấu hình electron lớp ngoài cùng là ns2np3. Trong hợp chất khí của R với hydrogen thì hydrogen chiếm 17,64% về khối lượng. R là
Nguyên tử R có cấu hình electron lớp ngoài cùng là ns2np3 ⟹ R thuộc nhóm VA. Hợp chất khí của R với H có công thức là RH3.
Ta có:
MR = 14
Vậy nguyên tố R là N.
Năm 1869, nhà hóa học đã công bố bảng tuần hoàn các nguyên tố hóa học là
Năm 1869, nhà hóa học đã công bố bảng tuần hoàn các nguyên tố hóa học là Mendeleev.
Nguyên tố nào sau đây có tính chất hóa học tương tự như nguyên tố Sodium (Z=11)?
Sodium: 1s22s22p63s1
Potassium: 1s22s22p63s23p64s1
Sodium (Z = 11), potassium (Z = 19) cùng thuộc nhóm IA nên có tính chất hóa học tương tự nhau.
Cho nguyên tố X, Y là hai nguyên tố cùng một nhóm A ở hai chu kì nhỏ liên tiếp nhau trong bảng tuần hoàn và ZX + ZY = 32 (ZX < ZY). Xác định nguyên tố X.
Gọi ZX, ZY lần lượt là số proton của nguyên tử nguyên tố X và Y. Ta có:
ZX + ZY = 32 (1)
Vì X và Y thuộc cùng nhóm A ở hai chu kì kế tiếp nhau nên số proton của chúng khác nhau 8, 18 hoặc 32 đơn vị.
Giả sử ZY > ZX.
Trường hợp 1: ZY – ZX = 8 (2)
Kết hợp (1) và (2) giải hệ phương trình ta được: ZX = 12; ZY = 20.
Cấu hình electron của X: 1s22s22p63s2 (nhóm IIA).
Cấu hình electron của Y: 1s22s22p63s23p64s2 (nhóm IIA).
Vậy trường hợp 1 thỏa mãn, X là magnesium (Mg) và Y là calcium (Ca).
Trường hợp 2: ZY – ZX = 18 (3)
Kết hợp (1) và (3) giải hệ phương trình ta được: ZX = 7; ZY = 25.
Cấu hình electron của X: 1s22s22p3 (nhóm VA)
Cấu hình electron của Y: 1s22s22p63s23p63d54s2 (nhóm VIIB)
Vậy trường hợp 2 không thỏa mãn.
Trường hợp 3: ZY – ZX = 32 (4)
Kết hợp (1) và (4) giải hệ phương trình ta được: ZX = 0; ZY = 32.
Vậy trường hợp 3 không thỏa mãn.
Nguyên tố s là nguyên tố mà
Các nguyên tố s, p, d, f là những nguyên tố mà nguyên tử có electron cuối cùng được điền vào phân lớp s, p, d, f tương ứng.
Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kì và có tổng số proton trong hai hạt nhân là 25. X và Y thuộc chu kì và nhóm nào trong bảng tuần hoàn?
Hai nguyên tố X và Y có tổng số proton trong hai hạt nhân là 25
⇒ ZY + ZX = 25 (1)
Hai nguyên tố X và Y đứng kế tiếp nhau trong một chu kì
⇒ ZY – ZX = 1 (2)
Từ (1) và (2) → ZY = 13; ZX = 12
⇒ Cấu hình electron của Y: 1s22s22p63s23p1
⇒ Y thuộc ô số 13, chu kì 3, nhóm IIIA.
Cấu hình electron của X: 1s22s22p63s2
⇒ X thuộc ô số 12, chu kì 3, nhóm IIA.
Anion X2– có cấu hình electron [Ne]3s23p5. Nguyên tố X có tính chất nào sau đây?
Nguyên tử X nhận thêm 2 electron để trở thành ion X2-
⇒ Cấu hình electron của nguyên tử X là: [Ne]3s23p3
X có 5 electron hóa trị ⇒ là phi kim.
Các khối nguyên tố d và f đều là
Các khối nguyên tố d và f đều là kim loại.
Công thức chung của các oxide kim loại nhóm IIA là
Công thức chung của các oxit kim loại nhóm IIA là RO.
Các nguyên tố X, Y, Z, K có số hiệu nguyên tử tương ứng là 6, 8, 16, 25. Kết luận nào dưới đây về vị trí nguyên tố trong bảng tuần hoàn là đúng?
X ( Z = 4): 1s22s22p2 → X thuộc chu kỳ 2 (do có 2 lớp electron); nhóm IVA (do có 2 electron hóa trị, nguyên tố s)
Y ( Z = 8): 1s22s22p4 → Y thuộc chu kỳ 2 (do có 2 lớp electron); nhóm VIA (do có 6 electron hóa trị, nguyên tố p)
Z (Z = 16): [Ne]3s23p4 → Z thuộc chu kỳ 3 (do có 3 lớp electron); nhóm VIA (do có 6 electron hóa trị, nguyên tố p)
K (Z = 25): [Ar]3d54s2 → K thuộc chu kỳ 4 (do có 4 lớp electron); nhóm VIIB (do có 7 electron hóa trị, nguyên tố d)
Ở trạng thái cơ bản, cấu hình electron của nguyên tử Na (Z = 11) là
Cấu hình electron của Na (Z = 11): 1s22s22p63s1
Độ âm điện của các nguyên tố Mg, Al, B và N xếp theo chiều tăng dần là
Mg và Al cùng thuộc một chu kì ⇒ Độ âm điện: Mg < Al
Al và B cùng thuộc một nhóm ⇒ Độ âm điện: Al < B
⇒ Độ âm điện Mg < Al < B (1)
Lại có N và B cùng thuộc một chu kì ⇒ Độ âm điện B < N (2)
Kết hợp (1) và (2). Độ âm điện của các nguyên tố xếp theo chiều tăng dần là:
Mg < Al < B < N.
X, Y, Z là 3 nguyên tố thuộc cùng một chu kì của bảng tuần hoàn hóa học. Biết oxide của X khi tan trong nước tạo thành một dung dịch làm hồng quỳ tím. Y phản ứng với nước làm xanh giấy quỳ tím, còn Z phản ứng được với cả acid và kiềm. Nếu sắp xếp theo trật tự tăng dần số hiệu nguyên tử thì trật tự đúng sẽ là:
- X là phi kim vì oxide của X tan trong nước tạo acid.
- Y phản ứng với nước làm xanh quỳ nên Y là base.
- Z phản ứng với cả acid và kiềm nên Z là kim loại có oxide lưỡng tính. Ví dụ như Al, Zn,...
Vì theo chiều tăng số hiệu nguyên tử thì tính acid tăng dần nên sắp xếp trật tự là Y, Z, X.
Theo quy luật biến đổi tính chất các đơn chất trong bảng tuần hoàn thì
Phi kim mạnh nhất là fluorine vì theo chiều tăng dần của điện tích hạt nhân:
Trong một chu kì, tính phi kim tăng dần → phi kim mạnh nhất ở nhóm VIIA.
Trong một nhóm, tính phi kim giảm dần → phi kim mạnh nhất là fluorine.
Cấu hình electron của nguyên tử nguyên tố X có dạng 1s22s22p63s23p5. Phát biểu nào sau đây là sai?
Cấu hình electron của X: 1s22s22p63s23p5
X ở ô số 17 trong bảng tuần hoàn vì có 17 electron
Lớp ngoài cùng là lớp thứ 3 có tổng số electron là 2 + 5 = 7 (electron) nên nguyên tử X là phi kim
Nguyên tử của nguyên tố X có 11 electron p
Phát biểu "Nguyên tử của nguyên tố X có 3 phân lớp electron" sai vì X có 5 phân lớp: 1s; 2s; 2p; 3s; 3p.
Trong một nhóm A (trừ nhóm VIIIA), theo chiều tăng của điện tích hạt nhân nguyên tử,
Trong một nhóm A (trừ nhóm VIIIA), theo chiều tăng của điện tích hạt nhân nguyên tử:
Bán kính nguyên tử tăng dần, độ âm điện giảm dần.
Tính kim loại tăng dần và tính phi kim giảm dần.
Công thức oxide cao nhất của nguyên tố R là R2O7. hợp chất khí của nguyên tố này với H chứa 97,26% về khối lượng. Nguyên tố R là:
Công thức oxide cao nhất của nguyên tố R là R2O7 nên thuộc nhóm VIIA.
Công thức hợp chất khí với H là RH.
Hợp chất khí của nguyên tố này với H chứa 97,26% về khối lượng nên ta có:
R = 35,5 (Cl)
Vậy R là chlorine.
Cho cấu hình electron của nguyên tử hai nguyên tố sau:
X: 1s22s22p63s23p3
Y: 1s22s22p63s23p63d34s2
X, Y lần lượt thuộc nhóm nguyên tố nào sau đây?
X: 1s22s22p63s23p3
Y: 1s22s22p63s23p63d34s2
Nguyên tử X, Y đều có 5 electron hóa trị nên chúng ở cùng nhóm V.
Nguyên tử X có 5 electron lớp ngoài cùng, là nguyên tố p, thuộc nhóm VA.
Nguyên tử Y có 5 electron ở lớp ngoài cùng và sát lớp ngoài cùng, là nguyên tố d, thuộc nhóm VB.
Nguyên tố Phosphorus (P) ở ô 15, chu kì 3, nhóm VA. Phát biểu nào sau đây không đúng?
Nguyên tố chlorine (Cl) ở ô 17, chu kì 3, nhóm VIIA.
Suy ra:
Số hiệu nguyên tử Z = 15 = Số electron = Số proton.
Số lớp electron = Số thứ tự chu kì = 3.
Số electron lớp ngoài cùng = Số thứ tự nhóm A = 5.
⇒ Cấu hình electron của nguyên tử P: 1s22s22p63s23p3
P là nguyên tố phi kim.
Nhóm B bao gồm các nguyên tố:
Khối các nguyên tố d gồm các nguyên tố thuộc nhóm B, có cấu hình electron: [Khí hiếm](n-1)d110ns1
2.
Ô nguyên tố không cho biết thông tin nào sau đây?
Ô nguyên tố không cho biết số khối của hạt nhân.
Tùy theo từng loại bảng, ô nguyên tố cho ta biết một số thông tin như:
Số hiệu nguyên tử
Kí hiệu nguyên tố
Tên nguyên tố
Nguyên tử khối trung bình.
Ngoài ra: Số hiệu nguyên tử = Số đơn vị điện tích hạt nhân = số thứ tự ô nguyên tố = số proton = số electron.
Một số loại bảng tuần hoàn còn cho biết độ âm điện, năng lượng ion hóa, ....
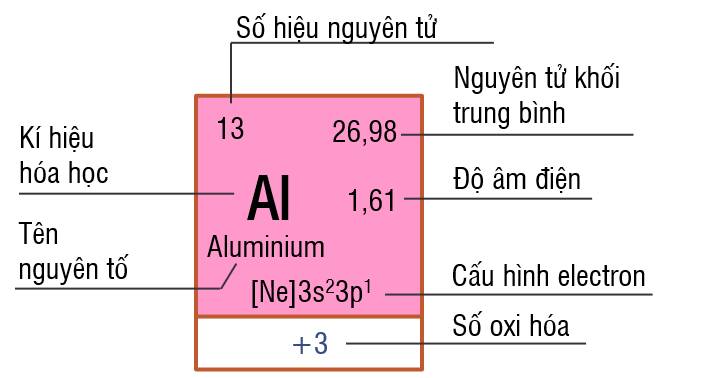
Đâu không phải thông tin về nguyên tố hóa học mà một ô nguyên tố biểu diễn?
Một ô nguyên tố biểu diễn số hiệu nguyên tử, cấu hình electron và kí hiệu nguyên tố.
Nguyên tố X ở chu kì 3, nhóm IIIA của bảng tuần hoàn. Cấu hình electron của nguyên tử nguyên tố X là
Nguyên tố X ở chu kì 3 ⇒ Có 3 lớp electron.
Nguyên tố X thuộc nhóm IIIA ⇒ Lớp ngoài cùng có 3 electron.
⇒ 1s22s22p63s23p1
Hydroxide nào có tính base mạnh nhất trong các hydroxide sau đây?
Strontium hydroxide: Sr(OH)2
Barium hydroxide: Ba(OH)2
Calcium hydroxide: Ca(OH)2
Magnesium hydroxide: Mg(OH)2
Ta có Sr, Ba, Ca, Mg ở cùng trong nhóm IIA, đi từ trên xuông dưới theo chiều điện tích hạt nhân tăng tính base của các hydroxide tăng dần.
⇒ Hydroxide nào có tính base mạnh nhất là Barium hydroxide
Cho các nguyên tố sau: F, Cl, Br, I. Nguyên tử của nguyên tố có bán kính bé nhất là
F (Z = 9), Cl (Z = 17), Br (Z = 35), I ( Z = 53) cùng thuộc nhóm VIIA
Trong 1 nhóm A, bán kính nguyên tử giảm dần theo chiều tăng dần của điện tích hạt nhân
⇒ Bán kính F < Cl < Br < I
Hydroxide của nguyên tố T có tính base mạnh và tác dụng được với dung dịch HCl theo tỉ lệ mol giữa hydroxide của T và HCl là 1 : 2. Nhóm của T trong bảng tuần hoàn là
Hydroxide của nguyên tố T có tính base mạnh ⇒ công thức có dạng: T(OH)x
T(OH)x + xHCl ⟶ TClx + xH2O
Mà tỉ lệ mol giữa hydroxide của T và HCl là 1 : 2 ⇒ x = 2
⇒ T có hóa trị II mà hydroxide của T có tính base mạnh ⇒ T thuộc nhóm IIA.
Cho 18,4 gam một kim loại kiềm tác dụng với nước dư thu được 9,916 lít khí hydrogen (ở đkc). Kim loại kiềm là
Gọi kim loại kiềm là R thì
Phương trình hóa học tổng quát:
R + H2O → ROH + H2
Ta có nH2 = 9,916 : 24,79 = 0,4 mol
⇒ nR = 0,8 mol
→ MA = 18,4 : 0,8 = 23 (gam/mol)
Vậy kim loại kiềm là Na
Cho 5,6 gam oxide của kim loại X (thuộc nhóm IIA) tác dụng vừa đủ với 200 ml dung dịch HCl 1M. Kim loại X là
X thuộc nhóm IIA ⇒ hóa trị II
⇒ Công thức oxide có dạng: XO
nHCl = 0,2.1 = 0,2 (mol)
Phương trình có dạng
XO + 2HCl ⟶ XCl2+ H2O
0,1 ← 0,2 (mol)
MXO= 5,6 : 0,1 = 56 (g/mol)
Mà MXO= MX + 16 ⇒ MX + 16 = 56 ⇒ MX= 40 (g/mol)
Vậy X là Ca
