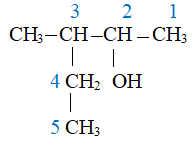Hydrate hóa 2 alkene được hỗn hợp Z gồm 2 alcohol liên tiếp trong dãy đồng đẳng. Đốt cháy hoàn toàn 0,53 gam Z rồi hấp thụ toàn bộ sản phẩm cháy vào 2 lít dung dịch NaOH 0,05M được dung dịch T trong đó nồng độ của NaOH là 0,025M (Giả sử thể tích dung dịch thay đổi không đáng kể). Công thức cấu tạo của 2 alkene là
Vì NaOH dư nên
CO2 + 2 NaOH → Na2CO3 + H2O
nNaOH p/ứng = 2.(0,05 – 0,025 ) = 0,05 mol
nCO2 = 0,025 mol
Gọi công thức chung của 2 alcohol là CnH2n+2O.
n = 2,5
Vậy alcohol là C2H5OH và C3H7OH
Alkene là: CH2=CH2, CH3CH=CH2.