mbình 1 tăng= mH2O = 1,8 gam
⇒ nH2O = 1,8 : 18 = 0,1 (mol)
⇒ nH = 2nH2O = 2.0,1 = 0,2 mol
Bảo toàn nguyên tố "C":
nCO2 = nCaCO3 = 15 : 100 = 0,15 (mol) ⇒ nC= nCO2 = 0,15 (mol)
Bảo toàn khối lượng ta có:
mO (Y) = mY - mC - mH = 5,2 - 0,15.12 - 0,2.1 = 3,2 gam
⇒ nO(Y) = 3,2 : 16 = 0,2 (mol)
Đặt công thức phân tử của X: CxHyOz (đk: x, y, z, nguyên dương)
Ta có: x: y : z = nC : nH : nO = 0,15 : 0,2 : 0,2 = 3: 4: 4
⇒ Công thức phân tử Y có dạng: (C3H4O4)n
Ta có X và O2 có cùng thể tích nên:
nX = nO2 = 0,025 mol
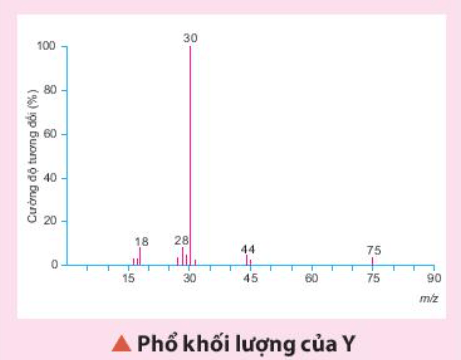
⇒ MX = 2,6 : 0,025 = 104
⇒ n = 1 thỏa mãn
⇒ Công thức phân tử Y: C3H4O4
Dãy gồm các dẫn xuất của hydrocarbon là: C2H6O, C3H7Cl, C2H5Br.