Cồn 70o là dung dịch ethyl alcohol, được dùng để sát trùng vết thương. Nội dung nào sau đây về cồn 70o là đúng?
Trong 100 mL dung dịch cồn 70o có 70 mL ethyl alcohol nguyên chất.
Cồn 70o là dung dịch ethyl alcohol, được dùng để sát trùng vết thương. Nội dung nào sau đây về cồn 70o là đúng?
Trong 100 mL dung dịch cồn 70o có 70 mL ethyl alcohol nguyên chất.
Hỗn hợp x mol phenol và y mol stiren. Để phản ứng hết với hỗn hợp trên cần dùng 250 gam dung dịch Br2 3,2%. Sau phản ứng thu được hỗn hợp các chất phản ứng vừa đủ với 25,23 cm3 dung dịch NaOH 10% (khối lượng riêng bằng 1,11 g/cm3). Cho biết dung dịch xút loãng không thủy phân được nhóm halogen gắn trực tiếp vào nhân thơm. Giá trị của x và y là:
mddNaOH = d.V = 1,11.25,23 = 28 gam
C6H5OH + 3Br2 → C6H2Br3OH + 3HBr
x 3x 3x
C6H5CH=CH2 + Br2 → C6H5CBr-CH2Br
y y
C6H5CBr-CH2Br + 2NaOH → C6H5COH-CH2OH + 2NaBr
y y
NaOH + HBr → NaBr + H2O
3x 3x
Ta có hệ phương trình:
Cho các alcohol sau: CH3OH, C2H5OH, HOCH2-CH2OH, HOCH2-CH2-CH2OH, CH3-CH(OH)-CH2OH.
Số alcohol trong các alcohol cho ở trên phản ứng được với Cu(OH)2 ở nhiệt độ thường là
Các alcohol phản ứng được với Cu(OH)2 ở nhiệt độ thường trong phân tử phải có từ 2 nhóm -OH liền kề nhau trở lên:
HOCH2-CH2OH; CH3-CH(OH)-CH2OH
Có bao nhiêu phản ứng xảy ra khi cho các chất C6H5OH; NaHCO3; NaOH; HCl tác dụng với nhau từng đôi một?
Các phản ứng xảy ra:
C6H5OH + NaOH → C6H5ONa + H2O
NaHCO3 + NaOH → Na2CO3 + H2O
NaHCO3 + HCl → NaCl + CO2 + H2O
NaOH + HCl → NaCl + H2O
Chất nào sau đây là dẫn xuất halogen của hydrocarbon?
Khi thay thế nguyên tử hydrogen trong phân tử hydrocarbon bằng nguyên tử halogen được dẫn xuất halogen của hydrocarbon
Vậy C6H5-CH2-Cl là dẫn xuất halogen của hydrocarbon.
Người ta có thể điều chế phenol từ canxicacbua theo sơ đồ sau:
CaC2 → X → Y → Z → T → C6H5OH
X, Y, Z, T lần lượt là:
X: C2H2; Y: C6H6; Z: C6H5Cl; T: C6H5ONa
Phương trình phản ứng minh họa
CaC2 + 2H2O → C2H2 + Ca(OH)2
CH≡CH C6H6
C6H6 + Cl2 C6H5Cl + HCl
C6H5Cl + 2NaOH ⟶ C6H5ONa + H2O + NaCl.
Một alcohol no Y có công thức đơn giản nhất là C2H5O. Y có công thức phân tử là
Ancol no Y có công thức đơn giản nhất là C2H5O
CTPT của Y có dạng (C2H5O)n
Độ bất bão hòa của Y:
n = 2
Vậy công thức phân tử của Y là C4H10O2
Đun nóng một alcohol đơn chức X với dung dịch H2SO4 đặc trong điều kiện nhiệt độ thích hợp sinh ra chất hữu cơ Y, tỉ khối hơi của X so với Y là 0,6956. Công thức phân tử của Y là
X nhẹ hơn Y Y là ether, Y = 2X - 18
Mà X/Y = 0,6956
X = 32 (CH4O)
Tên thay thế của alcohol có công thức cấu tạo thu gọn CH3CH2CH2OH là
Tên thay thế của alcohol có công thức cấu tạo thu gọn CH3CH2CH2OH là propan-1-ol.
Cho phản ứng hóa học sau:
C2H5-Cl + NaOH ![]() C2H5-OH + NaCl.
C2H5-OH + NaCl.
Phản ứng trên thuộc loại phản ứng nào sau đây?
Phản ứng thuộc loại phản ứng tách.
C2H5-Cl + NaOH C2H5-OH + NaCl.
Alcohol nào sau đây có số nguyên tử carbon nhiều hơn số nhóm -OH?
Ethyl alcohol: C2H5OH
Methyl alcohol: CH3OH
Ethylene glycol: HO-CH2-CH2OH
Glycerol: C3H5(OH)3.
Trong các chất sau, chất nào thuộc loại phenol?
Phenol là những hợp chất hữu cơ trong phân tử có một hay nhiều nhóm hydroxy liên kết trực tiếp với nguyên tử carbon của vòng benzene.
Vậy hợp chất thuộc loại phenol là:
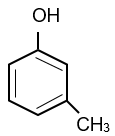
Dẫn xuất halogen nào sau đây có đồng phân hình học?
Dẫn xuất halogen có đồng phân hình học là C6H5CH=CFCH3 do 2 nguyên tử carbon mang nối đôi đính với 2 nguyên tử/ nhóm nguyên tử khác nhau.
Tên theo danh pháp thay thế của dẫn xuất halogen có công thức cấu tạo: ClCH2CH(CH3)CHClCH3 là
Picric acid (2,4,6-trinitrophenol) trước đây được sử dụng làm thuốc nổ. Để tổng hợp picric acid, người ta cho 37,6 g phenol phản ứng với hỗn hợp HNO3 đặc/ H2SO4 đặc, dư. Tính khối lượng picric acid thu được, biết hiệu suất phản ứng là 65%.
Phương trình phản ứng
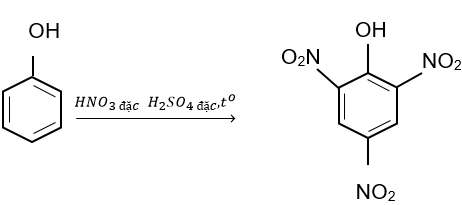
Số mol phenol: nphenol = 37,6 : 94 = 0,4 (mol)
Số mol picric acid tạo thành:
Khối lượng picric acid thu được:
mpicricacid = 0,26.229 = 59,54 (g).
Dẫn xuất halogen nào sau đây khi tác dụng với NaOH không tạo thành alcohol?
Các dẫn xuất halogen tác dụng với NaOH tạo thành alcohol: C2H5Cl, C6H5CH2Br, CH3CH(Br)CH3.
C6H5Cl khi tác dụng với NaOH thu được muối sodium phenolate:

Hydrate hóa 2 alkene chỉ tạo thành 2 alcohol. Hai alkene đó là
2 alkene + H2O → 2 sản phẩm mỗi alkene tạo 1 sản phẩm.
Vì H2O là tác nhân bất đối xứng cả 2 anken đều đối xứng
Vậy ethene và but-2-en thõa mãn vì CH2=CH2 và CH3-CH=CH-CH3 đều đối xứng
- But-1-en: CH2=CH-CH2-CH3 bất đối xứng.
- Propene: CH2=CH-CH3 bất đối xứng.
- 2-methylpropene: (CH3)2CHCH2OH đều bất đối xứng.
Phương pháp nào sau đây dùng để sản xuất ethanol sinh học.
Lên men tinh bột là phương pháp dùng để sản xuất ethanol sinh học.
Trong số các chất sau, chất tan trong nước ở điều kiện thường là
C2H5OH là chất lỏng, không màu, tan vô hạn trong nước.
Oxi hóa 1 mol alcohol no, mạch hở X bằng CuO, đun nóng được Y. Cho toàn bộ Y phản ứng với dung dịch AgNO3/NH3 được 4 mol Ag. Cho 1 mol X tác dụng hết với Na được một mol H2. đốt cháy một mol X cho lượng CO2 nhỏ hơn 90 gam. Tìm công thức phân tử của X.
- 1 mol Y tráng bạc đc 4 mol Ag loại C2H5OH và C3H6(OH)3
- 1 mol X tác dụng vs Na đc 1 mol H2 C2H4(OH)2 thỏa mãn
Số đồng phân cấu tạo anken ở thể khí (đktc) mà khi cho mỗi anken đó tác dụng với dung dịch HCl chỉ cho một sản phẩm hữu cơ duy nhất là
Có 2 công thức thỏa mãn là:
CH2=CH2
CH3-CH=CH-CH3
Cho m gam một alcohol no, đơn chức qua bình đựng CuO dư, nung nóng. Sau khi phản ứng xảy ra hoàn toàn, khối lượng chất rắn trong bình giảm 0,32 gam. Hỗn hợp thu được có tỉ khối đối với hydrogen là 15,5. Giá trị của m là:
Phương trình phản ứng:
CnH2n+1CH2OH + CuO → CnH2n+1CHO + Cu + H2O
0,02 0,02 0,02
Khối lượng chất rắn giảm = mO phản ứng
nO = nCuO = 0,32 : 16 = 0,02 mol
Do phản ứng xảy ra hoàn toàn nên alcohol hết, sản phẩm chỉ có aldehyde và hơi nước.
Ta có:
m = 0,02.46 = 0,92 gam.
Phân tử chất A có một nguyên tử oxygen và một vòng benzene. Trong A, phần trăm khối lượng các nguyên tố C, H và O lần lượt là: 77,78%; 7,41% và 14,81%. Xác định công thức phân tử A.
Đặt công thức của A là CxHyO.
Phân tử chất A có một nguyên tử oxygen
⇒ Khối lương mol của A là
Vậy công thức phân tử của A là C7H8O
Hai alcohol nào sau đây cùng bậc?
Propan-2-ol và 1-phenyletan-1-ol là hai alcohol bậc 2.
Cho các alcohol gồm: methanol, propan-1-ol, butan-2-ol, 3-methylbutan-2-ol và 2-methylpropan-2-ol. Số alcohol khi tác dụng với CuO/to tạo ra ketone là
Các alcohol khi tác dụng với CuO/to tạo ra ketone là các alcohol bậc hai gồm: butan-2-ol, 3-methylbutan-2-ol.
Đun nóng 1,91 gam hỗn hợp X gồm C3H7Cl và C6H5Cl với dung dịch NaOH loãng vừa đủ, sau đó thêm tiếp dung dịch AgNO3 đến dư vào hỗn hợp sau phản ứng, thu được 1,435 gam kết tủa. Phần trăm khối lượng C6H5Cl trong hỗn hợp đầu là
Chỉ có C3H7Cl phản ứng với dung dịch NaOH loãng, đun nóng.
Gọi số mol của C3H7Cl là x.
C3H7Cl + NaOH → C3H7OH + NaCl
x → x
NaCl + AgNO3 → AgCl↓ + NaNO3
x → x
x = nAgCl = 1,435/143,5 = 0,01 mol
→ mC3H7Cl = 0,01.78,5 = 0,785 gam
→ %mC3H7Cl = (0,785/1,91).100% = 41,1%
→ %mC6H5Cl = 100% – 41,1% = 58,9%
Ancol etylic và phenol cùng tác dụng với
Ancol etylic và phenol cùng tác dụng với Na
Phương trình phản ứng minh họa
C2H5OH + Na → C2H5ONa + 1/2H2.
C6H5OH + Na → C6H5ONa + 1/2H2.
Cồn công nghiệp chứa nhiều tạp chất nên rất nguy hiểm cho con người nếu sử dụng để uống. Do có chứa chất nào dưới đây mà cồn công nghiệp vô cùng có hại cho sức khỏe con người?
Methanol gây độc do uống, hít, thấm qua da. Ngộ độc cấp thường có biểu hiện: đau đầu, mệt, buồn nôn, giảm thị lực, nặng hơn sẽ bị mù, co giật, giãn đồng tử, suy sụp tuần hoàn, suy hô hấp, rồi tử vong. Methanol còn gây ngộ độc mạnh như giảm thị lực.
Công thức của glycerol là
Công thức của glycerol là C3H5(OH)3.
Phân ứng thế bromine vào vòng thơm của phenol xảy ra dễ dàng hơn so với benzene là do:
Do ảnh hưởng của nhóm -OH, phản ứng thế nguyên tử hydrogen ở vòng benzene phenol xảy ra dễ dàng hơn so với benzene
Người ta có thể điều chế phenol từ Calci carbide theo sơ đồ sau:
CaC2 → X → Y → Z → T → C6H5OH
Hãy chọn X, Y, Z, T phù hợp
Sơ đồ hoàn chỉnh
CaC2 → C2H2 → C6H6 → C6H5Cl→ C6H5ONa→ C6H5OH
Phương trình phản ứng minh họa
CaC2 + 2H2O → C2H2 + Ca(OH)2
CH≡CH C6H6
C6H6 + Cl2 C6H5Cl + HCl
C6H5Cl + 2NaOH ⟶ C6H5ONa + H2O + NaCl
Khi đốt cháy hoàn toàn m gam hỗn hợp hai alcohol no đơn chức, mạch hở thu được V lít khí CO2 (đktc) và a gam H2O. Biểu thức liên hệ giữa m, a vầ V là
Vì các alcohol là no đơn chức nên:
nO (alcohol) = nalcohol = nH2O - nCO2
Áp dụng định luật bảo toàn khối lượng ta có:
m = malcohol = mC + mH + mO (alcohol)
Dãy đồng đẳng của Alcohol ethylic có công thức tổng quát là:
Dãy đồng đẳng của Alcohol ethylic (C2H5OH) có công thức tổng quát là: CnH2n+1OH (n≥1)
Phản ứng chứng minh nguyên tử H trong nhóm -OH của phenol (C6H5OH) linh động hơn alcohol là
Phương trình phản ứng:
C6H5OH + NaOH → C6H5ONa + H2O
Để điều chế picric acid, người ta cho 23,5 gam phenol tác dụng với HNO3 đặc, H2SO4 đặc. Biết lượng acid HNO3 đã lấy dư 25% so với lượng cần thiết. Số mol HNO3 cần dùng và khối lượng picric acid tạo thành là:
nC6H5OH = 0,25 mol
C6H5OH + 3HNO3 C6H2(NO2)3OH + 3H2O
0,25 → 0,75 → 0,25
Ta có: lượng HNO3 đã lấy dư 25% so với lượng cần thiết nên
⇒ nHNO3 dùng = 0,75 + 25%.0,75 = 0,9375 mol
mpicric acid = 0,25.229 = 57,25 gam
Cho các chất: C2H5OH, C2H5Br, C6H5OH, C6H5CH2OH, CH3COOH. Số chất tác dụng được với dung dịch NaOH, đun nóng là
Chất tác dụng được với dung dịch NaOH:
CH3COOH + NaOH → CH3COONa + H2O
C6H5OH + NaOH → C6H5ONa + H2O
C2H5Br + NaOH C2H5OH + NaBr
Công thức cấu tạo đúng của 2,2- dimethylbutan-1-ol là:
Công thức cấu tạo đúng của 2,2- dimethylbutan-1-ol là CH3-CH(CH3)-CH(CH3)-CH2-O.
Khi đun sôi hỗn hợp gồm C2H5Br và KOH trong C2H5OH thấy thoát ra một chất khí không màu. Dẫn khí này đi qua ống nghiệm đựng nước bromine thấy hiện tượng
Phương trình phản ứng xảy ra
CH3-CH2-Br + KOH CH2=CH2 + KBr + H2O
CH2=CH2 + Br2 → CH2Br-CH2Br.
Đốt cháy hoàn toàn x gam alcohol X rồi cho các sản phầm cháy vào bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng y gam và tạo z gam kết tủa. Biết 100y = 71z; 102z = 100(x + y). Có các nhận xét sau:
a. X có nhiệt độ sôi cao hơn ethyl alcohol
b. Từ ethylene phải ít nhất qua 2 phản ứng mới tạo được X
c. X tham gia được phản ứng trùng hợp
d. Ta không thể phân biệt được X với C3H5(OH)3 chỉ bằng thuốc thử Cu(OH)2
e. Đốt cháy hoàn toàn X thu được số mol nước lớn hơn số mol CO2
Số phát biểu đúng là
Theo bài ra ta có:
Ta có:
a g X + O2 → CO2 + H2O
CO2 + Ca(OH)2 → CaCO3 + H2O
nCaCO3 = z : 100 = 0,01z mol nCO2 = nCaCO3 = 0,01z (mol)
mbình tăng = mCO2 + mH2O = 44.0,01z + 18nH2O = y nH2O =
mol
Bảo toàn C có nC(X) =nCO2 = 0,01z mol
Bảo toàn H có nH(X) = 2nH2O = =
= 0,03z mol
Lại có:
mX = mC + mH + mO = x 0,31z = 12.0,01z + 0,03z.1 + mO
mO = 0,16z
nO = 0,01z
Suy ra X có C : H : O = nC : nH : nO = 0,01z : 0,03z : 0,01z = 1 : 3 : 1
CTĐGN là CH3O
CTPT là (CH3O)n thì 3n ≤ 2n+ 2
n ≤ 2
n = 2
X là C2H6O2 (C2H4(OH)2)
a. Đúng
b. Sai vì chỉ cần cho C2H4 + KMnO4 → C2H4(OH)2
c. Sai vì X không có liên kết đôi
d. Đúng vì cả hai đều tạo phức màu xanh lam
e. Đúng
Vậy có 3 phát biểu đúng
Cho biết có bao nhiêu đồng phân của alcohol no, đơn chức, mạch hở từ C3 đến C5 khi tách nước chỉ tạo thành 1 alkene?
Các đồng phân alcohol thõa mãn là:
- C3H7OH: CH3CH2CH2OH và CH3CH(OH)CH3
- C4H9OH: CH3CH2CH2CH2OH; CH3C(OH)(CH3)CH3 và CH3CH(CH3)CH2OH.
- C5H11OH: CH3[CH2]3CH2OH; (CH3)2CHCH2CH2OH; CH2OHCH(CH3)CH2CH3.
