Hydrogen halide nào sau đây được sử dụng trong quá trình sản xuất teflon (dùng làm chất chống dính ở nồi, chảo)?
Hydrogen fluoride được sử dụng trong quá trình sản xuất teflon (dùng làm chất chống dính ở nồi, chảo) theo sơ đồ:
Hydrogen halide nào sau đây được sử dụng trong quá trình sản xuất teflon (dùng làm chất chống dính ở nồi, chảo)?
Hydrogen fluoride được sử dụng trong quá trình sản xuất teflon (dùng làm chất chống dính ở nồi, chảo) theo sơ đồ:
Ở điều kiện chuẩn, 1 mol nhôm tác dụng vừa đủ với khí chlorine tạo ra muối aluminium chloride và giải phóng một lượng nhiệt 695,405 kJ. Biến thiên enthalpy chuẩn của phản ứng bằng bao nhiêu? Phản ứng trên thu nhiệt hay tỏa nhiệt?
1 mol nhôm tác dụng vừa đủ với khí chlorine tạo ra muối aluminium chloride và giải phóng một lượng nhiệt 695,405 kJ.
Biến thiên enthalpy chuẩn của phản ứng = 695,405 kJ, phản ứng tỏa nhiệt.
Cho 100 gam CaCO3 tác dụng với dung dịch HCl 2M ở nhiệt độ, áp suất không đổi. Tốc độ phản ứng tăng khi:
Tốc độ phản ứng tăng khi tăng nồng độ chất phản ứng.
⇒ Tốc độ phản ứng trên tăng khi dùng dung dịch HCl 4 M thay cho dung dịch HCl 2 M.
Biến thiên enthalpy của một phản ứng được ghi ở sơ đồ dưới đây. Kết luận nào sau đây là đúng?
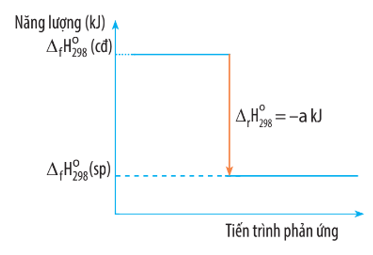
Từ sơ đồ ta thấy: (sp) <
(cđ) nên
< 0 và
= -a kJ
Do đó đây là phản ứng tỏa nhiệt.
Cho phản ứng sau đây là phản ứng thu nhiệt:
CH4 (g) + H2O (l) → CO (g) + 3H2 (g)
Giá trị ![]() nào sau đây là đúng?
nào sau đây là đúng?
Vì phản ứng thu nhiệt nên > 0 ⇒
= 250 kJ.
Dẫn khí chlorine vào dung dịch KBr xảy ra phản ứng hóa học:
Cl2 + 2KBr ![]() 2KCl + Br2
2KCl + Br2
Trong phản ứng hóa học trên, xảy ra quá trình oxi hóa chất nào?
Sự thay đổi số oxi hóa của các nguyên tố:
Ta thấy nguyên tử Br nhường electron KBr là chất khử hay là chất bị oxi hóa.
Vậy trong phản ứng xảy ra quá trình oxi hóa KBr.
Cho phản ứng: 3O2(g) → 2O3(g)
Ban đầu nồng độ oxygen là 0,024M. Sau 5s thì nồng độ của oxygen là 0,02M. Tốc độ trung bình của phản ứng trên trong 5s đầu tiên là
Tốc độ trung bình của phản ứng tính theo oxygen trong 5s đầu tiên là:
Có một dung dịch hỗn hợp KF, KBr, KI. Thổi một luồng khí Cl2 vào dung dịch cho đến dư. Sản phẩm nào sau đây được tạo thành?
2KBr + Cl2 → 2KCl + Br2
2KI + Cl2 → 2KCl + I2
Hydrogen halide nào sau đây có nhiệt độ sôi cao bất thường so với các hydrogen halide còn lại?
HF lỏng có nhiệt độ sôi cao bất thường là do phân tử HF phân cực mạnh, có khả năng tạo liên hết hydrogen.
H-F…H-F…H-F
Hoà tan khí Cl2 vào dung dịch KOH loãng, nguội, dư, thu được có các chất thuộc dãy nào dưới đây?
Ở nhiệt độ thường:
Cl2 + KOH KCl + KClO + H2O
Sản phẩm sau phản ứng có cả KOH dư.
Cho sơ đồ phương trình: KMnO4 + FeSO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 + H2O. Tổng hệ số của chất oxi hóa và chất khử trong phản ứng trên là
Fe+2SO4 + KMn+7O4 + H2SO4 → Fe+32(SO4)3 + Mn+2SO4 + K2SO4 + H2O
FeSO4 đóng vai trò là chất khử
KMnO4 là chất oxi hóa
Quá trình oxi hóa: 5x Quá trình khử: 2x | 2Fe+2 → 2Fe+3 + 2e Mn+7 + 5e → Mn+2 |
Đặt các hệ số tìm được vào phản ứng và tính các hệ số còn lại:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Chất oxi hóa là KMnO4 có hệ số là 2
Chất khử là FeSO4 có hệ số là 10
Tổng hệ số của chất oxi hóa và chất khử trong phản ứng trên là 10 + 2 = 12
Khi cho cùng một lượng aluminium vào cốc đựng dung dịch HCl 0,1M, tốc độ phản ứng sẽ lớn nhất khi dùng aluminium ở dạng nào sau đây?
Aluminium dạng bột mịn có diện tích bề mặt tiếp xúc lớn nhất tốc độ phản ứng lớn nhất.
Mệnh đề nào sau đây không đúng?
Mệnh đề không đúng: Tất các các muối AgX (X là halogen) đều không tan.
Vì AgF là muối tan.
Đơn chất halogen ở trạng thái khí trong điều kiện thường, màu vàng lục là
Đơn chất halogen ở trạng thái khí trong điều kiện thường, màu vàng lục là Cl2.
Chất nào sau đây tác dụng với dung dịch HF nhưng không tác dụng với dung dịch HCl?
SiO2 tác dụng với dung dịch HF nhưng không tác dụng với dung dịch HCl
Cho 1,49 gam muối potassium halide (KX) tác dụng với dung dịch AgNO3 dư thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 2,16 gam Ag. Xác định halogen X.
Cho 1,49 gam muối potassium halide (KX) tác dụng với dung dịch AgNO3 dư thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 2,16 gam Ag. Xác định halogen X.
Phương trình hóa học:
KX + AgNO3 → AgX↓ + KNO3
2AgX → 2Ag + X2
Theo PTHH: nKX = nAgX = nAg = 0,02 (mol)
⇒ X = 74,5 − 39 = 35,5 (Cl)
Hằng số tốc độ phản ứng k bằng vận tốc tức thời ![]() khi nào?
khi nào?
Hằng số tốc độ phản ứng k bằng vận tốc tức thời khi nồng độ chất phản ứng bằng đơn vị (1M), khi đó k là tốc độ phản ứng và được gọi là tốc độ riêng.
Tìm phát biểu sai.
Đặc điểm nào dưới đây không phải là đặc điểm chung của các nguyên tố halogen?
Đặc điểm không phải là đặc điểm chung cho các nguyên tố halogen (F, Cl, Br, I) là: Chỉ có số oxi hóa -1 trong các hợp chất.
Cho sơ đồ phản ứng sau: Al + HNO3 → Al(NO3)3 + N2 + H2O. Hệ số cân bằng của phản ứng lần lượt là:
Xác định vai trò của từng chất tham gia phản ứng và nêu sự oxi hóa, sự khử:
Al0 + H+5NO3loãng → Al+3(NO3)3+ N02+ H2O
Số oxi hóa của Al tăng từ 0 lên +3 ⇒ Al là chất khử
Số oxi hóa của N giảm từ +5 xuống 0 ⇒ HNO3 là chất oxi hóa
Sự oxi hóa: Al → Al+3 + 3e
Sự khử: 2N+5 + 10e → N2
b) Cân bằng phản ứng trên theo phương pháp thăng bằng electron.
0Al + H+5NO3 loãng → Al+3(NO3)3+ 0N2 + H2O
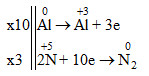
Phương trình phản ứng
10Al + 36HNO3 loãng → 10Al(NO3)3 + 3N2 + 18H2O
Cho 34,8 gam MnO2 tác dụng với axit HCl đặc, dư, thu được V lít khí Cl2 (đktc). Giá trị của V là bao nhiêu?
nMnO2 = 34,8 : 87 = 0,4 mol
Phương trình phản ứng hóa học
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
Theo phương trình phản ứng
nMnO2 = nCl2 = 0,4 mol
VCl2 = 0,4.22,4 = 8,96 lít
Hỗn hợp khí X gồm chlorine và oxygen. X phản ứng vừa hết với một hỗn hợp gồm 4,8 gam magnesium và 8,1 gam nhôm tạo ra 37,05 gam hỗn hợp các muối halide và oxide của hai kim loại. Thành phần phần trăm theo khối lượng của chlorine và oxygen trong hỗn hợp X lần lượt là
Các phương trình hóa học:
Mg + Cl2 → MgCl2 (1)
2Al + 3Cl2 → AlCl3 (2)
3Mg + O2 → 2MgO (3)
4Al + 3O2 → 2AlO3 (4)
mmuối + moxide = mKL + mCl- + mO- = 37, 05
⇒ mCl- + mO- = 37,05 – (4,80 + 8,10) = 24, 15 (gam)
nMg = 4,8/24 = 0,2 (mol); nAl = 8,1/27 = 0,3 (mol)
Gọi số mol O2 và Cl2 trong hỗn hợp lần lượt là x, y (mol):
Phương trình nhường e:
Al → Al3+ + 3e
Mg → Mg2+ + 2e
ne nhường = 0,2.2 + 0,3.3 = 1,3 (mol)
Phương trình nhận e:
O2 + 4e → 2O-
x → 4x → 2x
Cl2 + 2e → 2Cl-
y → 2y → 2y
ne nhận = 4x + 2y ⇒ 4x + 2y = 1,3 (1)
mO- + mCl- = 16.2x + 35,5.2y = 24,15 (2)
Từ (1) và (2) ta có x = 0,2; y = 0,25
%mCl2 = 100% – 26,5% = 73,5%
Biết phản ứng đốt cháy khí carbon monoxide (CO) như sau:
CO(g) + ![]() O2(g) → CO2(g)
O2(g) → CO2(g) ![]() = −851,5 kJ
= −851,5 kJ
Ở điều kiện chuẩn, nếu đốt cháy 2,479 L khí CO thì nhiệt lượng toả ra là
Số mol CO cần đốt cháy là 0,1 mol.
Ta có:
Khi đốt cháy 1 mol CO tỏa ra 851,5 kJ nhiệt.
⇒ Khi đốt cháy 0,1 mol CO tỏa ra 851,5.0,1 = 85,25 kJ nhiệt.
Phát biểu nào sau đây là đúng?
- Sản phẩm cuối cùng của phản ứng giữa Fe3O4(s) và HI(aq) vừa đủ là FeI2, I2 và H2O.
- Ở trạng thái lỏng, giữa các phân tử HF tạo được liên kết hydrogen mạnh.
- Không thể làm khô khí hydrogen chlorine bằng NaOH(s), do xảy ra phản ứng:
NaOH + HCl → NaCl + H2O
- Dung dịch hydrohalic acid có khả năng ăn mòn thủy tinh là HF.
Cho 24,6 gam hỗn hợp X gồm Cu và Al tác dụng vừa đủ với hỗn hợp Y gồm O2 và Cl2 (có số mol bằng nhau) được 45,2 gam hỗn hợp Z gồm oxide và muối. Mặt khác, cho 12,3 gam X tác dụng với dung dịch HCl dư, thu được V lít khí H2. Giá trị của V là
Gọi số mol nO2 = nCl2 = a (mol)
Áp dụng bảo toàn khối lượng
24,6 + 32a + 71a= 45,2
⇒ a = 0,2
Gọi x, y lần lượt là số mol Cu, Al trong hỗn hợp.
⇒ 64x + 27y = 24,6 (1)
Bảo toàn electron:
2nCu + 3nAl = 4nO2 + 2nCl2
⇒ 2x + 3y= 0,2.4 + 0,2 . 2 = 1,2 (2)
Từ (1) và (2) giải hệ phương trình ta được:
x = 0,3 (mol)
y = 0,2 (mol)
Trong 12,3 gam X số mol Al là:
0,2 : 2 = 0,1 mol
Áp dụng bảo toàn electron: 3nAl = 2nH2
⇒ nH2 = 0,15 mol
⇒ VH2 = 0,15.24,79 = 3,7185 lít.
Loại phản ứng nào sau đây luôn luôn không phải là phản ứng oxi hóa - khử:
Phản ứng trao đổi (vôi cơ) luôn luôn không phải là phản ứng oxi hóa - khử:
Cho phản ứng:
3CO + Fe2O3 ![]() 2Fe + 3CO2
2Fe + 3CO2
Trong phản ứng trên, CO đóng vai trò là
Ta có:
Nguyên tử C trong CO nhường electron CO là chất khử.
Đối với phản ứng có chất khí tham gia thì
Đối với phản ứng có chất khí tham gia, khi áp suất tăng, tốc độ phản ứng tăng.
Thêm 78 ml dung dịch AgNO3 10% (D = 1,09 g/ml) vào dung dịch có chứa 3,88 g hỗn hợp KBr và NaI. Lọc bỏ kết tủa. Nước lọc phản ứng vừa đủ với 13,3 ml dung dịch HCl 1,5 M. Phần trăm khối lượng KBr trong hỗn hợp muối ban đầu là
mdd AgNO3 = D.V = 1,09.78 = 85,02 g
⇔ mAgNO3 = 8,502g ⇔ nAgNO3 = 0,05 mol
KBr + AgNO3 → KNO3 + AgBr
x x
NaI + AgNO3 → AgI + NaNO3
y y
Phần nước lọc phản ứng tác dụng với dung dịch HCl ⇒ AgNO3 còn dư
nHCl = 0,02 mol
AgNO3 + HCl → AgCl + HNO3
0,02 0,02
Ta có hệ phương trình:
Phần trăm khối lượng của KBr:
Ở mỗi phát biểu a), b), c), d), hãy chọn đúng hoặc sai.
Cho phản ứng: N2(g) + 3H2(g) → 2NH3(g). Ở điều kiện chuẩn, cứ 1 mol N2 phản ứng hết sẽ giải phóng 92,22 kJ.
(a) Nhiệt tạo thành của NH3 là –92,22 kJ/mol. Sai || Đúng
(b) Biến thiên enthalpy phản ứng trên là –46,11 kJ. Sai || Đúng
(c) Phản ứng trên là phản ứng tỏa nhiệt. Đúng || Sai
(d) Enthalpy tạo thành chuẩn của H2 bằng 0. Đúng || Sai
Ở mỗi phát biểu a), b), c), d), hãy chọn đúng hoặc sai.
Cho phản ứng: N2(g) + 3H2(g) → 2NH3(g). Ở điều kiện chuẩn, cứ 1 mol N2 phản ứng hết sẽ giải phóng 92,22 kJ.
(a) Nhiệt tạo thành của NH3 là –92,22 kJ/mol. Sai || Đúng
(b) Biến thiên enthalpy phản ứng trên là –46,11 kJ. Sai || Đúng
(c) Phản ứng trên là phản ứng tỏa nhiệt. Đúng || Sai
(d) Enthalpy tạo thành chuẩn của H2 bằng 0. Đúng || Sai
(a) sai. Ta có, cứ 1 mol N2 phản ứng hết sẽ tỏa ra 91,8 kJ và tạo thành 2 mol NH3
⇒ cứ 0,5 mol N2 phản ứng hết sẽ tỏa ra 91,8.0,5 = 45,9 (kJ) và tạo thành 1 mol NH3
Mà đây là phản ứng tỏa nhiệt nên < 0.
Vậy enthalpy tạo thành chuẩn của NH3 là = −45,9 kJ/mol.
(b) sai. Biến thiên enthalpy phản ứng trên là –92,22.
(c) đúng.
(d) đúng.
