Khớp khuỷu tay, khớp đầu gối thuộc:
Khớp khuỷu tay, khớp đầu gối thuộc khớp động do có thể cử động dễ dàng.
Khớp khuỷu tay, khớp đầu gối thuộc:
Khớp khuỷu tay, khớp đầu gối thuộc khớp động do có thể cử động dễ dàng.
Biện pháp nào dưới đây giúp cải thiện tình trạng táo bón?
1. Ăn nhiều rau xanh.
2. Hạn chế thức ăn chứa nhiều tinh bột và protein.
3. Uống nhiều nước.
4. Uống chè đặc.
Để cải thiện tình trạng táo bón, chúng ta cần ăn nhiều rau xanh, hạn chế thức ăn chứa nhiều tinh bột và protein, uống nhiều nước.
Việc nào sau đây không được làm khi sử dụng hóa chất?
Việc không được làm khi sử dụng hóa chất là dùng tay tiếp xúc trực tiếp với hóa chất.
Sản phẩm của phản ứng: Sắt (iron) + hydrochloric acid → iron (II) chloride + hydrogen là
Trong phản ứng hóa học, chất tham gia phản ứng gọi là chất đầu, chất mới tạo thành gọi là sản phẩm.
⇒ Sản phẩm của phản ứng trên là iron(II) chloride và hydrogen.
Cho 12,8 gam một kim loại R hóa trị II tác dụng với khí chlorine vừa đủ, thu được 27 gam muối chloride (RCl2). R là kim loại
Số mol của kim loại R ban đầu là:
Phương trình hóa học:
R + Cl2 → RCl2
mol: →
⇒ MR = 64
Vậy kim loại R là Cu (copper).
Khí X có tỉ khối đối với khí oxygen là 1,375. Tính số mol có trong 6,6 gam khí X.
Khí X có tỉ khối đối với khí oxygen là 1,375 ⇒ Khối lượng mol của khí X là:
⇒ Số mol có trong 6,6 gam khí X là:
Dầu chứa trong một bình có thể tích 0,330 lít. Biết khối lượng riêng của dầu là D = 0,920 kg/l. Xác định khối lượng của dầu chứa trong bình theo đơn vị gam.
Khối lượng của dầu chứa trong bình:
m = D.V = 0,920.0,330 ≈ 0,304 (kg) = 304 (g).
Các bệnh về tim mạch là bệnh lí xảy ra do
Các bệnh về tim mạch là bệnh lí xảy ra do sự bất thường trong cấu tạo, hoạt động của tim và mạch máu.
Thành phần nào sau đây của máu đóng vai trò chủ chốt trong quá trình đông máu?
Vai trò của tiểu cầu: Tham gia vào quá trình đông máu, bảo vệ cơ thể, tránh mất máu khi bị thương.
Hệ cơ quan nào dưới đây có vai trò điều khiển, điều hòa và phối hợp thực hiện hoạt động của các hệ cơ quan khác trong cơ thể?
Hệ thần kinh và hệ nội tiết có chức năng điều khiển, điều hòa và phối hợp thực hiện hoạt động của các cơ quan trong cơ thể.
Để đốt cháy m gam kim loại magnesium cần vừa đủ 1 gam oxygen, thu được 2,5 g hợp chất magnesium oxide (MgO). Tính giá trị của m.
Phương trình phản ứng:
2Mg + O2 2MgO
Áp dụng định luật bảo toàn khối lượng ta có:
mMg + mO2 = mMgO
⇒ mMg = mMgO – mO2 = 2,5 – 1 = 1,5 (g)
Xương có tính cứng chắc nhờ thành phần nào?
Chất vô cơ làm cho xương cứng chắc, chất hữu cơ giúp xương mềm dẻo.
Vai trò của dạ dày là gì?
Vai trò của dạ dày là co bóp giúp nghiền nát và trộn lẫn thức ăn với dịch vị.
Hiện tượng biến đổi nào sau đây không có sự biến đổi hóa học?
Hiện tượng không có sự biến đổi hóa học là sắt hút nam châm. Do không có sự tạo thành chất mới.
Hòa tan hết 20 gam sodium chloride vào 380 gam nước thì thu được dung dịch có nồng độ là
Nồng độ dung dịch thu được là:
Khi cắm ống hút vào cốc sữa và hút sữa vào miệng thì không khí bên ngoài tác dụng lên vỏ hộp sữa làm hộp sữa bị ép lại. Đây là do áp suất khi quyển gây nên.
Để tác dụng vừa đủ với 0,5 gam khí hydrogen thì cần dùng thể tích O2 (đkc) là
Số mol khí hydrogen là:
Phương trình phản ứng:
2H2 + O2 → 2H2O
mol: 0,25 → 0,125
Thể tích khí oxygen cần dùng là:
V = 0,125.24,79 ≈ 3,099 (lít)
Một người thợ lặn, lặn xuống độ sâu 36 m so với mặt nước biển. Cho biết trọng lượng riêng của nước biển là 10300 N/m3. Cửa chiếu sáng của áo lặn có diện tích 160 cm2. Tính áp lực của nước biển tác dụng lên cửa chiếu sáng của áo lặn?
Đổi 160 cm2 = 0,016 m2
Áp suất ở độ sâu 36 m là:
p = d.h = 36.10300 = 370800 Pa
Áp lực của nước tác dụng lên phần diện tích 160 cm2 là:
F = p.S = 370800.0,016 = 5932,8 (N)
Nhỏ một lượng nhỏ dung dịch (khoảng 1 ml) thường dùng dụng cụ nào sau đây?
Khi nhỏ một lượng nhỏ dung dịch (khoảng 1 ml) thường dùng ống hút nhỏ giọt.
Một sà lan có dạng hình hộp chữ nhật có kích thước là 10m × 4m × 2m. Khối lượng của sà lan và các thiết bị đặt trên xà lan bằng 50 tấn. Hỏi có thể đặt vào sà lan kiện hàng nặng bao nhiêu? Biết trọng lượng riêng của nước là 10000 N/m3.
Lực đẩy Archimedes lớn nhất tác dụng lên sà lan là:
FA = V.dn = 10.4.2.10000 = 800000 (N)
Để sà lan không bị chìm, trọng lượng của sà lan là:
P < FA ⇒ 10m < FA
⇒ m < 80 (tấn)
Khối lượng của hàng đặt lên sà lan là:
mh < m − ms ⇒ mh < 80 − 50
⇒ mh < 30 (tấn)
Nhóm máu không mang kháng thể α và β có thể truyền được cho nhóm máu nào dưới đây?
Nhóm máu không mang kháng thể α và β là nhóm máu AB.
⇒ Nhóm máu này chỉ có thể truyền được cho nhóm máu AB.
Điều chế khí oxygen bằng cách nhiệt phân 1 mol KClO3 thì thu được 43,2 g khí oxygen và một lượng potassium chloride (KCl). Tính hiệu suất phản ứng.
Phương trình hóa học:
2KClO3 2KCl + 3O2
mol: 1 → 1,5
Khối lượng oxygen thu được theo lý thuyết là:
mO2 lt = 1,5.32 = 48 (g)
Hiệu suất của phản ứng là:
Chọn phép biến đổi sai.
Phép biến đổi sai là: 1 kg/m3 = 0,01 g/cm3.
Đúng: 1 kg/m3 = 0,001 g/cm3
Phế quản thuộc hệ cơ quan nào sau đây?
Phế quản là cơ quan thuộc hệ hô hấp.
Cho V1 ml dung dịch Na2SO4 0,3 M vào V2 ml dung dịch Na2SO4 1,7 M thu được 1400 ml dung dịch Na2SO4 0,6 M. Tính V1 và V2.
Số mol chất tan có trong V1 ml dung dịch Na2SO4 0,3 M là:
Số mol chất tan có trong V2 ml dung dịch Na2SO4 1,7 M là:
⇒ Tổng số mol chất tan là:
nct = nNa2SO4 (1) + nNa2SO4 (2) = 0,0003V1 + 0,0017V2
Mặt khác, theo đề ra trong 1400 ml dung dịch Na2SO4 0,6 M có số mol chất tan là:
nct = 1,4.0,6 = 0,84 (mol)
⇒ 0,0003V1 + 0,0017V2 = 0,84 (1)
Tổng khối lượng dung dịch là:
V = V1 + V2 ⇒ V1 + V2 = 1400 (2)
Từ (1) và (2) ⇒ V1 = 1100; V2 = 300
Vậy V1 = 1100 ml và V2 = 300 ml
Áp suất tác dụng vào chất lỏng:
Áp suất tác dụng vào chất lỏng sẽ được chất lỏng truyền đi nguyên vẹn theo mọi hướng.
Phát biểu nào sau đây đúng khái niệm áp lực?
Áp lực là lực ép có phương vuông góc với bề mặt bị ép.
Một bình đựng chất lỏng như hình dưới đây. Áp suất tại điểm nào là lớn nhất?
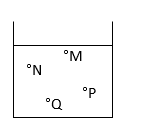
Ta có: Áp suất chất lỏng tăng dần theo độ sâu Áp suất tại điểm Q là lớn nhất, tại điểm M là nhỏ nhất.
Khi nhai kĩ bánh mì trong miệng ta thấy có vị ngọt vì:
Khi nhai kĩ bánh mì trong miệng ta thấy có vị ngọt vì enzyme amylase trong nước bọt làm biến đổi một phần tinh bột chín thành đường đôi (maltose) có vị ngọt.
Nguyên lí hoạt động của giác mút là:
Nguyên lí hoạt động của giác mút là: Khi áp mặt lõm của giác mút vào tường, không khí bên trong giác mút bị đẩy ra ngoài khiến áp suất không khí bên trong giảm. Sự chênh lệch giữa áp suất không khí ở bên ngoài và bên trong giác mút đẩy giác mút dính chặt vào tường.
