Quá trình nào sau đây là biến đổi hóa học?
Quá trình đốt cháy củi trong trong lò là biến đổi hóa học vì có chất mới sinh ra
Quá trình nào sau đây là biến đổi hóa học?
Quá trình đốt cháy củi trong trong lò là biến đổi hóa học vì có chất mới sinh ra
Khi đốt dây sắt trong không khí, sắt phản ứng cháy với oxygen theo phương trình:
3Fe + 2O2 ⟶ Fe3O4
Thể tích khí O2 (đkc) cần dùng để phản ứng hoàn toàn với 16,8 gam Fe là
Số mol Fe tham gia phản ứng là:
nFe = 16,8 : 56 = 0,3 mol
Phương trình phản ứng hóa học:
3Fe + 2O2 ⟶ Fe3O4
3 2 1
Theo tỉ lệ phương trình phản ứng, ta có:
nO2 = nFe = 0,3.
= 0,2 mol
Thể tích khí O2 ở điều kiện chuẩn là:
VO2 = n.24,79 = 0,2.24,79 = 4,958 L
Nồng độ mol của 0,05 mol KCl có trong 200 mL dung dịch là:
Đổi 200mL = 0,2L
Áp dụng công thức tính nồng độ mol
CM = n/V = 0,05 : 0,2 = 0,25M
Khi tăng nhiệt độ thì độ tan của chất rắn trong nước thay đổi như thé nào?
Khi tăng nhiệt độ thì độ tan của chất rắn trong nước phần lớn là tăng.
Vì có phần nhỏ chất rắn khi tăng nhiệt độ thì độ tăng giảm.
Hòa tan hoàn toàn 20 g đường vào 180 g nước thì thu được dung dịch nước đường có nồng độ bằng
Khối lượng dung dịch là:
mdung dịch = mct + mH2O = 20 + 180 = 200 g
Áp dụng công thức tính nồng độ phần trăm ta có:
Dụng cụ ở hình bên có tên gọi là gì và thường dùng để làm gì?


Pipette, dùng lấy hóa chất.
Các cơ quan trong ống tiêu hoá bao gồm:
Các cơ quan trong ống tiêu hoá bao gồm: miệng, hầu, thực quản, dạ dày, ruột non, ruột già.
Cơ quan nào dưới đây không nằm trong ống tiêu hóa?
Tuyến ruột không nằm trong ống tiêu hóa
Điền vào chỗ chấm lần lượt để được nội dung đúng:
Hệ cơ cũng có nhiều cơ, trong đó …(1)… là cơ bám vào xương nhờ các mô …(2)… như dây chằng, gân.
Hệ cơ cũng có nhiều cơ, trong đó cơ xương là cơ bám vào xương nhờ các mô liên kết như dây chằng, gân.
Việc làm nào sau đây không có lợi cho hệ vận động:
Bê vác đồ nặng thường xuyên ảnh hưởng không tốt cho sự phát triển và hoạt động của hệ vận động, dễ dẫn đến những bệnh tật liên quan đến hệ vận động như cong vẹo cột sống, trật khớp,…
Xương nào không nằm trong nhóm xương thân:
Phân loại các xương vào ba phần của bộ xương:
+ Xương đầu: Xương sọ não, xương sọ mặt.
+ Xương thân: Xương ức, xương sườn, xương sống.
+ Xương chi: Xương tay, xương chân.
Hệ cơ quan nào lọc các chất thải có hại cho cơ thể từ máu và thải ra môi trường?
Hệ bài tiết giúp lọc các chất thải có hại cho cơ thể từ máu và thải ra môi trường.
Ở cơ thể người, cơ quan nào sau đây nằm trong khoang bụng?
Ở cơ thể người, dạ dày là cơ quan nằm trong khoang bụng; tim, phổi, thực quản đều nằm trong khoang ngực.
Các bọt bong bóng xà phòng thường có dạng hình cầu bởi vì
Các bọt bong bóng xà phòng thường có dạng hình cầu bởi vì không khí bị giữ trong bọt tác dụng áp suất như nhau theo mọi hướng.
Trường hợp nào sau đây không do áp suất khí quyển gây ra?
Quả bóng bàn bị bẹp thả vào nước nóng sẽ phồng lên như cũ trường hợp chất khí nở ra vì nhiệt.
Cho hình vẽ sau:
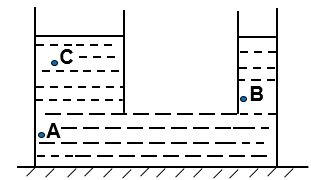
So sánh áp suất tại các điểm A, B, C trong hình trên nào dưới đây là đúng?
So với mặt thoáng chất lỏng, ta có: hA > hB > hC.
Do vậy, pA > pB > pC.
Nhận định nào sau đây không đúng
Đơn vị đo áp suất chất lỏng là N/m3 sai
Vì đơn vị đo áp xuất chất lỏng là N/m2, hoặc đo bằng Paxcan (Pa)
Một áp lực 750 N gây ra áp suất 3750 N/m2 lên diện tích bị ép có độ lớn
Áp dụng công thức tính áp suất
Diện tích bị ép có độ lớn
Từ công thức tính áp suất p = F/S. Để làm tăng áp suất ta cần:
Từ công thức tính áp suất p = F/S
Muốn tăng áp suất ta tăng áp lực hoặc giảm diện tích bị ép, ngược lại muốn giảm áp suất ta giảm áp lực và tăng diện tích bị ép.
Một khối gang hình hộp chữ nhật có chiều dài các cạnh tương ứng là 3 cm, 4 cm, 6 cm và có khối lượng 504 g. Hãy tính khối lượng riêng của gang.
Thể tích của khối gang là: V = 3 . 4 . 6 = 72 cm3.
Khối lượng riêng của gang là:
Phương trình hóa học nào sau đây biểu diễn đúng đúng quá trình nhiệt phân aluminium hydroxide sinh ra aluminium oxide và nước.
Nhiệt phân aluminium hydroxide sinh ra aluminium oxide và nước.
2Al(OH)3→ Al2O3+ 3H2O
Xác định hệ số a, b, c của phản ứng sau: aFe + bO2 ![]() cFe3O4
cFe3O4
Fe + O2 Fe3O4
Số nguyên tử Fe và O ở hai vế không bằng nhau, nhưng O có số nguyên tử nhiều hơn nên ta bắt đầu từ nguyên tố này trước.
Do O2 có 2 nguyên tử O còn Fe3O4 có 4 nguyên tử O nên ta đặt hệ số 2 trước O2;
Fe + 2O2 Fe3O4
Để cân bằng tiếp số nguyên tử Fe ta đặt hệ số 3 vào trước Fe ở vế trái.
3Fe + 2O2 Fe3O4
Phương trình hoá học của phản ứng hoàn thiện như sau:
3Fe + 2O2 → Fe3O4.
Hệ số a, b, c lần lượt là: 3:2:1
Cho luồng khí H2 đi qua ống thủy tinh chứa 20 gam bột CuO ở nhiệt độ cao. Sau phản ứng thu được 16,8 gam chất rắn. Hiệu suất của phản ứng là? Biết phương trình hóa học của phản ứng như sau:
CuO + H2 → Cu + H2O
Gọi x là số mol của H2
Phương trình phản ứng hóa học
CuO + H2 → Cu + H2O
Theo tỉ lệ số mol phương trình phản ứng ta có:
nH2O = nH2 = x mol
⇒ mH2O = 18x;
mH2 = 2x
Áp dụng định luật bảo toàn khối lượng ta có:
mCuO + mH2 = mCu + mH2O
⇔ 20 + 2x = 16,8 + 18x
⇒ x = 0,2 (mol)
Theo phương trình ta có
nCuO phản ứng = nH2 = 0,2 (mol)
⇒ mCuO phản ứng = 0,2.80 = 16 gam
Vậy hiệu suất phản ứng là:
Hòa tan 11,2 gam kim loại iron Fe vào dung dịch có chứa 14,6 gam hydrochloric acid HCl. Sau một thời gian, kim loại Fe tan hết thu được dung dich có chứa 25,4 gam muối iron (II) chloride FeCl2 và x gam khí hydrogen thoát ra. Tìm x gam:
Ta có phương trình phản ứng
Fe + 2HCl → FeCl2 + H2↑
Áp dụng bảo toàn khối lượng ta có:
mFe + mHCl = mFeCl2 + mH2
⇒ mH2 = mFe + mHCl - mFeCl2
⇒ mH2 = 11,2 + 14,6 - 25,4 = 0,4 gam
Khí hydrogen được điều chế trong phòng thí nghiệm bằng cách cho kim loại zinc tác dụng với dung dịch hydrochloric acid. Dấu hiệu nào chứng tỏ phản ứng có tạo ra khí hydrogen?
Dấu hiệu nào chứng tỏ phản ứng có tạo ra khí hydrogen kim loại zinc tan dần, có bọt khí bay lên.
Quá trình nào sau đây không phải là quá trình thu nhiệt?
Quá trình cho nước vào vôi sống (tôi vôi) là quá trình tỏa nhiệt
Quá trình nào sau đây có sự biến đổi hóa học?
Quá trình dây xích xe đạp bị gỉ có sự biến đổi hóa học
Những dụng cụ nào dưới đây dùng để đo thể tích chất lỏng trong phòng thí nghiệm?
Dụng cụ đo thể tích chất lỏng: Ống đong, cốc chia vạch, pipet, bình tam giác, ...
Khối lượng NaOH có trong 200 mL dung dịch nồng độ 0,15 M là
Áp dụng công thức tính nồng độ mol ta có:
Số mol NaOH:
nNaOH = 0,2.0,15 = 0,03 (mol).
Khối lượng NaOH:
mNaOH = 0,03.40 = 1,2 (gam).
Ở 25oC, độ tan của AgNO3 trong nước là 333 g. Để pha được 75 g dung dịch AgNO3 bão hoà ở 25oC, cần lấy bao nhiêu gam nước?
Nồng độ phần trăm của dung dịch AgNO3 bão hoà ở 25oC:
Áp dụng công thức tính nồng độ phần trăm
Khối lượng AgNO3 cần lấy để pha 50 g dung dịch bão hoà:
Khối lượng nước cần lấy:
mH2O = mdd - mAgNO3 = 75 - 57,68 = 17,32 (gam)
