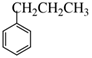
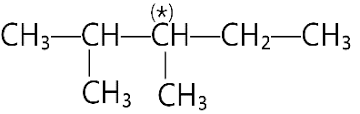
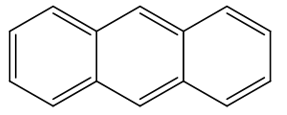
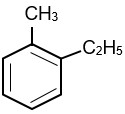
Trong các chất dưới đây, chất nào có nhiệt độ sôi thấp nhất?
Khi số nguyên tử carbon trong alkane tăng, tương tác van der Waals giữa các phân tử alkane tăng, dẫn đến nhiệt độ sôi và nhiệt độ nóng chảy của các alkane nói chung cũng tăng.
⇒ Alkane có nhiệt độ sôi thấp nhất là alkane có số carbon nhỏ nhất: methane








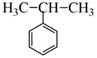 ;
;