Trường hợp nào dưới đây có hiệu điện thế bằng 0?
Trường hợp không có hiệu điện thế là giữa hai đầu bóng đèn có ghi 2,5V khi chưa mắc vào mạch vì bóng điện không được mắc với nguồn điện nên hiệu điện thế của nó bằng 0.
Trường hợp nào dưới đây có hiệu điện thế bằng 0?
Trường hợp không có hiệu điện thế là giữa hai đầu bóng đèn có ghi 2,5V khi chưa mắc vào mạch vì bóng điện không được mắc với nguồn điện nên hiệu điện thế của nó bằng 0.
Cho V ml dung dịch A gồm hai acid HCl 0,1 M và H2SO4 0,1 M trung hòa vừa đủ 30 ml dung dịch B gồm hai base NaOH 0,8 M và Ba(OH)2 0,1 M. Trị số của V là?
nOH- = nNaOH + 2.nBa(OH)2 = 0,8.0,03 + 2.0,1.0,03 = 0,03 (mol)
nH+ = nHCl + 2.nH2SO4 = V.0,1 + 2.V.0,1 = 0,3V
Phương trình phản ứng trung hòa:
H+ + OH– → H2O
mol: 0,03 ← 0,03
⇒nH+ = 0,3V = 0,03
⇒ V = 0,1 (l) = 100 ml
Cho các phát biểu sau:
(1) Xoang mũi có hệ thống mao mạch dày đặc có chức năng làm ấm không khí.
(2) Xoang mũi có tuyến tiết chất nhầy có chức năng làm ẩm không khí trước khi vào phổi.
(3) Xoang mũi có hệ thống mao mạch dày đặc, có chức năng trao đổi không khí: O2 đi từ xoang mũi vào mao mạch, CO2 đi từ mao mạch ra xoang mũi.
(4) Xoang mũi có nhiều lông mũi có chức năng lọc không khí.
Phát biểu nào là đúng?
(1), (2), (4) Đúng. Xoang mũi có lớp niêm mạc tiết chất nhầy, có nhiều lông mũi và lớp mao mạch dày đặc giúp ngăn bụi, làm ẩm, làm ấm không khí vào phổi.
(3) Sai. Trao đổi không khí là chức năng của phế nang.
Acid nào sau đây có trong giấm ăn với nồng độ khoảng 4%?
Acetic acid (CH3COOH) là một acid hữu cơ có trong giấm ăn với nồng độ khoảng 4%.
Phát biểu nào sau đây là sai?
Các vật liệu cao su, nhựa, sứ là các vật liệu cách điện không cho dòng điện chạy qua.
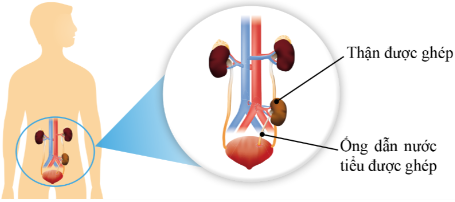
Vị trí thận mới được ghép vào cơ thể là
Vị trí thận mới được ghép vào cơ thể là trong ổ bụng, giữa thận bị suy và bóng đái.
Bạn B có thể nhìn bình thường ở cự ly xa nhưng không nhìn rõ những mục tiêu ở cự li gần. Hỏi bạn B bị bệnh hay tật gì liên quan đến mắt?
Người bị viễn thị có thể nhìn bình thường đối với những mục tiêu ở cự ly xa, song không nhìn rõ những mục tiêu ở cự ly gần.
Cơ quan nào dưới đây không phải là cơ quan có chức năng bài tiết?
Các cơ quan bài tiết gồm: da, gan, thận, phổi.
Muốn đo hiệu điện thế giữa hai đầu ổ cắm điện trong nhà, ta phải chỉnh trên vôn kế có giới hạn đo:
Muốn đo hiệu điện thế giữa hai đầu ổ cắm điện trong nhà, ta phải chỉnh trên vôn kế có giới hạn đo điện xoay chiều (AC), GHĐ lớn hơn 220 V.
Cho 3,6 gam Mg vào lượng dư dung dịch hydrochloric acid HCl. Sau khi phản ứng xảy ra hoàn toàn, thu được m gam muối magnesium chloride. Giá trị của m là:
Phương trình hóa học:
Mg + 2HCl → MgCl2 + H2
mol: 0,15 → 0,15
⇒ m = 0,15.95 = 14,25 (g)
Điều kiện để có dòng điện là
Điều kiện để có dòng điện là chỉ cần duy trì một hiệu điện thế giữa hai đầu vật dẫn.
Khi dây chì của cầu chì trong lớp học bị đứt, để đảm bảo an toàn cho mạng điện ta có thể dùng cách nào sau đây?
Khi dây chì của cầu chì trong lớp học bị đứt, để đảm bảo an toàn cho mạng điện nên thay bằng một dây chì khác cùng loại với dây chì bị đứt.
Dãy gồm các dung dịch nào sau đây làm đổi màu quỳ tím thành đỏ?
Các dung dịch HCl, H2SO4, HNO3, H3PO4 là các dung dịch acid làm quỳ tím chuyển sang màu đỏ.
Thiết bị sinh hoạt hàng ngày như bàn là, bếp điện hoạt động dựa vào:
Thiết bị sinh hoạt hàng ngày như bàn là, bếp điện hoạt động dựa vào tác dụng nhiệt của dòng điện
Hai vật mang điện trái dấu đặt gần nhau sẽ không thể
Hai vật mang điện trái dấu đặt gần nhau sẽ không thể đẩy nhau.
Cho các dung dịch và chất lỏng sau: HCl, NaOH, H2O. Trình tự tăng dần giá trị pH của các dung dịch, chất lỏng này là
Ta có: Dung dịch HCl có pH < 7; nước có pH = 7; dung dịch NaOH có pH > 7.
⇒ Trình tự tăng dần giá trị pH của các dung dịch, chất lỏng này là:
HCl < H2O < NaOH.
Các phát biểu dưới đây:
(1) Nguyên tử được cấu tạo từ hạt nhân mang điện dương và các electron mang điện âm đứng yên ở gần đó.
(2) Khi các vật cọ xát với nhau, các electron có thể di chuyển từ vật này sang vật khác làm cho chúng trở nên nhiễm điện.
(3) Hai vật mang điện cùng dấu sẽ hút nhau.
(4) Hai vật mang điện trái dấu sẽ đẩy nhau.
Phát biểu nào sai?
(1) Sai. Nguyên tử được cấu tạo từ hạt nhân mang điện dương và các electron mang điện âm chuyển động xung quanh hạt nhân.
(2) Đúng.
(3) Sai. Hai vật mang điện cùng dấu sẽ đẩy nhau.
(4) Sai. Hai vật mang điện trái dấu sẽ hút nhau.
Dòng điện không có tác dụng nào dưới đây?
Dòng điện không có tác dụng nhiễu xạ.
Dung dịch NaOH có thể tác dụng với dung dịch nào sau đây?
Dung dịch NaOH có thể tác dụng với dung dịch HCl.
NaOH + HCl → NaCl + H2O
Phản ứng nào sau đây đúng?
Phản ứng đúng là: Cu(OH)2 + 2HNO3 → Cu(NO3)2 + 2H2O
Sửa các phản ứng còn lại:
2NaOH + H2SO4 → Na2SO4 + 2H2O
Ba(OH)2 + 2HCl → BaCl2 + 2H2O
KOH + HNO3 → KNO3 + H2O
Kí hiệu sau đây là của thiết bị điện nào?
![]()
Kí hiệu ![]() là của điôt phát quang (đèn LED).
là của điôt phát quang (đèn LED).
Bộ phận gồm hai ống, phân nhánh nhiều lần, nối khí quản với phổi là
Bộ phận gồm hai ống, phân nhánh nhiều lần, nối khí quản với phổi là phế quản.
Thông thường các loại nước, bao gồm cả nước uống duy trì độ pH trong khoảng 6,5 - 8,5. Khi môi trường bị ô nhiễm bởi các chất khí SO2, NO2…sinh ra trong sản xuất công nghiệp và đốt cháy nhiên liệu tạo thành nước mưa có độ pH < 5,6. Nước mưa này tích tụ ở sông hồ có thể giết chết cá và nhiều sinh vật khác; cũng là nguyên nhân phá hủy nhiều công trình xây dựng bằng kim loại. Hiện tượng trên được gọi tên là gì?
Hiện tượng nước mưa có pH < 5,6 là hiện tượng mưa acid.
Để hoà tan vừa hết 4,48 gam Fe phải dùng bao nhiêu ml dung dịch hỗn hợp HCl 0,5 M và H2SO4 0,75 M?
nFe = 0,08 mol
Gọi thể tích dung dịch hỗn hợp acid cần dùng là V (lít)
⇒ nHCl = 0,5V mol, nH2SO4 = 0,75V mol
Phương trình hóa học:
Fe + 2HCl → FeCl2 + H2
mol: 0,25V ← 0,5V
Fe + H2SO4 → FeSO4 + H2
mol: 0,75V ← 0,75V
⇒ nFe = 0,25V + 0,75V = 0,08
⇒ V = 0,08 lít = 80 ml
Bộ phận, cơ quan nào dưới đây không thuộc cơ quan thính giác?
Cơ quan cảm giác âm thanh gồm tai (tai ngoài, tai giữa, tai trong), dây thần kinh thính giác và trung khu thính giác ở não bộ. Cơ quan thính giác có chức năng nhận biết âm thanh.
Nhỏ từ từ dung dịch NaOH 1M vào 50 mL dung dịch H2SO4. Khi H2SO4 được trung hoà hoàn toàn thì thấy dùng hết 40 mL dung dịch NaOH. Tính nồng độ dung dịch H2SO4 ban đầu.
Số mol NaOH đã phản ứng là:
nNaOH = 0,04.1 = 0,04 (mol).
Phương trình phản ứng:
2NaOH + H2SO4 → Na2SO4 + 2H2O
Số mol: 0,04 → 0,02 mol
Vậy nồng độ dung dịch H2SO4 ban đầu là:
Để đo cường độ dòng điện khoảng 120 mA, ta nên chọn ampe kế nào trong các ampe kế sau?
- GHĐ là độ lớn lớn nhất mà dụng cụ đo được
- ĐCNN là độ lớn nhỏ nhất mà dụng cụ đo được.
Để đo cường độ dòng điện 120 mA, nên ta chọn ampe kế phù hợp nhất là ampe kế có GHĐ là 150 mA.
Cho các bước có trong sơ cứu người cảm lạnh như sau:
(1) Uống nước ấm hoặc ăn cháo ấm.
(2) Cởi hết quần áo ướt (nếu bị ướt).
(3) Gọi cấp cứu 115.
(4) Làm ấm bằng quần áo và chăn khô.
(5) Di chuyển bệnh nhân đến nơi khô ráo, ấm áp.
Thứ tự đúng các bước sơ cứu người cảm lạnh là:
Thứ tự đúng các bước sơ cứu người cảm lạnh là:
- Di chuyển bệnh nhân đến nơi khô ráo, ấm áp.
- Gọi cấp cứu 115.
- Cởi hết quần áo ướt (nếu bị ướt ).
- Làm ấm bằng quần áo và chăn khô.
- Uống nước ấm hoặc ăn cháo ấm.
Tên gọi của base Al(OH)3 là
Tên gọi của base Al(OH)3 là aluminium hydroxide.
Cho những thành phần sau:
1) Máu.
(2) Nước tiểu.
(3) Dịch mô.
(4) Dịch bạch huyết.
(5) Dịch tiêu hóa.
Những thành phần thuộc môi trường trong cơ thể là
Môi trường trong cơ thể bao gồm máu, dịch mô (dịch giữa các tế bào) và dịch bạch huyết → (1), (3), (4).
