Công thức hóa học của Magnesium carbonate là:
Công thức hóa học của Magnesium carbonate là MgCO3
MgSO4: magnesium sulfate
Mg(NO3)2: magnesium nitrate.
MgCl2: Magnesium chloride
Công thức hóa học của Magnesium carbonate là:
Công thức hóa học của Magnesium carbonate là MgCO3
MgSO4: magnesium sulfate
Mg(NO3)2: magnesium nitrate.
MgCl2: Magnesium chloride
Cho dung dịch chứa 32,5 gam muối chloride của một kim loại M tác dụng với 300 mL dung dịch NaOH vừa đủ, thu được 21,4 gam kết tủa. Công thức muối chloride là:
Gọi hóa trị của kim loại M là n,
⇒ Muối có công thức MCln; số mol muối là a mol.
MCln + nNaOH → M(OH)n + nNaCl
a → na a na mol
Ta có theo đầu bài
Khối lượng muối là 32,5 gam nên:
a(M + 35,5n) = 32,5
(1)
Khối lượng kết tủa là 21,4 gam nên: a(M + 17n) = 21,4 (2)
(2)
Từ (1) và (2) ta có:
⇔ 32,5.(M + 17n) = 21,4(M + 35,5n)
⇔ 11,1M = 207,2n
Vậy n = 3; M = 56 thoả mãn.
Kim loại M là Fe, muối là FeCl3.
Vào năm 1991, các nhà khoa học đã phát hiện ra xác ướp Otzi - xác ướp tự nhiên được tìm thấy trong tuyết lạnh (có niên đại cách đây 5300 năm) trên dãy núi Alps gần biên giới giữa Áo và Italy. Việc bảo quản xác ướp này dựa trên ảnh hưởng của yếu tố nào đến tốc độ phân hủy xác?
Yếu tố ảnh hưởng là: Nhiệt độ
Tuyết lạnh có nhiệt độ rất thấp, nhiệt độ này gây ức chế sự phát triển của các vi sinh vật phân hủy xác ướp. Vì vậy quá trình phân huỷ xác cũng bị ức chế nên xác ướp không cần đến hoá chất mà vẫn giữ nguyên vẹn hình thể.
Phát biểu nào sau đây sai khi nói về đặc điểm của áp suất chất lỏng?
Chất lỏng gây ra áp suất theo mọi phương lên các vật ở trong lòng nó.
Móc một quả nặng vào lực kế, số chỉ của lực kế là 10 N. Nhúng quả nặng đó vào nước, số chỉ của lực kế thay đổi như thế nào?
Do khi nhúng vật vào nước, vật chịu tác dụng của lực đẩy Acsimet hướng lên trên ⇒ số chỉ của lực kế sẽ giảm đi.
Trong các hiện tượng sau đây, hiện tượng nào không do áp suất khí quyển gây ra?
Vật rơi từ trên cao xuống do lực hút của Trái Đất, không do áp suất khí quyển gây ra.
Gió gây ra áp suất lên bất kì một bề mặt nào mà gió thổi vào. Nếu gió gây ra một áp suất 2000 Pa lên một cánh cửa có diện tích là 3,5 m2 thì áp lực tác dụng lên cánh cửa bằng bao nhiêu?
Áp lực tác dụng lên cánh cửa là F = p.S = 2000.3,5 = 7000 N.
Biết tỉ khối của khí B so với oxygen là 0,5 và tỉ khối của khí A đối với khí B là 2,125. Xác định khối lượng mol của khí A.
Tỉ khối của khí B so với oxygen là 0,5
Lại có tỉ khối của khí A đối với khí B là 2,125
Khối lượng của nguyên tố N có trong 100 gam (NH2)2CO là
Khối lượng của nguyên tố N có trong 100 gam (NH2)2CO là:
Sản phẩm tạo khi cho dung dịch KOH dư tác dụng với khí sulfur dioxide là
Phương trình phản ứng:
NaOH (dư) + SO2 → Na2SO3 + H2O
Sản phẩm tạo khi cho dung dịch KOH dư tác dụng với khí sulfur dioxide là K2SO3 và H2O.
Quá trình biến đổi hóa học là
Quá trình biến đổi hóa học là quá trình chất biến đổi có sự tạo thành chất mới.
Muốn đo khối lượng riêng của một vật rắn không thấm nước ta cần những dụng cụ gì?
- Dùng cân để xác định khối lượng của vật rắn không thấm nước.
- Dùng bình chia độ để đo thể tích của vật rắn.
Muối nào sau đây là không tan?
BaSO4 là muối khan không tan.
BaCl2 và Ba(NO3)2 là muối tan.
Al(OH)3 là base.
Chất nào sau đây không phản ứng với zinc?
Chất không phản ứng với zinc là NaNO3.
2CH3COOH + Zn → (CH3COO)2Zn + H2
H2SO4 + Zn → ZnSO4 + H2
2HCl + Zn → ZnCl2 + H2
Ứng dụng nào sau đây không phải của của acetic acid?
Ứng dụng không phải của của acetic acid là sản xuất phân bón.
Cặp base nào sau đây không tan trong nước.
Cặp base Cu(OH)2 và Fe(OH)3 không tan trong nước
Cho phương trình phản ứng sau: Fe2O3 + H2SO4 → Fe2(SO4)3 + H2O. Hệ số cân bằng của phương trình là:
Sơ đồ phản ứng:
Fe2O3 + H2SO4 → Fe2(SO4)3 + H2O
Số nhóm (SO4) ở vế phải và vế trái chưa bằng nhau, ta đặt hệ số 3 trước H2SO4.
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + H2O
Số nguyên tử H ở vế phải và vế trai chưa bằng nhau ta thêm 3 ở trước phân tử H2O
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
Phương trình phản ứng hoàn chỉnh
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
→ Hệ số cân bằng của phương trình là 1:3:1:3.
Một khối hình hộp chữ nhật có thể tích 60 cm3, khối lượng 48 g. Khối lượng riêng của vật liệu làm khối hình hộp là
Khối lượng riêng của vật liệu làm khối hình hộp là:
Thang pH thường dùng có giá trị:
Thang pH thường dùng có giá trị từ 1 đến 14.
Cho hai quá trình sau:
(1) Đun nước đá nóng chảy thành nước lỏng.
(2) Nung thuốc tím rắn chuyển thành bột màu đen và có khí không màu thoát ra.
Kết luận đúng là:
Quá trình (1) là quá trình biến đổi vật lí do nước chỉ biến đổi trạng thái mà không tạo thành chất mới.
Quá trình (2) là biến đổi hóa học do thuốc tím ban đầu bị biến đổi và có tạo ra chất mới (bột màu đen và khí thoát ra).
Điểm nào trong hình dưới đây là điểm tựa của đòn bẩy?

Điểm tựa của đòn bẩy là điểm N.
Hiện tượng xảy ra khi nhỏ từ từ đến dư dung dịch Ba(OH)2 vào dung dịch chứa H2SO4 là:
Nhỏ từ từ đến dư dung dịch Ba(OH)2 vào dung dịch chứa H2SO4 xuất hiện kết tủa trắng.
Ba(OH)2 + H2SO4 → BaSO4 + H2O
Một thanh thẳng có thể quay quanh trục O như dưới hình lần lượt tác dụng lực F (phương thẳng đứng, chiều từ trên xuống dưới, độ lớn không đổi) vào các vị trí A, B, C, O. Tác dụng làm quay của lực F tại vị trí nào là lớn nhất?

Vị trí A xa trục quay nhất nên tác dụng làm quay của lực F tại vị trí A là lớn nhất.
Tình huống nào sau đây xuất hiện mômen lực?
Moomen lực xuất hiện khi lực làm vật quay tại một điểm cố định.
⇒ Cánh cửa quay quanh bản lề xuất hiện moomen lực.
Lượng chất nào sau đây chứa số mol nhiều nhất?
Áp dụng công thức tính số mol:
| O2 | SO2 | CuSO4 | Fe2O3 | |
| Khối lượng (m) | 8 | 4 | 8 | 16 |
| Khối lượng mol (M) | 32 | 64 | 160 | 160 |
| Số mol tính được (n) | 0,25 | 0,0625 | 0,05 | 0,1 |
Vậy 8 gam O2 chứa số mol nhiều nhất.
Cho oxide của kim loại R có hóa trị III, trong đó R chiếm 70% về khối lượng. Công thức của oxide là
Kim loại R có hóa trị III ⇒ Gọi công thức chung của oxide là: R2O3
R chiếm 70% về khối lượng của oxide:
⇒ R = 56
Vậy công thức oxide sắt là Fe2O3.
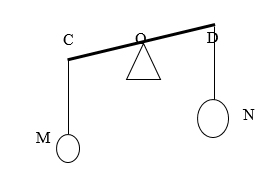
Có hai vật: Vật M bằng sắt, vật N bằng nhôm có cùng khối lượng. Hai vật này treo vào 2 đầu của thanh CD (CO = OD), như hình vẽ. Nếu nhúng ngập cả 2 vật vào trong rượu thì thanh CD sẽ:

Ta thấy, thể tích của vật bằng nhôm lớn hơn.
⇒ Lực đẩy Acsimet tác dụng lên vật bằng nhôm lớn hơn ⇒ Phía đầu D được lực đẩy nâng lên nhiều hơn dẫn đến thanh CD nghiêng về phía bên trái.
Trộn lẫn 2 lít dung dịch urea 0,02 M (dung dịch A) với 3 lít dung dịch urea 0,1 M (dung dịch B), thu được 5 lít dung dịch C. Tính nồng độ mol của dung dịch C.
Trong dung dịch A:
nurea 1 = 0,02.2 = 0,04 (mol)
Trong dung dịch B:
nurea 2 = 0,1.3 = 0,3 (mol)
Số mol ure sau khi trộn là:
nurea = 0,34 (mol)
Trong các loại phân bón hoá học sau loại nào là phân đạm?
Phân đạm là những phân chuyên cung cấp nguyên tố dinh dưỡng nitrogen cho cây trồng.
⇒ Phân đạm là: (NH2)2CO.
Cho 3,25 gam Zn tác dụng vừa đủ với dung dịch HCl. Dẫn toàn bộ khí thu được qua CuO dư đun nóng, thu được m gam kim loại Cu. Tính giá trị của m.
Số mol Zn đem phản ứng là:
Phương trình phản ứng:
Zn + 2HCl → ZnCl2 + H2
mol: 0,05 → 0,05
Khí thu được là H2, dẫn khí H2 qua CuO:
H2 + CuO Cu + H2O
mol: 0,05 → 0,05
mCu = 0,05.64 = 3,2 (g)
