Khử aldehyde bằng NaBH4 thu được sản phẩm là một alcohol bậc mấy?
Dưới tác dụng của NaBH4 hoặc LiAlH4, aldehyde bị khử sinh ra alcohol bậc một.
C2H5CHO + 2[H] CH3CH2CH2OH
Khử aldehyde bằng NaBH4 thu được sản phẩm là một alcohol bậc mấy?
Dưới tác dụng của NaBH4 hoặc LiAlH4, aldehyde bị khử sinh ra alcohol bậc một.
C2H5CHO + 2[H] CH3CH2CH2OH
Khối lượng ethylene thu được khi đun nóng 230 g ethanol (C2H5OH) với H2SO4 đậm đặc, hiệu suất phản ứng đạt 40% là
nC2H5OH = 5 (mol)
Phương trình phản ứng:
CH3CH2OH CH2=CH2 + H2O
mol: 5 → 5
Do hiệu suất phản ứng đạt 40% nên:
methylene = 5.28.40% = 56 (gam)
Hai hợp chất hữu cơ X và Y có cùng công thức phân tử C3H4O2. X tác dụng với CaCO3 tạo ra CO2. Y tác dụng với dung dịch AgNO3/NH3 tạo Ag. Công thức cấu tạo thu gọn phù hợp của X, Y lần lượt là
Theo bài ra ta có:
X tác dụng với CaCO3 tạo ra CO2 X hợp chất có nhóm -COOH
Y tác dụng với dung dịch AgNO3/NH3 tạo Ag Y là hợp chất có nhóm -CHO.
Vì X và Y có cùng công thức phân tử C3H4O2 X và Y là CH2=CHCOOH, HOCCH2CHO.
Hỗn hợp X gồm hai aldehyde no, mạch hở. Đốt cháy hoàn toàn hỗn hợp X tạo ra số mol nước đúng bằng số mol X đã phản ứng. Mặt khác khi cho 0,25 mol hỗn hợp X phản ứng hoàn toàn với lượng dư dung dịch AgNO3/NH3, thu được m gam Ag. Giá trị của m là:
Gọi công thức phân tử của hai aldehyde no, mạch hở X là:
Giả sử đốt cháy 1 mol X:
nH2O = 1 mol
Vậy 2 công thức phân tử của hai aldehyde no, mạch hở là HCHO và CHO-OHC:
Ta có sơ đồ: X + AgNO3 → 4Ag
0,25 mol → 1 mol
nAg = 4nX = 4. 0,25 = 1 (mol) mAg = 108 (g)
Tên thay thế của CH3-CH(CH3)-CH2-CHO là
Tên gọi theo danh pháp thay thế của aldehyde đơn chức:
Tên hydrocarbon (bỏ e ở cuối) + al
Lưu ý:
Đối với hợp chất carbonyl mạch nhánh hoặc có gốc hydrocacbon chưa no thì việc đánh số mạch chính bắt đầu từ phía đầu nào gần nhóm carbonyl hơn.
Cho Na tác dụng vừa đủ với 2,48 gam hỗn hợp 3 ancol đơn chức X, Y, Z thấy thoát ra 0,672 lít khí H2 (đkc). Khối lượng muối natri ancolat thu được là
Phương trình tổng quát
ROH + Na → RONa + 1/2 H2
nNa = 2.nH2 = 2. 0,672 : 22,4 = 0,06 mol
Áp dụng định luật bảo toàn khối lượng:
mMuối = mancol + mNa - mH2 = 2,48 + 0,06.23 – 0,03.2 = 3,8 gam
Cặp dung dịch nào sau đây đều có thể hòa tan Cu(OH)2 ở nhiệt độ thường?
Ở nhiệt độ thường:
C3H5(OH)3 + Cu(OH)2 [C3H5(OH)2O]2Cu + H2O
2CH3COOH + Cu(OH)2 (CH3COO)2Cu + 2H2O
Alcohol bị oxi hoá bởi CuO, t° tạo thành aldehyde là
- Alcohol bậc I bị oxi hoá bởi CuO, t° tạo thành aldehyde.
- Alcohol bậc II bị oxi hoá bởi CuO, t° tạo thành ketone.
- Alcohol bậc III không bị oxi hóa bởi CuO, t°.
⇒ CH3CH2OH bị oxi hoá bởi CuO, t° tạo thành aldehyde.
Các chất đều phản ứng được với dung dịch phenol
Br2 và NaOH đều phản ứng được với dung dịch phenol.
C6H5OH + 3Br2 → C6H2Br3OH + 3HBr
↓ trắng
C6H5OH + NaOH → C6H5ONa + H2O
Hydrocarbon X có công thức C8H10 không làm mất màu dung dịch bromine. Khi đun nóng X với dung dịch thuốc tím tạo thành C7H5KO2 (N). Cho N tác dụng với dung dịch aicd HCl tạo thành hợp chất C7H6O2. X có tên gọi nào sau đây?
Số nguyên tử H = 2.8 + 2 = 2k = 10 k = 4
X không tác dụng với dung dịch bromine không chứa liên kết đôi tự do
X chứa vòng benzene (3 liên kết π + 1 vòng).
X + dung dịch thuốc tím C7H5KO2
1 nhóm COOK
N + HCl C7H6O2
chỉ có 1 nhóm thế
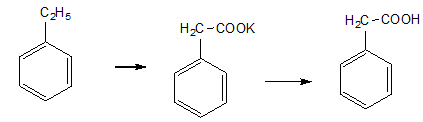
Nhận xét nào sau đây đúng?
Tính acid của phenol mạnh hơn so với alcohol.
Tính chất nào sau đây không phải là tính chất vật lí của alkene?
Chỉ dùng một chất nào trong các chất dưới đây để nhận biết được các chất: ethyl alcohol, glycerol, dung dịch aldehyde acetic đựng trong ba lọ mất nhãn?
Để nhận biết 3 chất trên ta sử dụng Cu(OH)2/OH-
Trích mẫu thử và đánh số thứ tự
Glycerol phản ứng với Cu(OH)2/OH- ở nhiệt độ thường tạo phức màu xanh.
Cu(OH)2 + 2C3H5(OH)3 → [C3H5(OH)2O]2Cu + 2H2O
Aldehyde acetic phản ứng với Cu(OH)2/OH- khi đún nóng tạo kết tủa đỏ gạch
CH3CHO + 2Cu(OH)2 + NaOH CH3COONa + Cu2O ↓ + 3H2O
Số liên kết σ có trong phân tử ethene; ethyne; buta-1,3-diene lần lượt là:
Ethene: CH2=CH2 gồm 1 liên kết π và 5 liên kết σ.
Ethyne: CHCH gồm 2 liên kết π và 3 liên kết σ.
Buta-1,3-diene: CH2=CH-CH=CH2 gồm 2 liên kết π và 9 liên kết σ.
Cho 54,5 g một alkyl chloride X tác dụng với dung dịch KOH trong C2H5OH đun nóng nhẹ, thu được V lít khí Y và 7,45 g muối Z. Xác định alkyl chloride X và thể tích khí thoát ra.
nKCl = 0,1 mol
Gọi công thức phân tử của alkyl chloride là CnH2n+1Cl
Phương trình hóa học:
CnH2n+1Cl + KOH CnH2n + KCl + H2O
0,1 ← 0,1 ← 0,1
Malkyl chloride = 5,45/0,1 = 54,5 (g/mol)
⇒ Công thức của X là C2H5Cl.
Thể tích khí thu được là:
VC2H4 = 0,1.24,79 = 2,479 lít
Dẫn xuất halogen bậc hai là:
Dẫn xuất halogen bậc hai là 2-chlorobutane: CH3CH2CHClCH3.
Tên gọi của CH3CH(CH3)CH2COOH là
Tên gọi của CH3CH(CH3)CH2 COOH là 3-methylbutanoic acid.
Tên thay thế alkene có công thức C2H4 là:
Tên thay thế alkene có công thức C2H4 là ethene còn Ethylene là tên thông thường
Hợp chất hữu cơ A có công thức phân tử là C4H10O có bao nhiêu đồng phân?
Các đồng phân của A là:
- Alcohol: CH3CH2CH2CH2OH; CH3CH2CH(OH)CH3; (CH3)2CHCH2OH; (CH3)3COH.
- Ether: CH3-O-CH2CH2CH3; CH3-O-CH(CH3)2; C2H5-O-C2H5.
Cho các nhận định sau về:
(1) Acetic aldehyde thể hiện tính oxi hóa khi tác dụng với H2 (xúc tác Ni, to)
(2) Aldehyde phản ứng với H2 (xúc tác Ni, to) tạo ra ancol bậc hai.
(3) Acetic acid không tác dụng được với Ca(OH)2.
(4) Phương pháp hiện đại để sản xuất acetic aldehyde là oxi hóa không hoàn toàn ethylene.
(5) Để điều chế aldehyde từ ancol bằng một phản ứng, người ta dùng ancol bậc 1.
Số phát biểu đúng là
(2) Aldehyde phản ứng với H2 (xúc tác Ni, to) luôn tạo ra alcohol bậc hai sai vì tạo ra alcohol bậc 1.
(3) Acetic acid không tác dụng được với Ca(OH)2 ⇒ Sai có phản ứng
Ca(OH)2 + 2CH3COOH → (CH3COO)2Ca ↓ + 2H2O.
Dãy sắp xếp các chất có nhiệt độ sôi tăng dần
Tương tác van der Waals ảnh hưởng đến nhiệt độ sôi của các dẫn xuất halogen, từ trái sang, số lượng nguyên tử chlorine tăng làm cho tương tác van der Waals tăng.
Thứ tự nhiệt độ sôi tăng dần theo chiều: CH4 < CH3Cl < CH2Cl2 < CHCl3 < CCl4.
Khử hợp chất hữu cơ X bằng LiAlH4, thu được (CH3)2CH-CH2-CH2OH. Chất X có tên là
Phương trình phản ứng
(CH3)2CH−CH2−CHO + 2[H] (CH3)2CH−CH2−CH2OH
Chất X là (CH3)2CH-CH2-CHO; có tên 3-methylbutanal.
Cặp chất nào sau đây là đồng phân?
o-cresol: o-CH3-C6H4-OH
Benzyl alcohol: C6H5-CH2OH
Cả 2 chất đều có công thức phân tử là C7H8O nên là đồng phân của nhau.
Hợp chất CH3CHO có tên thường là
Hợp chất CH3CHO có tên thường là acetic aldehyde.
Để phân biệt styrene và phenylacetylene chỉ cần dùng chất nào sau đây?
Phenylacetylene có công thức cấu tạo:
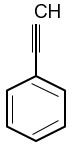
Phenylacetylene phản ứng được với dung dịch AgNO3/NH3 tạo ra kết tủa.
Cho 50 ml dung dịch (chứa 0,035 mol hỗn hợp một carboxylic acid đơn chức và muối của nó với một kim loại kiềm) tác dụng với 12 ml dung dịch Ba(OH)2 1,25M. Sau phản ứng, để trung hòa dung dịch cần thêm 3,75 gam dung dịch HCl 1,46%. Sau đó cô cạn dung dịch thì thu được 5,4325 gam muối khan. Nếu đem 50 ml dung dịch A ở trên tác dụng với 20 ml dung dịch NaOH 1M, phản ứng hoàn toàn, cô cạn dung dịch thì khối lượng chất rắn thu được là bao nhiêu?
nBa(OH)2 = 0,015 mol; nHCl = 0,015 mol
2HCl + Ba(OH)2 → BaCl2 + 2H2O
0,015 → 0,0075
nBa(OH)2 pư = 0,0075 mol
nacid = 2nBa(OH)2 = 0,015 mol
nmuối = 0,035 – 0,015 = 0,02 mol
Áp dụng định luật bảo toàn khối lượng ta có:
5,4325 = mBaCl2 + mhh ban đầu + mtăng của hỗn hợp pư với Ba(OH)2
5,4325 = 0,0075.208 + mhh ban đầu + 0,0075.(137 – 2)
mhh ban đầu = 2,86 gam
Khi tác dụng với NaOH thì khối lượng chất rắn thu được gồm NaOH dư và khối lượng muối.
Áp dụng tăng giảm khối lượng:
mrắn = 2,86 + 0,015.22 + 0,005.40 = 3,39 gam
Cho các phát biểu sau:
(a) Aldehyde có nhóm carbonyl trong phân tử còn alcohol thì không.
(b) Aldehyde phản ứng với nước bromine còn alcohol thì phản ứng dễ dàng với sodium.
(c) Aldehyde có phản ứng với Cu(OH)2 trong môi trường base còn alcohol thì có phản ứng tráng bạc.
(d) Aldehyde có phản ứng với hydrogen cyanide còn alcohol thì không.
Những phát biểu đúng về sự khác biệt giữa aldehyde và alcohol là
(c) sai vì alcohol không có phản ứng tráng bạc.
Cho các chất sau: (1) C3H8, (2) C2H5OH, (3) CH3CHO, (4) CH3COOH. Thứ tự các chất theo chiều tăng dần nhiệt độ sôi từ trái sang phải là
Khi phân tử khối của các chất chênh lệch nhau không nhiều thì nhiệt độ sôi của các chất tăng dần từ alkane < aldehyde < alcohol < carboxylic acid.
Thứ tự các chất theo chiều tăng dần nhiệt độ sôi từ trái sang phải là (1), (3), (2), (4).
Hợp chất hữu cơ mạch hở có công thức chung là CnH2nO2 có thể thuộc dãy đồng đẳng nào sau đây?
Carboxylic acid no, đơn chức có công thức chung là CnH2nO2.
Trong điều kiện thích hợp glucose lên men tạo thành khí CO2 và chất nào dưới đây?
Trong điều kiện thích hợp glucose lên men tạo thành khí CO2 và C2H5OH.
C6H12O6 2C2H5OH + 2CO2
Cho các phản ứng sau:
(a) CH3CH2OH + CuO ![]()
(b) (CH3)2CHOH + CuO ![]()
(c) 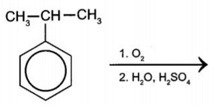
(d) CH≡CH + H2O ![]()
Số phản ứng sản phẩm tạo thành aldehyde là
Các phương trình phản ứng:
(a) CH3CH2OH + CuO CH3CHO + Cu + H2O
(b) (CH3)2CHOH + CuO CH3COCH3 + Cu + H2O
(c) 
(d) CH≡CH + H2O CH3CHO
Vậy các phản ứng sinh ra aldehyde là (a), (d).
Acetic acid (CH3COOH) không tác dụng được với chất nào sau đây?
Acetic acid (CH3COOH) không tác dụng được với Cu.
Oxi hóa alcohol nào sau đây thu được sản phẩm là aldehyde?
CH3CH2OH là alcohol bậc I bị oxi hóa thành aldehyde
Cho 0,1 mol hợp chất hữu cơ thơm X (C, H, O) tác dụng với 400 ml dung dịch MOH 1M (M là kim loại kiềm). Cô cạn dung dịch sau phản ứng thu được rắn khan Y. Đốt cháy toàn bộ lượng rắn khan Y bằng O2 dư; thu được 8,96 lít CO2 (đktc); 3,6 gam nước và 21,2 gam M2CO3. Số đồng phân cấu tạo của X là
nMOH = 0,4 mol; nCO2 = 0,4 mol; nH2O = 0,2 mol
Ta có:
nM2CO3 = ½ . nMOH = 0,2 mol
MM2CO3 = 2M + 60 = 21,2/0,2 = 106 g/mol
⇒ M = 23
⇒ M là Na
nC trong Y = nCO2 + nM2CO3 = 0,4 + 0,2 = 0,6 mol
⇒ Số C trong Y = 0,6/0,1 = 6 (nguyên tử)
Vậy Y có 6C ⇒ X có 6C
nH trong Y = 2.nH2O = 0,2.2 = 0,4 mol
Số H trong Y = 0,4/0,1 = 4 (nguyên tử)
Vậy công thức phân tử của Y là NaOC6H4ONa
⇒ Công thức phân tử của X là HOC6H4OH
⇒ X có 3 đồng phân cấu tạo.
Propanoic acid có công thức cấu tạo là
Propanoic acid là acid mà trong phân tử có 3 nguyên tử carbon.
Ứng dụng nào sau đây không còn được sử dụng?
Acid được dùng để sản xuất thủy tinh hữu cơ là
Acrylic acid và methacrylic acid được dùng để sản xuất thủy tinh hữu cơ.
Chất CH3-CH2-CH2-CO-CH3 có tên là gì?
Cho một dung dịch chứa 11,52 gam một carboxylic acid X đơn chức, mạch hở tác dụng hết với CaCO3 thu được 14,56 gam muối carboxylate. Công thức cấu tạo của X là
Gọi công thức của X là RCOOH.
2RCOOH + CaCO3 ⟶ (RCOO)2Ca + CO2↑ + H2O
Áp dụng phương pháp tăng giảm khối lượng
nX = (14,56 − 11,52) : 19 = 0,16 (mol)
⇒ MX = 11,52 : 0,16 = 72 (g/mol).
MR = 72 - 45 = 27
Vậy X có công thức là: CH2=CHCOOH.
Phương pháp điều chế ethanol từ chất nào sau đây là phương pháp sinh hóa?
Phương pháp sinh hóa sử dụng enzyme để lên men tinh bột và các loại đường trong tự nhiên, chuyển hóa thành ethanol:
(C6H10O5)n + nH2O nC6H12O6
C6H12O6 2C2H5OH + 2CO2
