Luyện tập tính chất hóa học oxit và axit
1. Tính chất hóa học của oxit
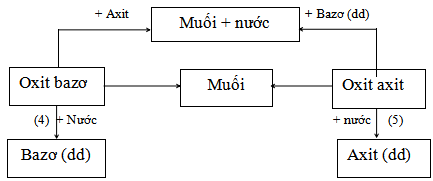
Sơ đồ tính chất hóa học của oxit
| Tính chất | Oxit axit | Oxit bazơ |
|
Tác dụng với nước
|
Nhiều oxit axit như P2O5, SO2, SO3, N2O5... tác dụng với nước tạo thành dung dịch axit. P2O5 + H2O → H3PO4 |
Một số oxit bazơ tác dụng được với nước tạo thành dung dịch bazơ tương ứng (kiềm). CaO + H2O → Ca(OH)2 |
| Tác dụng với dung dịch axit |
- |
Oxit bazơ tác dụng với axit tạo thành muối và nước. CuO + 2HCl → CuCl2 + H2O |
| Tác dụng với bazơ |
Oxit axit tác dụng với dung dịch bazơ tạo thành muối và nước CO2 + Ca(OH)2 → CaCO3 + H2O
|
- |
| Tác dụng với oxit axit |
- |
Một số oxit bazơ tác dụng với oxit axit tạo thành muối. CaO + CO2 → CaCO3 |
| Tác dụng với oxit bazơ |
Oxit axit tác dụng với một số oxit bazơ tạo thành muối. SO2 + Na2O → Na2SO3 |
- |
2. Tính chất hóa học của axit

Sơ đồ tính chất hóa học của axit
| Tính chất | Axit |
| Làm đổi màu quỳ tím | Axit làm quỳ tím chuyển sang màu đỏ. |
|
Tác dụng với kim loại |
Dung dịch axit tác dụng được với một số kim loại tạo thành muối và giải phóng khí hidro. 2Al + 6HCl → 2AlCl3 + 3H2 |
| Tác dụng với bazơ |
Axit tác dụng với bazơ tạo thành muối và nước. Phản ứng của axit với bazơ được gọi là phản ứng trung hòa. Cu(OH)2 + H2SO4 → CuSO4 + 2H2O |
| Tác dụng với oxit bazơ |
Axit tác dụng với oxit bazơ tạo thành muối và nước. Fe2O3 + 6HCl → 2FeCl3 + 3H2O |
| Tác dụng với muối |
Axit tác dụng với muối tạo muối mới và axit mới. H2SO4 + BaCl2 → BaSO4↓ + 2HCl |
Lưu ý: H2SO4 có những tính chất hóa học riêng
Tác dụng với kim loại không giải phóng khí hidro:
2H2SO4 (đặc) + Cu → CuSO4 + 2H2O + SO2
Tính háo nước, hút ẩm:
C12H22O11 ![]() 12C + 11H2O
12C + 11H2O








