Đề thi cuối kì 2 KHTN 7 phân môn Hóa sách Kết nối tri thức Nâng cao - Đề 1
Đề thi cuối kì 2 KHTN 7 phân môn Hóa sách Kết nối tri thức Nâng cao được biên soạn gồm 2 phần. Phần 1 gồm 30 câu hỏi trắc nghiệm khách quan. Phần 2 gồm 2 câu hỏi tự luận, giúp đánh giá đúng năng lực học tập.|
SỞ GIÁO DỤC VÀ ĐÀO TẠO TRƯỜNG THCS………………. |
ĐỀ THI HỌC KÌ II Môn: KHOA HỌC TỰ NHIÊN 7 Thời gian làm bài: … phút (không kể thời gian giao đề) |
Họ và tên học sinh: …………………………………………… Lớp: 7……..
Phần I: Trắc nghiệm (6,0 điểm)
Câu 1: Trong nguyên tử, hạt mang điện tích dương là
| A. electron. | B. proton. | C. neutron. | D. proton và electron. |
Câu 2: Kí hiệu nào sau đây là kí hiệu hóa học của nguyên tố magnesium?
| A. mg. | B. mG. | C. MG. | D. Mg |
Câu 3: Iron có hóa trị III trong công thức nào sau đây?
| A. FeO. | B. Fe2O3. | C. FeSO4. | D. FeCl2. |
Câu 4: Trong phân tử chlorine (Cl2), khi hai nguyên tử chlorine liên kết với nhau, chúng
A. góp chung proton.
B. chuyển electron từ nguyên tử này sang nguyên tử kia.
C. chuyển proton từ nguyên tử này sang nguyên tử kia.
D. góp chung electron.
Câu 5: Bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo nguyên tắc
| A. chiều nguyên tử khối tăng dần. | B. chiều điện tích hạt nhân tăng dần. |
| C. tính kim loại tăng dần. | D. tính phi kim tăng dần. |
Câu 6: Khối lượng phân tử của BaCO3 là
| A. 197 amu. | B. 137 amu. | C. 157 amu. | D. 177 amu. |
Câu 7: Nguyên tử nguyên tố argon (Z = 18) có bao nhiêu lớp electron?
| A. 2 lớp. | B. 1 lớp. | C. 3 lớp. | D. 4 lớp. |
Câu 8: Nguyên tố hóa học là những nguyên tử có cùng
| A. nguyên tử khối. | B. số proton. | C. số khối. | D. số neutron. |
Câu 9: Đây là sơ đồ nguyên tử nguyên tố nào?
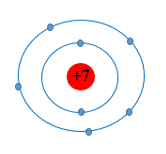
| A. Na. | B. N. | C. Al. | D. O. |
Câu 10: Nguyên tố oxygen có cùng số lớp electron với nguyên tố nào sau đây?
| A. Chlorine. | B. Fluorine. | C. Bromine. | D. Sulfur. |
Câu 11: Nguyên tố X thuộc nhóm VIIA, chu kì 3. Điện tích hạt nhân nguyên tử nguyên tố X là
| A. +17. | B. +16. | C. +15. | D. +20. |
Câu 12: Tính chất của nguyên tố bromine gần giống với tính chất của nguyên tố nào sau đây?
| A. Phosphorus. | B. Nitrogen. | C. Chlorine. | D. Sulfur. |
Câu 13: Số nguyên tố trong chu kỳ 3 và 5 là:
| A. 8 và 8. | B. 8 và 18. | C. 18 và 8. | D. 18 và 18. |
Câu 14: Cho các hợp chất sau: MgCl2, Na2O, NH3, HCl, NaCl. Hợp chất nào có liên kết cộng hóa trị?
| A. HCl và NaCl. | B. Na2O và NH3. | C. MgCl2 và Na2O. | D. NH3 và HCl. |
Câu 15: Nguyên tử của nguyên tố Y có 3 lớp electron, lớp electron ngoài cùng có 2 electron. Vị trí của nguyên tố X là
| A. thuộc chu kì 3, nhóm VIA. | B. thuộc chu kì 3, nhóm IIA. |
| C. thuộc chu kì 2, nhóm IIIA. | D. thuộc chu kì 2, nhóm IIA. |
Câu 16: Có các chất được biểu diễn bằng công thức hóa học sau: Zn, CO2, CaCO3, Br2, K, H2, CuO, Cl2. Số các đơn chất và hợp chất trong các chất trên là:
| A. 2 đơn chất và 6 hợp chất. | B. 5 đơn chất và 3 hợp chất. |
| C. 4 đơn chất và 4 hợp chất. | D. 3 đơn chất và 5 hợp chất. |
Câu 17: Nguyên tử nhôm aluminium (aluminium) có 13 electron ở vỏ. Số electron ở lớp trong cùng của nguyên tử nhôm là
| A. 2. | B. 8. | C. 10. | D. 18. |
Câu 18: Nguyên tử Ba khi nhường đi 2 electron thì tạo thành ion nào?
| A. Ba+. | B. Ba2+. | C. Ba–. | D. Ba2–. |
Câu 19: Cho một số công thức hóa học: MgCl, Ba3(SO4)2, Na2O, KCO3, H3SO4. Số công thức hóa học viết sai là
| A. 2. | B. 4. | C. 3. | D. 5. |
Câu 20: Phát biểu nào sau đây không đúng?
A. Các nguyên tố phi kim tập trung ở các nhóm VA, VIA, VIIA.
B. Các nguyên tố khí hiếm nằm ở nhóm VIIIA.
C. Các nguyên tố kim loại có mặt ở tất cả các nhóm trong bảng tuần hoàn.
D. Các nguyên tố lanthanide và actinide, mỗi họ gồm 14 nguyên tố được xếp riêng thành hai dãy ở cuối bảng.
Câu 21: Phân tử methane gồm 1 nguyên tử carbon liên kết với 4 nguyên tử hydrogen. Khối lượng phân tử methane là
| A. 16 amu. | B. 17 amu. | C. 15 amu. | D. 18 amu. |
Câu 22: Dãy nào sau đây gồm các nguyên tố đều là phi kim?
| A. F, O, Na, N. | B. H, N, O, K. | C. H, О, Cl, Вr. | D. K, Na, Mg, Al. |
Câu 23: Cho công thức hóa học R2O3. Biết khối lượng phân tử của R2O3 là 160. R là nguyên tố hóa học nào sau đây?
| A. Fe. | B. Cu. | C. Al. | D. Zn. |
Câu 24: Cho các chất sau:
(1) Khí nitrogen do nguyên tố N tạo nên.
(2) Khí carbon dioxide do 3 nguyên tố Na, O và H tạo nên.
(3) Sodium hydroxide do 3 nguyên tố Na, O và H tạo nên.
(4) Sulfur do nguyên tố S tạo nên.
Số chất là đơn chất trong những chất trên là
| A. 1. | B. 2. | C. 3. | D. 4. |
Câu 25: Hạt nhân của một nguyên tử potassium có 19 proton 20 neutron. Khối lượng nguyên tử potassium là
| A. 39 amu. | B. 41 amu. | C. 38 amu. | D. 40 amu. |
Câu 26: Hợp chất nào sau đây có phần trăm khối lượng nguyên tố aluminium (Al) là 32,92%?
| A. Al2O3. | B. Al(OH)3. | C. NaAlO2. | D. Al2(SO4)3. |
Câu 27: Khi đốt cháy một chất trong oxygen thu được khí carbon dioxide (CO2) và hơi nước (H2O). Nguyên tố nhất thiết phải có trong thành phần của chất mang đốt là
| A. carbon và hydrogen. | B. carbon và oxygen. |
| C. carbon, hydrogen và oxygen. | D. hydrogen và oxygen. |
Câu 28: Cho công thức phân tử calcium hydroxide: Ca(OH)2.
Nhận định nào sau đây sai?
A. Calcium hydroxide tạo bởi ba nguyên tố Ca, H và O.
B. Calcium hydroxide gồm 1 nguyên tử Ca, 2 nguyên tử O và 2 nguyên tử H.
C. Calcium hydroxide có khối lượng phân tử là 57 amu.
D. Calcium hydroxide là hợp chất.
Câu 29: Khi tạo thành liên kết trong phân tử NaCl, nguyên tử Cl có xu hướng
| A. nhận 1 electron. | B. nhường 1 electron. |
| C. góp chung 1 electron. | D. nhường 7 electron. |
Câu 30: Hợp chất của nguyên tố X với S là X2S3 và hợp chất của nguyên tố Y với H là YH3. Công thức hóa học hợp chất của X với Y là
| A. XY. | B. X2Y. | C. XY2. | D. X2Y. |
Phần II: tự luận (4,0 điểm)
Câu 31 (2 điểm): Hợp chất XY2 là chất góp phần gây nên hiệu ứng nhà kính. Biết rằng:
- Nguyên tử X có tổng số hạt (proton, neutron, electron) là 18 hạt, số hạt mang điện nhiều hơn số hạt không mang điện là 6 hạt.
- Nguyên tử Y có tổng số hạt là 24 hạt, trong hạt nhân nguyên tử Y, số hạt mang điện bằng số hạt không mang điện.
a) Hãy xác định số hạt mỗi loại trong các nguyên tử X, Y và cho biết X và Y là những nguyên tử của nguyên tố hóa học nào.
b) Xác định tên (theo danh pháp IUPAC) và cho biết loại liên kết giữa các nguyên tử trong hợp chất XY2.
Câu 32 (2 điểm): Hợp chất được tạo thành từ nguyên tố M và oxygen có khối lượng phân tử 160 amu. Trong đó, khối lượng của M chiếm 70%. Biết trong hợp chất trên, M có hóa trị III. Hãy xác định nguyên tố A và công thức hóa học của hợp chất.
H = 1 amu; C = 12 amu; N = 14 amu; O = 16 amu; Na = 23 amu; Al = 27 amu; S = 32 amu;
K = 39 amu; Fe = 56 amu; Cu = 64 amu; Zn = 65 amu; Ba = 137 amu
------------HẾT-----------








