Trong nguyên tử, hạt nào mang điện dương:
Cấu tạo nguyên tử gồm:
Hạt nhân:
+ Hạt proton (p) mang điện tích dương
+ Hạt neutron (n) không mang điện
Vỏ: tạo bởi các electron (e) mang điện tích âm
Trong nguyên tử, hạt nào mang điện dương:
Cấu tạo nguyên tử gồm:
Hạt nhân:
+ Hạt proton (p) mang điện tích dương
+ Hạt neutron (n) không mang điện
Vỏ: tạo bởi các electron (e) mang điện tích âm
Số electron tối đa ở lớp thứ nhất là
Số electron tối đa ở lớp thứ nhất là 2
Số electron tối đa ở lớp thứ hai là 8
Số electron tối đa ở lớp thứ ba là 8
Trừ hạt nhân của nguyên tử hydrogen, hạt nhân các nguyên tử còn lại được thành từ các hạt:
Trừ hạt nhân của nguyên tử hydrogen, hạt nhân các nguyên tử còn lại được thành từ các hạt eletron, proton và neutron.
Phát biểu nào sau đây không mô tả đúng mô hình nguyên tử của Rơ - dơ-pho- Bo
Nguyên tử có cấu tạo đặc khít, gồm hạt nhân nguyên tử và các electron mô tả không đúng vì nguyên tử có cấu tạo rỗng.
Số electron tối đa ở lớp thứ hai là:
Số electron tối đa ở lớp thứ hai 8
Phát biểu nào sau đây không mô tả đúng vỏ nguyên tử theo mô hình nguyên tử của Rơ – dơ – pho – Bo?
"Lớp electron trong cùng gần hạt nhân nhất có tối đa 8 electron, các lớp electron khác có chứa tối đa nhiều hơn 8 electron" không mô tả đúng vì:
Lớp electron trong cùng gần hạt nhân nhất có tối đa 2 electron, các lớp electron khác có chứa tối đa 8 electron hoặc nhiều hơn.
Ví dụ:
+ Lớp thứ nhất có tối đa 2 electron.
+ Lớp thứ 2 có tối đa 8 electron.
+ Lớp thứ 3 có tối đa 18 electron.
Một nguyên tử có 10 proton trong hạt nhân. Theo mô hình nguyên tử của Rơ – dơ – pho – Bo, số lớp electron của nguyên tử đó là
Ta có: số electron = số proton = 10.
Nguyên tử có 10 electron được phân bố vào 2 lớp (lớp thứ nhất có 2 electron, lớp thứ hai có 8 electron)
Muối ăn chứa hai nguyên tố hóa học là natri (sodium) và chlorine. Trong hạt nhân nguyên tử của các nguyên tố natri và chlorine có lần lượt 11 và 17 proton. Số electron ở lớp ngoài cùng của vỏ nguyên tử sodium và chlorine lần lượt là
+ Nguyên tử natri có số electron = số proton = 11.
Lớp electron bên trong gần hạt nhân có 2 electron, lớp tiếp theo có 8 electron.
Lớp ngoài cùng có: 11 – 8 – 2 = 1 electron.
+ Nguyên tử chlorine có số electron = số proton = 17.
Lớp electron bên trong, gần hạt nhân có 2 electron, lớp tiếp theo có 8 electron.
Lớp ngoài cùng có: 17 – 8 – 2 = 7 electron.
Nguyên tử X có tổng số hạt trong nguyên tử là 36. Biết số hạt không mang điện nhiều hơn số hạt mang điện là 12. Số electron lớp ngoài cùng của nguyên tử X là:
Gọi P, N và E lần lượt là số proton, neutron và electron của X.
Trong đó P = E.
Theo bài ra X có tổng số các hạt là 36 nên P + N + E = 36 hay
2P + N = 36 (1)
Biết số hạt không mang điện nhiều hơn số hạt mang điện là 12
2P - N = 12 (2)
Lấy (1) - (2) ta đươc: 2N = 24 ⇒ N = 12 ⇒ P = 12 = Z
Vẽ được mô tả nguyên tử X có
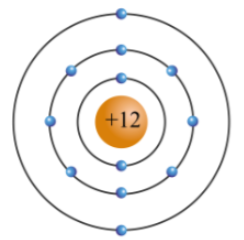
Nguyên tử X có 16 proton, số electron ở lớp ngoài cùng là
Nguyên tử lưu huỳnh (sulfur) có số electron = số proton = 16.
Lớp electron trong cùng, gần hạt nhân có 2 electron, lớp tiếp theo có 8 electron.
Lớp ngoài cùng có: 16 – 8 – 2 = 6 electron.
Trong nguyên tử, hạt không mang điện là
Trong nguyên tử, hạt không mang điện là neutron
Nguyên tử X có tổng số hạt là 52, trong đó số proton là 17. Số electron và số neutron lần lượt là:
Tổng số hạt trong nguyên tử là: p + e + n = 52
p = e = 17
⇒ n = 52 - 17 - 17 = 18
