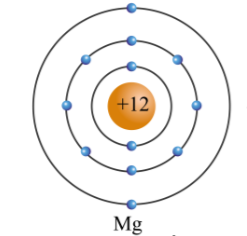
Vì sao có thể coi khối lượng nguyên tử bằng khối lượng hạt nhân?
Khối lượng của một nguyên tử bằng tổng khối lượng của proton, neutron và electron trong nguyên tử đó.
Proton và neutron đều có khối lượng xấp xỉ bằng 1 amu. Khối lượng của electron là 0,00055 amu, nhỏ hơn nhiều lần so với khối lượng của proton và neutron nên có thể coi khối lượng nguyên tử bằng khối lượng hạt nhân.