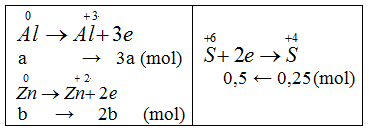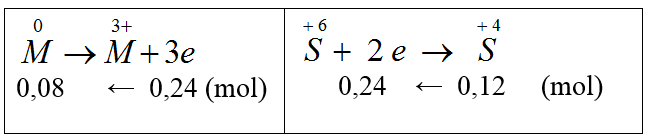Cho 4,8 gam kim loại R tan hoàn toàn trong dung dịch HNO3 đặc, nóng, dư thu được 8,96 lít khí NO2 (đktc). Kim loại R là
nNO2 = 0,4 mol
Quá trình nhường nhận electron
R0 → R+n +ne
nR → n.nR mol
N+5 + 1e → N+4
0,4 ← 0,4 (mol)
Áp dụng bảo toàn electron:
n.nR = nNO2 = 0,4 mol
→
Lập bảng biện luận ta có:
|
n |
1 |
2 |
3 |
|
M |
12 (Loại) |
24 (Mg) |
36 (Loại |
Vậy kim loại cần tìm là Mg