Cho 1 amu = 1,6605.10-27 kg. Nguyên tử khối của neon là 20,179 amu. Vậy khối lượng theo đơn vị kg của neon là
Ta có: mNe = NTK.mamu = 20,179.(1,6605.10 -27) = 33,5.10 -27 (kg)
Cho 1 amu = 1,6605.10-27 kg. Nguyên tử khối của neon là 20,179 amu. Vậy khối lượng theo đơn vị kg của neon là
Ta có: mNe = NTK.mamu = 20,179.(1,6605.10 -27) = 33,5.10 -27 (kg)
Số thứ tự chu kì trong bảng hệ thống tuần hoàn cho biết:
Số thứ tự chu kì trong bảng hệ thống tuần hoàn cho biết số lớp electron.
Có những tính chất sau đây của nguyên tố:
(1) Hóa trị của nguyên tố trong hợp chất với oxygen;
(2) Bán kính nguyên tử;
(3) Tính kim loại – phi kim;
(4) Tính acid - base của hợp chất hydroxide
Trong các tính chất trên, số tính chất biến đổi tuần hoàn trong một nhóm A là
Các tính chất 2, 3, 4 biến đổi tuần hoàn trong một nhóm.
Hóa trị của nguyên tố trong hợp chất với oxygen không biến đổi tuần hoàn trong một nhóm A.
Nội dung nào dưới đây không phải đối tượng nghiên cứu của hóa học?
Đối tượng nghiên cứu của hóa học là chất và sự biến đổi của chất.
⇒ Sự lớn lên và sinh sản của tế bào không phải đối tượng nghiên cứu của chất.
Cation M2+ có cấu hình electron ở phân lớp ngoài cùng là 2p6. Phần trăm khối lượng của M trong oxide cao nhất là
Cấu hình electron của M2+: 1s22s22p6.
Nguyên tử M nhường 2 electron để tạo thành cation M2+:
M → M2+ + 2e.
Cấu hình electron của nguyên tử M: 1s22s22p63s2 (Z = 12).
M là Mg, có hóa trị II.
Oxide cao nhất của M là: MO.
Theo viện thiên văn học ETH, ![]() và
và ![]() là một trong những chất khí tạo nên Mặt Trời. Phát biểu nào sau đây là đúng?
là một trong những chất khí tạo nên Mặt Trời. Phát biểu nào sau đây là đúng?
Ta thấy và
có cùng số proton và khác neutron
2 nguyên tử là đồng vị của nhau.
Oxide của kim loại M (M2O) được ứng dụng rất nhiều trong ngành hóa chất như sản xuất xi măng, sản xuất phân bón, … Trong sản xuất phân bón, chúng ta thường thấy M2O có màu trắng, tan nhiều trong nước và là thành phần không thể thiếu cho mọi loại cây trồng. Tổng số hạt cơ bản trong phân tử X có công thức M2O là 140, trong phân tử X có tổng số hạt mang điện nhiều hơn số hạt không mang điện là 44. Xác định công thức phân tử của M2O.
Trong X có 2 nguyên tử M và 1 nguyên tử O.
Nguyên tử O có pO = 8 và nO = 8
Tổng số hạt cơ bản trong phân tử X có công thức M2O là 140 nên:
4pM + 2nM + 2pO + nO = 140 hay 4pM + 2nM = 116 (1)
Trong phân tử X có tổng số hạt mang điện nhiều hơn số hạt không mang điện là 44 nên:
(4pM + 2pO) – ( 2nM + nO) = 44 hay 4pM – 2nM = 36 (2)
Từ (1) và (2) có pM = 19 và nM = 20.
Vậy M là K (potassium); X là K2O.
Biết 1 mol nguyên tử zinc có khối lượng bằng 65 gam, một nguyên tử zinc có 30 electron. Số hạt electron có trong 6,5 gam zinc là
Trong 6,5 gam zinc có số nguyên tử zinc là:
nguyên tử zinc
Mà 1 nguyên tử zinc có 30 electron.
Vậy tổng số hạt electron trong 6,5 gam zinc là 6,02.1022.30 = 18,06.1023
Nếu phóng to đường kính của hạt nhân lên thành 3 cm thì đường kính của nguyên tử là
Nguyên tử có đường kính gấp khoảng 10000 lần đường kính hạt nhân Nếu phóng to đường kính của hạt nhân lên thành 3 cm thì đường kính của nguyên tử là:
3.10000 = 30000 (cm) = 300 (m)
Chọn câu đúng khi nói về độ âm điện của nguyên tố hóa học:
Độ âm điện là đại lượng đặc trưng cho khả năng hút electron liên kết của một nguyên tử trong phân tử.
Một ion có 8 proton, 8 neutron và 10 electron. Ion này có điện tích là :
Điện tích hạt nhân của ion là: +8
Điện tích lớp vỏ electron của ion là: -10
⇒ Ion có điện tích là: 2-.
Thông tin về 4 đồng vị của nguyên tố Y được ghi nhận theo bảng sau:
| Đồng vị | A1Y1 | A2Y2 | A3Y3 | A4Y4 |
| Tỉ lệ phần trăm số nguyên tử | 4,34 | 83,79 | 9,50 | 2,37 |
| Thông tin về số hạt neutron trong hạt nhân | Ít hơn đồng vị A2Y2 là 2 neutron | - | Nhiều hơn đồng vị A2Y2 là 1 neutron | Nhiều hơn đồng vị A2Y2 là 2 neutron |
Biết đồng vị A2Y2 có tổng số hạt cơ bản là 76, trong đó tỉ lệ giữa số hạt mang điện trong hạt nhân và số hạt không mang điện là 6 : 7. Nguyên tử khối trung bình của Y là
Xét đồng vị A2Y2, ta có hệ:
A2 = 24 + 28 = 52
A1Y1 ít hơn đồng vị A2Y2 là 2 neutron A1 = 24 + 26 = 50
A3Y3 nhiều hơn đồng vị A2Y2 là 1 neutron A3 = 24 + 29 = 53
A4Y4 nhiều hơn đồng vị A2Y2 là 2 neutron A4 = 24 + 30 = 54
Nguyên tử khối trung bình của Y là:
Trong bảng tuần hoàn các nguyên tố, nguyên tố có tính phi kim mạnh nhất là
Trong bảng tuần hoàn các nguyên tố, nguyên tố có tính phi kim mạnh nhất là fluorine.
Ion X2- có 18 electron. Trong ion X2-, số hạt mang điện nhiều hơn số hạt không mang điện là 17. Số khối của hạt nhân nguyên tử X là
Ion X2- có 18 electron X có 16 electron
Z = 16
Ta có: 2Z + 2 – N = 17 hay 2.16 + 2 – N = 17 N = 17
A = Z + N = 16 + 17 = 33
Nguyên tố hóa học ở vị trí nào trong bảng tuần hoàn có các electron hóa trị là 3d54s1?
Nguyên tố có 4 lớp e chu kì 4
Nguyên tố có e cuối cùng được điền vào phân lớp d thuộc nhóm B
Nguyên tố có 6 e lớp ngoài cùng nhóm VIB
Cho biết tổng số electron trong anion AB32- là 42. Trong các hạt nhân A cũng như B có số proton bằng với số neutron. Khi đốt hỗn hợp các đơn chất của A, B thu được một hợp chất C. Xác định công thức hóa học của hợp chất C.
Tổng số electron trong anion AB32- là 42 eA + 3.eB + 2 = 42
pA + 3.pB = 40
Trong hạt nhân A cũng như B có số proton bằng số neutron nA = pA; nB = pB
pA = 16 (S) và pB = 8 (O) vì hạt nhân S và O có số p = số n
Hợp chất C là SO2.
Magnesium có 3 đồng vị 24Mg, 25Mg và 26Mg. Chlorine có 2 đồng vị 35Cl và 37Cl. Có bao nhiêu loại phân tử MgCl2 khác tạo nên từ các đồng vị của 2 nguyên tố đó
Ứng với mỗi đồng vị của Mg có 3 loại phân tử MgCl2 khác nhau, tương ứng với 2 nguyên tử Cl lần lượt là (35,35), (37,37), (35,37).
Có tất cả 3.3 = 9 loại phân tử MgCl2 khác nhau
Đâu không phải thông tin về nguyên tố hóa học mà một ô nguyên tố biểu diễn?
Một ô nguyên tố biểu diễn số hiệu nguyên tử, cấu hình electron và kí hiệu nguyên tố.
Trong một chu kì các nguyên tố nhóm A theo chiều tăng dần điện tích hạt nhân, tính chất nào sau đây giảm dần?
Trong một chu kì các nguyên tố nhóm A theo chiều tăng dần điện tích hạt nhân, tính kim loại và tính base giảm dần.
Cho số proton của các nguyên tử sau: pX = 15; pY = 16; pT = 15; pR = 24; pI = 15; pL= 24. Những nguyên tử nào thuộc cùng nguyên tố hóa học?
Nguyên tố hóa học là những nguyên tử có cùng điện tích hạt nhân (cùng số proton, số electron).
Những nguyên tử thuộc cùng nguyên tố hóa học là X, T, I do có cùng p = 15.
Những vấn đề về khí thải động cơ ô tô, xe máy cần được xử lí để đạt tiêu chuẩn cho phép thuộc vai trò của hóa học về
Những vấn đề về khí thải động cơ ô tô, xe máy cần được xử lí để đạt tiêu chuẩn cho phép thuộc vai trò của hóa học về môi trường.
Cho các nguyên tố có cấu hình electron như sau:
(A) 1s22s22p63s2.
(B) 1s22s22p63s23p64s1.
(C) 1s22s22p63s23p64s2.
(D) 1s22s22p63s23p5.
(E) 1s22s22p63s23p63d64s2.
(F) 1s22s22p63s23p1.
Các nguyên tố thuộc cùng chu kì nhỏ là:
Các nguyên tố thuộc cùng 1 chu kì có số lớp electron bằng nhau.
Từ cấu hình electron của các nguyên tố ta có: A, D, F thuộc chu kì 3 còn B, C, E thuộc chu kì 4.
Chu kì nhỏ là chu kì 1, 2 và 3
A, D, F thuộc chu kì nhỏ.
Cặp nguyên tố hóa học nào sau đây có tính chất hóa học giống nhau nhất?
- Ca và Mg là hai nguyên tố hóa học cùng thuộc nhóm IIA nên có tính chất hóa học tương tự nhau.
- Các cặp còn lại gồm các nguyên tố thuộc hai nhóm khác nhau nên tính chất hóa học khác nhau.
Hạt X và Y có cấu tạo như sau:
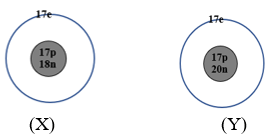
Phát biểu nào sau đây về X và Y là đúng?
X và Y có cùng số Z = 17p X và Y thuộc cùng một nguyên tố hóa học.
Số hiệu nguyên tử Z của nguyên tố X, A, M, Q lần lượt là 6, 7, 20, 19. Nhận định nào sau đây là đúng?
Cấu hình electron của:
X: 1s22s22p2
A: 1s22s22p3
M: 1s22s22p63s23p64s2
Q: 1s22s22p63s23p64s1
Vậy:
X thuộc nhóm IVA do có 2 electron hóa trị.
Y thuộc nhóm VA do có 5 electron hóa trị.
Z thuộc nhóm IIA do có 2 electron hóa trị.
Q thuộc nhóm IA do có 1 electron hóa trị.
Khẳng định nào sau đây là sai?
Kí hiệu 2p5 cho biết
- Chỉ số phía trên bên phải kí hiệu phân lớp biểu diễn số electron trong phân lớp. Nên kí hiệu 2p5 cho biết phân lớp 2p có 5 electron.
- Phân lớp 2p ở lớp thứ 2 có tên là lớp L.
- Phân lớp 2p có 5 electron phân bố vào 3 AO, mỗi AO chứa tối đa 2 electron nên sẽ có 1 AO chỉ có 1 electron, electron đó gọi là electron độc thân. Do đó phân lớp này có 1 electron độc thân.
- Phân lớp này chưa chứa đủ số electron tối đa (6 electron) nên chưa bão hòa.
Cấu hình electron nguyên tử của một nguyên tố là 1s22s22p5. Số electron độc thân của nguyên tố là
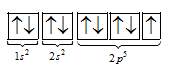
Từ cấu hình suy ra nguyên tố có 1 electron độc thân.
Các hình vẽ nào sau đây vi phạm nguyên lý Pauli khi điền electron vào orbital (AO)?
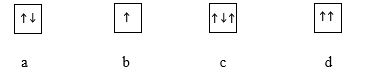
Trong mỗi một ô orbital chứa tối đa 2 electron, electron đầu tiên được biểu diễn bằng mũi tên quay lên, electron thứ hai được biểu diễn bằng mũi tên quay xuống.
Phát biểu nào sau đây là đúng?
- Bảng tuần hoàn các nguyên tố hóa học hiện nay hồm 118 nguyên tố hóa học.
- Bảng tuần hoàn gồm 7 chu kì, được đánh số từ 1 đến 7.
- Bảng tuần hoàn gồm 18 cột, được chia thành 8 nhóm A, đánh số từ IA đến VIIIA; 8 nhóm B, được đánh số từ IB đến VIIIB.
- Các nguyên tố trong bảng tuần hoàn được xếp theo chiều tăng dần điện tích hạt nhân.
Kí hiệu 1s2 cho biết
Kí hiệu 1s2 cho biết phân lớp 1s có 2 electron.
Nguyên tử R có điện tích ở lớp vỏ là -41,6.10-19 culong. Điều khẳng định nào sau đây là không chính xác?
Điện tích của 1 electron bằng -1,6.10-19 culong.
Số electron trong lớp vỏ của nguyên tử R là: (-41,6.10-19) : (-1,6.10-19) = 26
Số hạt electron bằng số hạt proton hạt nhân của R có 26 proton.
Trong nguyên tử R thì số hạt electron bằng số hạt proton. Do đó trong nguyên tử R thì tổng điện tích âm bằng tổng điện tích dương. Do đó nguyên tử R trung hòa về điện.
Nguyên tố X có số hiệu nguyên tử bằng 15. Hydroxide cao nhất của nó có tính chất gì?
Cấu hình electron nguyên tử X: 1s22s22p63s23p3.
X thuộc nhóm VA, công thức hydroxide có dạng: H3XO4, có tính acid
Trong ion âm X- có tổng số hạt là 29 và số hạt mang điện chiếm 65,52% tổng số hạt. Số hạt mang điện trong X là
Gọi số hạt trong X lần lượt là p, n, e.
Ion âm X- có tổng số hạt là 29:
p + n + (e + 1) = 29
2p + n = 28 (1)
Trong ion âm X- hạt mang điện chiếm 65,52% tổng số hạt trong ion âm
Từ (1) và (2): p = 9, n = 10 Số hạt mang điện trong X là 18.
Nhóm A bao gồm các nguyên tố:
Nhóm A bao gồm các nguyên tố s và nguyên tố p.
Các đám mây gây hiện tượng sấm sét tạo bởi những hạt nước nhỏ li ti mang điện tích. Một phép đo thực nghiệm cho thấy một giọt nước có đường kính 50 μm, mang một lượng điện tích âm là -3,204×10-17 C. Điện tích âm của giọt nước trên tương đương với điện tích của bao nhiêu electron?
Điện tích của 1 hạt electron là -1e0 = -1,602 × 10-19C
Điện tích âm của giọt nước trên tương đương với điện tích của số electron là:
Phát biểu nào dưới đây là đúng?
Theo trình tự sắp xếp, lớp K (n = 1) là lớp gần hạt nhân nhất. Năng lượng của electron phụ thuộc vào khoảng cách từ electron đó tới hạt nhân nguyên tử. Electron càng xa hạt nhân thì năng lượng càng cao.
Oxide cao nhất của một nguyên tố R thuộc nhóm A có dạng RO3. Cho các phát biểu sau:
(1) R có hóa trị cao nhất với oxygen là 6.
(2) Công thức hợp chất khí của R với H có dạng RH2.
(3) R là một phi kim.
(4) Acid tương ứng với oxide cao nhất của R là H2RO3.
Số phát biểu đúng là
- Oxide cao nhất của một nguyên tố R thuộc nhóm A có dạng RO3 Hóa trị cao nhất của R với oxygen là 6.
- R thuộc nhóm VIA nên có công thức electron lớp ngoài cùng là ns2np4 R là một phi kim.
- Hóa trị với hydrogen là: 8 – 6 = 2 Công thức hợp chất khí với hydrogen hóa là RH2
- Acid tương ứng của RO3 là H2RO4.
Các nhận định đúng là (1), (2), (3).
Cho phổ khối của nguyên tố X được biểu diễn tại hình 1.2. Nguyên tử khối trung bình của X là
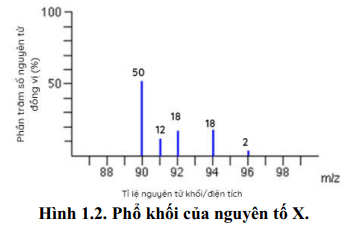
Nguyên tử khối trung bình của X là
Anion X2- có tổng số hạt cơ bản là 50, trong nguyên tử X thì số hạt mang điện nhiều hơn số hạt không mang điện là 16. Cấu hình electron của X2− là:
Gọi số p, n, e trong nguyên tử lần lượt là Z, N, E (nguyên dương)
Anion có tổng số hạt cơ bản là 50:
Z + E + P + 2e = 2Z + N + 2 = 50
2Z + N = 48
Trong nguyên tử X thì số hạt mang điện nhiều hơn số hạt không mang điện là 16:
2Z - N = 16
Từ đó ta có:
Cấu hình electron của X là: [Ne]3s23p4
Vậy cấu hình electron của S2− là [Ne]3s23p4
Các electron chuyển động xung quanh hạt nhân nguyên tử theo những quỹ đạo tròn hay bầu dục, giống như quỹ đạo của các hành tinh quay xung quanh Mặt Trời là cách nói theo
Các electron chuyển động xung quanh hạt nhân nguyên tử theo những quỹ đạo tròn hay bầu dục, giống như quỹ đạo của các hành tinh quay xung quanh Mặt Trời là cách nói theo mô hình nguyên tử của Rutherford – Bohr.
