Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học
Bài học: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học đã giới thiệu đến các em ý nghĩa về dấu, giá trị và cách tính biến thiên enthalpy. Bên cạnh là các ví dụ và bài tập có lời giải chi tiết, xây dựng dựa trên kiến thức trọng tâm chương trình hóa 10 Cánh diều.
I. Ý nghĩa về dấu và giá trị của biến thiên enthalpy phản ứng
Với các phản ứng có kèm theo sự trao đổi năng lượng dưới dạng nhiệt, có hai khả năng sau đây:
- Phản ứng tỏa nhiệt: biến thiên enthalpy của phản ứng có giá trị âm. Biến thiên enthalpy càng âm, phản ứng tỏa ra càng nhiều nhiệt.
- Phản ứng thu nhiệt: biến thiên enthalpy của phản ứng có giá trị dương. Biến thiên enthalpy càng dương, phản ứng thu vào càng nhiều nhiệt.
Với phản ứng tỏa nhiệt, năng lượng của hệ chất phản ứng cao hơn năng lượng của hệ sản phẩm, do vậy phản ứng diễn ra kèm theo sự giải phóng năng lượng dưới dạng nhiệt.
Với phản ứng thu nhiệt, năng lượng của hệ chất phản ứng thấp hơn năng lượng của hệ sản phẩm, do vậy phản ứng diễn ra kèm theo sự hấp thu năng lượng dưới dạng nhiệt.
Ví dụ: Cho phản ứng đốt cháy methane và acetylene:
CH4(g) + 2O2(g) ![]() CO2(g) + 2H2O(l)
CO2(g) + 2H2O(l) ![]()
C2H2(g) + 2,5O2(g) ![]() 2CO2(g) + H2O(l)
2CO2(g) + H2O(l) ![]()
Với chất khí trong cùng điều kiện nhiệt độ và áp suất, tỉ lệ về số mol bằng tỉ lệ thể tích nên khi đốt cháy cùng một thể tích CH4 và C2H2, lượng nhiệt do C2H2 sinh ra nhiều gấp khoảng 1,5 lần lượng nhiệt do CH4 sinh ra. Thực tế, người ta sử dụng C2H2 trong đèn xì để hàn, cắt kim loại mà không dùng CH4.

- Đối với phản ứng tỏa nhiệt, một số phản ứng cần phải khơi mào. Sau đó, phản ứng tỏa nhiệt có thể tự tiếp diễn mà không cần tiếp tục đun nóng. Một số phản ứng không cần khơi mào
Ví dụ: phản ứng không cần khơi mào như phản ứng tạo gỉ sắt, gỉ đồng, phản ứng trung hòa acid - base,...)
- Trái lại, phần lớn các phản ứng thu nhiệt diễn ra đều cẩn phải cung cấp năng lượng từ nguồn bên ngoài.
Ví dụ: phản ứng nung vôi cần nhiệt từ quá trình đốt cháy than, nếu dừng cung cấp nhiệt thì phản ứng nung vôi sẽ không tiếp diễn.
| Phản ứng thu nhiệt | Phản ứng tỏa nhiệt | |
| Giai đoạn khơi mào | Hầu hết các phản ứng cần thiết khơi mào (đun hoặc đốt nóng, …). | Có thể có hoặc không cần khơi mào, tùy phản ứng cụ thể. |
| Giai đoạn tiếp diễn | Hầu hết các phản ứng cần phải tiếp tục đun hoặc đốt nóng. | Hầu hết các phản ứng không cần tiếp tục đun hoặc đốt nóng. |
Các phản ứng tỏa nhiệt (![]() < 0) thường diễn ra thuận lợi hơn các phản ứng thu nhiệt (
< 0) thường diễn ra thuận lợi hơn các phản ứng thu nhiệt (![]() >0).
>0).
Ví dụ: Sau khi được đốt nóng, Na tự cháy trong chlorine cho đến hết do phản ứng này có ![]() rất âm.
rất âm.
Na(s) + 1/2Cl2(g) ![]() NaCl(s)
NaCl(s) ![]()
Phản ứng này diễn ra thuận lợi hơn rất nhiều so với phản ứng giữa N2 và O2. Ở điều kiện chuẩn, phản ứng chỉ xảy ra khi được đốt nóng đến khoảng 3000oC (cung cấp nhiệt), khi dừng đốt nóng phản ứng sẽ dừng lại.
N2(s) + 1/2O2(g) ![]() NO(g)
NO(g) ![]()
II. Cách tính biến thiên enthalpy phản ứng
1. Tính biến thiên enthalpy phản ứng theo enthalpy tạo thành
Cho phản ứng tổng quát:
aA + bB ![]() mM + nN
mM + nN
Biến thiên enthalpy chuẩn của phản ứng này được tính theo công thức:
![]() = m
= m![]()
![]() (M) + n
(M) + n![]()
![]() (N) - a.
(N) - a.![]() (A) - b.
(A) - b.![]() (B)
(B)
Ví dụ: Xét quá trình đốt cháy khí propane C3H8(g):
C3H8(g) + 5O2(g) ![]() 3CO2(g) + 4H2O(g)
3CO2(g) + 4H2O(g)
Tính ![]() của phản ứng dựa vào nhiệt tạo thành của hợp chất, biết:
của phản ứng dựa vào nhiệt tạo thành của hợp chất, biết: ![]() (C3H8(g)) = -105,00 kJ/mol;
(C3H8(g)) = -105,00 kJ/mol; ![]() (CO2(g)) = -393,50 kJ/mol;
(CO2(g)) = -393,50 kJ/mol; ![]() (H2O(g)) = -241,82 kJ/mol.
(H2O(g)) = -241,82 kJ/mol.
Hướng dẫn giải:
![]() = 3
= 3![]()
![]() CO2(g) + 4
CO2(g) + 4![]()
![]() H2O(g) - 1
H2O(g) - 1![]()
![]() C3H8(g) - 5
C3H8(g) - 5![]()
![]() O2(g)
O2(g)
= 3![]() (-393,50) + 4
(-393,50) + 4![]() (-241,82) - 1
(-241,82) - 1![]() (-105,00) - 5.0
(-105,00) - 5.0
= -2042,78 kJ/mol.
2. Tính biến thiên enthalpy phản ứng theo năng lượng liên kết
Khi các chất trong phản ứng ở thể khí, biến thiên enthalpy phản ứng cũng có thể tính được nếu biết giá trị năng lượng liên kết của tất cả các chất trong phản ứng.
Cho phản ứng tổng quát:
aA(g) + bB(g) → mM(g) + nN(g)
![]() = a×Eb(A) + b×Eb(B) - m×Eb(M) - n×Eb(N)
= a×Eb(A) + b×Eb(B) - m×Eb(M) - n×Eb(N)
Trong đó: Eb(A), Eb(B), Eb(M), Eb(N) lần lượt là tổng năng lượng liên kết của tất cả các liên kết trong các phân tử A, B, M, N.
Ví dụ: Tính ![]() của phản ứng:
của phản ứng:
N2H4(g) → N2(g) + 2H2(g)
Biết: E(N-H) = 391 kJ/mol; E(N![]() N) = 945 kJ/mol; E(H-H) = 432 kJ/mol; E(N - N) = 160 kJ/mol.
N) = 945 kJ/mol; E(H-H) = 432 kJ/mol; E(N - N) = 160 kJ/mol.
Hướng dẫn giải:
Công thức cấu tạo N2H4:
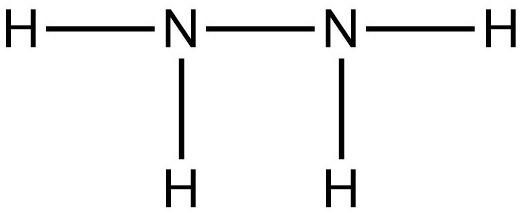
Hướng dẫn giải:
![]() = 1×Eb(N2H4) - 1×Eb(N2) - 1×(H2)
= 1×Eb(N2H4) - 1×Eb(N2) - 1×(H2)
![]()
![]() = 4×E(N-H) + 1×E(N - N) - 1×E(N
= 4×E(N-H) + 1×E(N - N) - 1×E(N![]() N) - 2×E(H-H)
N) - 2×E(H-H)
![]()
![]() = 4×391 + 1×160 - 1×945 - 2×432
= 4×391 + 1×160 - 1×945 - 2×432
![]()
![]() = -85 kJ/mol
= -85 kJ/mol
Phản ứng có ![]() âm nên phản ứng tỏa nhiệt và diễn ra thuận lợi. Trong thực tế, chỉ cần được chiếu ánh sáng mặt trời là phản ứng đã diễn ra.
âm nên phản ứng tỏa nhiệt và diễn ra thuận lợi. Trong thực tế, chỉ cần được chiếu ánh sáng mặt trời là phản ứng đã diễn ra.







