Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết khi các chất ở trạng thái nào?
Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết khi các chất đều ở thể khí.
Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết khi các chất ở trạng thái nào?
Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết khi các chất đều ở thể khí.
Phản ứng nào sau đây là phản ứng tỏa nhiệt?
Oxi hóa glucose thành CO2 và H2O, tương tự phản ứng đốt cháy glucose là phản ứng tỏa nhiệt.
Biên thiên enthalpy của phản ứng nào sau đây có giá trị âm:
Phản ứng tỏa nhiệt biến thiên enthalpy có giá trị âm.
Phản ứng thu nhiệt biến thiên enthalpy có giá trị dương.
Trong các quá trình sau, quá trình nào là quá trình thu nhiệt
Phản ứng nung đá vôi là quá trình thu nhiệt vì
CaCO3 (s) → CaO (s) + CO2 (g) . Nên đây là phản ứng thu nhiệt
Tính ![]() của phản ứng đốt cháy 1 mol C2H2(g) biết các sản phẩm thu được đều ở thể khí.
của phản ứng đốt cháy 1 mol C2H2(g) biết các sản phẩm thu được đều ở thể khí.
Cho enthalpy tạo thành chuẩn của các chất tương ứng là
| Chất | C2H2(g) | CO2(g) | H2O(g) |
| +227 | -393,5 | -241,82 |
C2H2(g) + O2(g) ⟶ 2CO2(g) + H2O(g)
= 2.
(CO2(g)) +
(H2O(g)) −
(O2(g)) −
(C2H2(g))
= 2×(−393,5) + (−241,82) − 52×0 − 227
= − 1255,82 (kJ)
Giá trị tuyệt đối của biến thiên enthalpy càng lớn thì
Giá trị tuyệt đối của biến thiên enthalpy càng lớn thì nhiệt lượng tỏa ra hay thu vào của phản ứng càng nhiều.
Phát biểu nào sau đây sai về biến thiên enthalpy của 1 phản ứng:
Biến thiên enthalpy của phản ứng
Chất tham gia ở dạng đơn chất hay hợp chất đều được.
Sản phẩm có thể là 1 hay nhiều chất.
Thạch cao nung (CaSO4.0,5H2O) là hóa chất được sử dụng để đúc tượng, bó bột trong y học. Có thể thu được thạch cao nung bằng cach nung thạch cao sống (CaSO4.2H2O) ở nhiệt độ khoảng 150oC. Phương trình nhiệt hóa học xảy ra như sau:
CaSO4.2H2O(s) ![]() CaSO4.0,5H2O(s) +
CaSO4.0,5H2O(s) + ![]() H2O(g)
H2O(g)
Cho giá trị nhiệt tạo thành chuẩn của các chất (![]() ) trong bảng dưới đây:
) trong bảng dưới đây:
| Chất | CaSO4.2H2O | CaSO4.0,5H2O | H2O |
| -2021 | -1575 | -241,82 |
Nhiệt lượng cần cung cấp để chuyển 20 kg thạch cao sống thành thạch cao nung ở điều kiện chuẩn là
Biến thiên enthanpy chuẩn của phản ứng nung thạch cao sống là:
=
.
(H2O(g)) +
(CaSO4.0,5H2O(s)) -
(CaSO4.2H2O(s))
=
.(−241,82) − 1575 − (−2021) = +83,27kJ
Để chuyển 1 mol thạch cao sống thành thạch cao nung cần cung cấp nhiệt là 83,27 kJ
Theo bài ra ta có:
Lượng nhiệt cần cung cấp để chuyển 20 kg thạch cao sống tức
mol thạch cao sống thành thạch cao nung là:
Cho các phản ứng dưới đây:
(1) CO (g) + O2 (g) → CO2 ![]()
(2) C (s) + H2O (g) → CO (g) + H2 (g) ![]()
(3) H2 (g) + F2 (g) → 2HF ![]()
(4) H2 (g) + Cl2 (g) → 2HCl ![]()
Phản ứng xảy ra thuận lợi nhất là
Phản ứng có thường xảy ra thuận lợi hơn
Vậy phản ứng H2 (g) + F2 (g) → 2HF có
nhỏ nhất nên xảy ra thuận lợi nhất.
Số lượng mỗi loại liên kết trong phân tử CH3Cl là
Công thức cấu tạo của CH3Cl là:
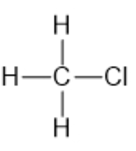 Vậy trong 1 phân tử CH3Cl có 3 liên kết C – H, 1 liên kết C – Cl.
Vậy trong 1 phân tử CH3Cl có 3 liên kết C – H, 1 liên kết C – Cl.
Để tính biến thiên enthalpy phản ứng theo năng lượng liên kết, phải viết được
Để tính biến thiên enthalpy phản ứng theo năng lượng liên kết, phải viết được công thức cấu tạo của tất cả các chất trong phản ứng để xác định số lượng và loại liên kết.
Tính năng lượng liên kết trung bình của các liên kết O-H trong phân tử nước, biết rằng năng lượng liên kết H-H và O=O tương ứng là 435,9 và 498,7 kJ/mol, khi đốt cháy 2 mol H2 tỏa ra 483,68 kJ/mol.
2H2(g) + O2(g) → 2H2O(g) = -483,68 kJ/mol
= 2.Eb(H2) + Eb(O2) - 2.Eb(H2O)
= 2.E(H-H) + E(O=O) – 2.2.E(O-H)
-483,68 = 2.435,9 + 498,7 – 4.E(O-H)
E(O-H) = -463,545 kJ/mol
Đơn vị của nhiệt tạo thành chuẩn là
Rót 100 ml dung dịch HCl 0,5M ở 25oC vào 100 ml dung dịch NaHCO3 0,5M ở 26oC. Biết nhiệt dung của dung dịch loãng bằng nhiệt dung của nước là 4,2 J/g.K và nhiệt tạo thành của các chất được cho trong bảng sau:
| Chất | HCl(aq) | NaHCO3(aq) | NaCl(aq) | H2O(l) | CO2(g) |
| -168 | -932 | -407 | -286 | -392 |
Sau phản ứng, dung dịch thu được có nhiệt độ là
Phương trình phản ứng xảy ra:
HCl(aq) + NaHCO3(aq) → NaCl(aq) + H2O(l) + CO2(g)
Biến thiên enthalpy của phản ứng là:
ΔrH = ΔfH(NaCl) + ΔfH(H2O) + ΔfH(CO2) − ΔfH(HCl) − ΔfH(NaHCO3)
= −407 − 286 − 392 + 168 + 932
= 15kJ
Phản ứng thu nhiệt
Ta có: nHCl = nNaHCO3 = 0,1.0,5 = 0,05 mol
Nhiệt lượng thu vào khi cho 0,05 mol HCl tác dụng với 0,05 mol NaHCO3 là:
Q = 0,05.15 = 0,75 kJ
Mà:
Do phản ứng thu nhiệt nên nhiệt độ giảm đi là 0,89oC
Nhiệt độ cuối cùng là 26 – 0,89 = 25,1oC
Phát biểu nào sau đây đúng về enthalpy tạo thành của một chất?
Enthalpy tạo thành của một chất
Chất tham gia phải là đơn chất bền nhất
Sản phẩm chỉ có 1 chất duy nhất.
Nhiệt tạo thành (ΔfH) của một chất là biến thiên enthalpy của phản ứng tạo thành
Nhiệt tạo thành (ΔfH) của một chất là biến thiên enthalpy của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền vững nhất, ở một điều kiện xác định.
Cho phản ứng:
![]()
![]()
Nếu chỉ thu được 0,5 mol NaCl (s) ở điều kiện chuẩn thì lượng nhiệt tỏa ra là
Enthalpy tạo thành chuẩn của một chất () là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn.
Phản ứng có (NaCl, s) = − 411,1 kJ/mol.
Nếu tạo thành 1 mol NaCl(s) thì lượng nhiệt tỏa ra là 411,1 kJ.
Nếu tạo thành 0,5 mol NaCl(s) thì lượng nhiệt tỏa ra là:
411,1.0,5 = 205,55 (kJ)
Cho các phản ứng dưới đây:
(1) Điều kiện chuẩn là điều kiện ứng với 1 bar (đối với chất lỏng).
(2) Độ biến thiên enthalpy của một quá trình không thay đổi theo nhiệt độ.
(3) Tính chất của enthalpy phụ thuộc vào bản chất của hệ.
(4) Ý nghĩa của enthapy là xác định hiệu ứng nhiệt trong quá trình đẳng áp, đẳng nhiệt.
Điều kiện chuẩn là điều kiện ứng với 1 bar (đối với chất khí)
Độ biến thiên enthalpy chỉ phụ thuộc vào trạng thái đầu và trạng thái cuối của hệ mà không phụ thuộc vào trạng thái trung gian.
Tính chất enthapy: thuộc tính khuếch độ của hệ phụ thuộc khối lượng của hệ, hàm trạng thái.
Sắp xếp các ý sau vào loại phản ứng phù hợp (thu nhiệt, tỏa nhiệt)
(1) Tăng Enthalpy
(2) Giảm Enthalpy
(3) Giải phóng nhiệt ra môi trường
(4) Hấp thu nhiệt môi trường
(5) Có thể xảy ra tự phát
(6) Cần cung cấp năng lượng để xảy ra.
Phản ứng thu nhiệt b, d, f.
Phản ứng tỏa nhiệt a, c, e.
Cho các phát biểu sau:
(1) Hầu hết các phản ứng thu nhiệt và tỏa nhiệt đều cần thiết khơi mào (đun hoặc đốt nóng …)
(2) Khi đốt cháy tờ giấy hay đốt lò than, ta cần thực hiện giai đoạn khơi mào như đun hoặc đốt nóng.
(3) Một số phản ứng thu nhiệt diễn ra bằng cách lấy nhiệt từ môi trường bên ngoài, nên làm cho nhiệt độ của môi trường xung quanh giảm đi.
(4) Sau giai đoạn khơi mào, phản ứng tỏa nhiệt cần phải tiếp tục đun hoặc đốt nóng.
Trong các phát biểu trên, số phát biểu đúng là:
Phát biểu đúng (2); (3); (4)
(1) Không đúng vì
Hầu hết các phản ứng thu nhiệt cần thiết khơi mào (Đun hoặc đốt nóng …)
Phản ứng tỏa nhiệt có thể có, có thể không cần khơi mào, tùy phản ứng cụ thể.
Cho phản ứng có dạng: aA + bB ⟶ mM + nN
Công thức tính biến thiên enthalpy phản ứng theo enthalpy tạo thành là
Cho 2 phương trình nhiệt hóa học sau:
C(s) + H2O(g) ![]() CO(g) + H2(g)
CO(g) + H2(g) ![]() = + 131,25 kJ (1)
= + 131,25 kJ (1)
CuSO4(aq) + Zn(s) ![]() ZnSO4(aq) + Cu(s)
ZnSO4(aq) + Cu(s) ![]() = −231,04 kJ (2)
= −231,04 kJ (2)
Khẳng định đúng là
Phản ứng (1) có = + 131,25 kJ > 0
Phản ứng thu nhiệt
Phản ứng (1) có = −231,04 kJ < 0
Phản ứng tỏa nhiệt
Kí hiệu của nhiệt tạo thành chuẩn là
Nhiệt tạo thành ⧍fH của một chất là biến thiên enthalpy của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền vững nhất, ở một điều kiện xác định.
Nhiệt tạo thành chuẩn () là nhiệt tạo thành ở điều kiện chuẩn.
Nhiệt tạo thành chuẩn của các đơn chất ở dạng bền vững nhất bằng
Nhiệt tạo thành chuẩn của các đơn chất ở dạng bền vững nhất bằng không.
Cho phản ứng: Na(s) + 1/2Cl2(g) ⟶ NaCl(s) có ![]() (NaCl, s) = −411,1 kJ/mol. Nếu chỉ thu được 0,5 mol NaCl (s) ở điều kiện chuẩn thì lượng nhiệt tỏa ra là
(NaCl, s) = −411,1 kJ/mol. Nếu chỉ thu được 0,5 mol NaCl (s) ở điều kiện chuẩn thì lượng nhiệt tỏa ra là
Enthalpy tạo thành chuẩn của một chất () là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn.
Na(s) + ½ Cl2(g) ⟶ NaCl (s) có (NaCl, s) = − 411,1 kJ/mol
Nếu tạo thành 1 mol NaCl(s) thì lượng nhiệt tỏa ra là 411,1 kJ
Vậy nếu tạo thành 0,5 mol NaCl(s) thì lượng nhiệt tỏa ra là 411,1.0,5 = 205,55 (kJ)
Phản ứng nào sau đây là phản ứng thu nhiệt?
Các phản ứng: tôi vôi, đốt than củi, đốt nhiên liệu đều giải phóng năng lượng dưới dạng nhiệt ra môi trường ⇒ Là phản ứng tỏa nhiệt.
Phản ứng phân hủy đá vôi cần cung cấp nhiệt để phản ứng xảy ra, ngừng cung cấp nhiệt phản ứng sẽ dừng lại ⇒ Là phản ứng thu nhiệt.
Cho ![]() . Biết 1 J = 0,239 cal. Enthalpy tạo thành chuẩn theo đơn vị kcal/mol của Fe2O3(s) là
. Biết 1 J = 0,239 cal. Enthalpy tạo thành chuẩn theo đơn vị kcal/mol của Fe2O3(s) là
1 J = 0,239 cal 1 kJ = 0,239 kcal
-825,5 kJ/mol = -197,3 kcal/mol
Khẳng định sai là
Biến thiên enthalpy càng dương thì phản ứng thu nhiệt càng nhiều.
Biến thiên enthalpy càng âm thì phản ứng tỏa nhiệt càng nhiều.
Điều kiện chuẩn của biến thiên enthalpy là
Điều kiện chuẩn của biến thiên enthalpy: áp suất 1 bar (đối với chất khí), nồng độ 1 mol/L (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 25oC (298K).
Cho các phản ứng dưới đây:
(1) CO(g) + 1/2 O2(g) ⟶ CO2(g) ![]() = − 283 kJ
= − 283 kJ
(2) C(s) + H2O(g) ![]() CO(g) + H2(g)
CO(g) + H2(g) ![]() = + 131,25 kJ
= + 131,25 kJ
(3) H2(g) + F2(g) ⟶ 2HF(g) ![]() = − 546 kJ
= − 546 kJ
(4) H2(g) + Cl2(g)⟶ 2HCl(g) ![]() = − 184,62 kJ
= − 184,62 kJ
Phản ứng xảy ra thuận lợi nhất là
Phản ứng có < 0 thường xảy ra thuận lợi hơn.
Mà phản ứng (3) có nhỏ nhất nên xảy ra thuận lợi nhất.
Phản ứng nào dưới đây là phản ứng thu nhiệt là
Nung NH4Cl tạo ra HCl và NH3 là phản ứng thu nhiệt
Phản ứng nhiệt phân hoàn toàn 1 mol Cu(OH)2, tạo thành 1 mol CuO và 1 mol H2O, thu vào nhiệt lượng 9,0 kJ. Phương trình nhiệt hóa học nào sau đây biểu diễn đúng?
Ta có phản ứng thu nhiệt nên ∆rHo298 > 0 và là phản ứng nhiệt phân Phương trình nhiệt hóa học đúng là:
Cu(OH)2(s) CuO(s) + H2O(l) ∆rHo298 = +9,0kJ.
Đâu là phản ứng toả nhiệt dưới đây?
Nước đóng băng, cần tỏa nhiệt ra môi trường, để giảm nhiệt độ và chuyển sang thể rắn.
Một mẫu cồn X (thành phần chính là C2H5OH) có lẫn methanol (CH3OH). Đốt cháy 6,2 g cồn X tỏa ra nhiệt lượng 172,8 kJ. Cho phương trình nhiệt hóa học của các phản ứng sau:
![]()
![]()
Thành phần tạp chất methanol trong X là
Gọi số mol của CH3OH và C2H5OH trong X lần lượt là a và b
Theo bài ta có hệ hai phương trình:
mCH3OH = 0,05.32 = 1,6 g
Phần trăm methanol trong X là:
Tính biến thiên enthalpy chuẩn của phản ứng:
C4H10(g) → C2H4(g) + C2H6(g)
Biết Eb(H-H) = 436 kJ/mol, Eb(C-H) = 418 kJ/mol, Eb(C-C) = 346 kJ/mol, Eb(C=C) = 612 kJ/mol.
= 3Eb(C−C) + 10Eb(C−H) − Eb(C=C) − 4Eb(C−H) − Eb(C−C) − 6Eb(C−H)
= 3.346 + 10.418 − 612 – 4.418 – 346 – 6.418
= 80 kJ
Biết rằng ở điều kiện chuẩn, 1 mol enthanol cháy tỏa ra một nhiệt lượng là 1,37.103 kJ. Nếu đốt cháy hoàn toàn 15,1 gam ethanol, năng được được giải phóng ra dưới dạng nhiệt bởi phản ứng là
Nếu đốt cháy hoàn toàn 15,1 gam ethanol, năng được được giải phóng ra dưới dạng nhiệt bởi phản ứng là
Tính biến thiên enthalpy chuẩn của phản ứng:
C3H6(g) + H2(g) → C3H8(g)
Biết Eb (H-H) = 436 kJ/mol, Eb (C-H) = 418 kJ/mol, Eb (C-C) = 346 kJ/mol, Eb (C=C) = 612 kJ/mol.
H2C=CH-CH3 + H-H H3C-CH2-CH2-CH3
= Eb(C=C) + 6Eb(C−H) + Eb(C−C) + Eb(H−H) − 2.Eb(C−C) − 8Eb(C−H)
= 612 + 6.418 + 346 + 436 − 2.346 − 8.418 = − 134 (kJ)
Phản ứng thu nhiệt là gì?
Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt
Phát biểu nào sau đây đúng?
Với phản ứng thu nhiệt năng lượng của hệ chất tham gia trong phản ứng thu nhiệt thấp hơn năng lượng của hệ sản phẩm
Cho hai phương trình nhiệt hóa học sau
C (s) + H2O (g) → CO (g) + H2 (g) ![]() (1)
(1)
CuSO4 (aq) + Zn (s) → ZnSO4 (aq) + Cu (s) ![]() (2)
(2)
Chọn phát biểu đúng
Phản ứng (1) là phản ứng thu nhiêt, phản ứng (2) là phản ứng tỏa nhiệt
