Liên kết ion
I. Khái niệm và sự hình thành liên kết ion
1. Khái niệm
Liên kết ion được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
Khi hình thành liên kết ion, năng lượng của hệ giảm đi tạo nên hệ bền vững hơn
Ví dụ 1: Liên kết ion trong hợp chất NaCl tạo bởi lực hút tính điện giữa cation Na+ và anion Cl-.
Na+ + Cl- → NaCl
Liên kết ion cũng có thể được hình thành từ ion đa nguyên tử.
Ví dụ 2:
K+ + NO3- → KNO3
NH4+ + NO3- → NH4NO3
Mg2+ + CO32- → MgCO3
Các hợp chất được tạo nên từ cation (ion mang điện tích dương) và anion (ion mang điện tích âm) gọi là hợp chất ion.
Lưu ý: Theo quy ước, điện tích của ion được viết số trước, dấu (+ hoặc -) sau để tránh nhầm lẫn với số oxi hóa.
Ví dụ: NO3−, PO43−, CO32−
2. Sự hình thành liên kết ion từ phản ứng giữa các nguyên tử
Quá trình hình thành liên kết ion diễn ra như sau:
- Các ion trái dấu hình thành từ các quá trình nguyên tử kim loại nhường electron và nguyên tử phi kim nhận electron theo quy tắc octet.
- Các ion trái dấu hút nhau bằng lực hút nhau bằng lực hút tĩnh điện tạo nên hợp chất ion. Các ion trái dấu kết hợp với nhau theo tỉ lệ sao cho tổng điện tích của các ion trong hợp chất phải bằng 0.
Ví dụ: Quá trình hình thành liên kết ion trong phân tử NaCl
Nguyên tử Na nhường 1 electron ở lớp electron ngoài cùng cho nguyên tử Cl để tạo thành ion dương Na+.
Nguyên tử Cl nhận vào lớp electron ngoài cùng 1 electron của nguyên tử Na để tạo thành ion âm Cl-.
Hai ion Na+ và Cl- được tạo thành mang điện tích ngược dấu hút nhau để hình thành liên kết ion trong phân tử NaCl.
Na+ + Cl- → NaCl
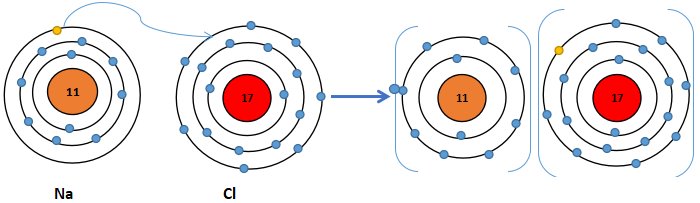
Quá trình hình thành liên kết ion trong phân tử NaCl
Nhận xét: Liên kết ion thường được hình thành giữa kim loại điển hình và phi kim điển hình.
II.Tinh thể ion
Ở điều kiện thường, các hợp chất ion tồn tại ở dạng tinh thể, đó là các chất rắn mà sự sắp xếp các cation và anion trong không gian tuân theo một trật tự nhất định tạo nên tinh thể ion.
1. Khái niệm
Tinh thể ion là loại tinh thể được tạo nên bởi các cation và anion.
Ví dụ: Tinh thể muối ăn (NaCl) được hình thành từ các ion Na+ và Cl- sắp xếp cạnh nhau một cách luân phiên.
 Mô hình cấu trúc tinh thể NaCl
Mô hình cấu trúc tinh thể NaCl
2. Đặc điểm của hợp chất ion
- Trong tinh thể ion, giữa các ion có lực hút tĩnh điện rất mạnh nên các hợp chất ion thường là chất rắn, khó nóng chảy, khó bay hơi ở điều kiện thường.
- Các tinh thể ion khá rắn chắc, nhưng khá giòn. Đây là tính chất đặc trưng của tinh thể ion.
- Các hợp chất ion có khả năng dẫn điện khi tan trong nước hay khi nóng chảy.
Ví dụ: NaCl nóng chảy ở 801oC, sôi ở 1465oC; CaO nóng chảy ở 2572oC, sôi ở 2850oC.
Giải thích: Các phần tử tạo nên hợp chất ion là các cation và anion. Chúng hút nhau bằng lực hút tĩnh điện. Do vậy, các phần tử này không chuyển động tự do được.
-
Chủ đề 1. Cấu tạo nguyên tử
-
Chủ đề 2. Bảng tuần hoàn các nguyên tố hóa học
-
Đề thi giữa học kì 1
-
Chủ đề 3. Liên kết hóa học
-
Đề thi cuối học kì 1
-
Chủ đề 4. Phản ứng Oxi hóa - khử
-
Chủ đề 5. Năng lượng hóa học
-
Đề thi giữa học kì 2
-
Chủ đề 6. Tốc độ phản ứng hóa học
-
Chủ đề 7. Nguyên tố nhóm VIIA (Nhóm Halogen)
-
Đề thi cuối học kì 2







