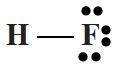Cho các phát biểu sai
(a) Nếu cặp electron dùng chung bị lệch về phía một nguyên tử khi đó là liên kết cộng hóa trị không cực.
(b) Nếu cặp electron dùng chung bị lệch về phía một nguyên tử thì đó là liên kết cộng hóa trị có cực.
(c) Cặp electron dùng chung luôn được tạo nên từ 2 electron của cùng một nguyên tử.
(d) Cặp electron dùng chung được tạo nên từ 2 electron hóa trị
(a) Sai vì: Nếu cặp electron chung bị lệch về phía một nguyên tử khi đó là liên kết cộng hóa trị có cực.
(b) Đúng.
(c) Sai vì: Cặp electron chung có thể được tạo nên từ 2 electron của cùng một nguyên tử (liên kết cho nhận) hoặc được tạo nên từ 2 electron của hai nguyên tử khác nhau, trong đó mỗi nguyên tử góp chung 1 electron.
(d) Đúng.