Tên gọi của alkane có công thức phân tử C3H8 là:
Tên gọi của alkane có công thức phân tử C3H8 là propane.
Tên gọi của alkane có công thức phân tử C3H8 là:
Tên gọi của alkane có công thức phân tử C3H8 là propane.
Trong các nhận xét dưới đây, nhận xét nào sai?
Nhận xét sai là: Tất cả các chất chỉ có liên kết đơn trong phân tử đều là alkane.
Ví dụ như chất CH3–O–CH3 đều chỉ có các liên kết đơn nhưng không phải là alkane.
Cho nhiệt đốt cháy hoàn toàn 1 mol các chất ethane, propane, butane và pentane lần lượt là 1570 kJmol−1; 2220 kJmol−1; 2875 kJmol−1 và 3536 kJmol−1. Khi đốt cháy hoàn toàn 1 gam chất nào sẽ thu được lượng nhiệt lớn nhất?
Nhiệt lượng khi đốt cháy 1 gam các hydrocarbon lần lượt là:
Ethane: . 1 570 = 52,33 (kJ)
Propane: .2 220 = 50,45 (kJ)
Butane: . 2 875 = 49,57 (kJ)
Pentane: . 3 536 = 49,11 (kJ)
Vậy đốt cháy ethane tỏa ra nhiều nhiệt lượng nhất.
Tính lượng nhiệt tỏa ra khi đốt cháy hỗn hợp gồm 0,3 mol butane và 0,5 mol propane. Biết rằng lượng nhiệt tỏa ra khi đốt cháy hoàn toàn 1 mol butane và 1 mol propane lần lượt là 2 877 kJ và 2 220 kJ.
Lượng nhiệt tỏa ra khi đốt cháy hỗn hợp gồm 0,3 mol butane và 0,5 mol propane là:
Q = 0,3.2 877 + 0,5.2 220 = 1973,1 (kJ)
Thành phần chính của khí thiên nhiên và khí mỏ dầu là:
Methane (CH4) là thành phần chính của khí thiên nhiên, khí mỏ dầu, biogas,...
Một loại xăng là hỗn hợp của các alkane có công thức phân tử C7H16 và C8H18. Để đốt cháy hoàn toàn 7,28 g xăng đó phải dùng vừa hết 19,832 lít O2 (lấy ở đkc). Phần trăm về khối lượng của C8H18 trong loại xăng đó là
Gọi lượng C7H16 là x mol, lượng C8H18 là y mol.
⇒ 100x + 114y = 7,28 (1)
Phương trình đốt cháy:
C7H16 + 11O2 → 7CO2 + 8H2O
mol: x 11x
C8H18 + O2 → 8CO2 + 9H2O
mol: y 12,5y
⇒ 11x + 12,5y = 0,8 (2)
Từ (1) và (2), tìm được x = 0,05; y = 0,02.
Phần trăm về khối lượng của C8H18 là:
Hình dưới biểu thị công thức cấu tạo đầy đủ của alkane A.
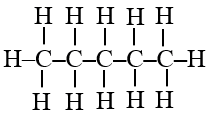
Công thức phân tử của alkane A là
Công thức phân tử của alkane A là C5H12.
Dãy nào sau đây chỉ gồm các alkane?
Công thức chung của các alkane là: CnH2n+2 (n ≥ 1).
⇒ Dãy chất chỉ gồm các alkane là: CH4, C2H6, C4H10, C5H12.
Cho các phát biểu sau về phản ứng cháy của alkane, phát biểu không đúng là:
Các alkane cháy tạo ra sản phẩm gồm CO2 và H2O.
Hydrocarbon A là alkane có khối lượng phân tử là 58 amu. Công thức phân tử của A là
Gọi công thức phân tử của A là CnH2n+2. Khối lượng phân tử của A là 58 amu nên:
14n + 2 = 58 ⇒ n = 4
Vậy alkane là C4H10.
Chất nào sau đây không phải là hydrocarbon?
Hydrocarbon là những hợp chất hữu cơ được tạo thành từ hai nguyên tố carbon và hydrogen.
Hợp chất CH3–CH2–OH có nguyên tố O trong phân tử nên không phải là hydrocarbon.
Gọi công thứng phân tử của X là CnH2n+2.
Alkane X có phần trăm khối lượng carbon bằng 81,82% nên:
⇒ n = 3
Vậy công thức phân tử của X là C3H8.
⇒ Tổng số các nguyên tử trong một phân tử X là 11.
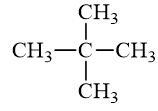
Số đồng phân cấu tạo mạch hở ứng với công thức phân tử C5H12 là
Các đồng phân cấu tạo mạch hở ứng với công thức phân tử C5H12 là
![]()
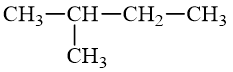
Trong thực tế, alkane thường được dùng làm nhiên liệu cho động cơ hoặc làm chất đốt. Tại sao alkane có ứng dụng này?
Khi đốt, alkane bị cháy tạo thì rất dễ cháy tạo ra CO2, H2O và tỏa nhiều nhiệt. Đặc biệt alkane còn có nhiều trong khí thiên nhiên và dầu mỏ nên được dùng làm nhiên liệu cho động cơ hoặc làm chất đốt.
Khi đốt cháy hoàn toàn một alkane X thu được 1,2 mol CO2 và 1,5 mol H2O. Công thức phân tử của X là
Gọi công thứng phân tử của X là CnH2n+2.
Phương trình phản ứng:
CnH2n+2 + O2 → nCO2 + (n + 1)H2O
mol: x → nx → (n + 1)x
⇒ n = 4
Vậy công thức phân tử của X là C4H10.
