Toluen tác dụng với Br2 chiếu sáng (tỷ lệ mol 1 : 1), thu được sẩn phẩm hữu cơ là
Khi toluen tác dụng với Br2 chiếu sáng (tỷ lệ mol 1 : 1) xảy ra phản ứng thế:
C6H5CH3 + Br2 C6H5CH2Br + HBr
Toluen tác dụng với Br2 chiếu sáng (tỷ lệ mol 1 : 1), thu được sẩn phẩm hữu cơ là
Khi toluen tác dụng với Br2 chiếu sáng (tỷ lệ mol 1 : 1) xảy ra phản ứng thế:
C6H5CH3 + Br2 C6H5CH2Br + HBr
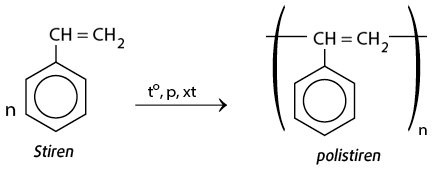
Chất nào sau đây có khả năng tham gia phản ứng trùng hợp tạo polime?
Stiren có khả năng tham gia phản ứng trùng hợp do có liên kết đôi kém bền dễ bị phá vỡ.
O-xylene có công thức cấu tạo là:




Đốt cháy hỗn hợp A gồm ba chất thuộc dãy đồng đẳng benzene cần dùng V lít không khí (đktc). Cho hấp thụ sản phẩm cháy vào bình đựng nước vôi thu được 3 gam kết tủa, khối lượng dung dịch tăng 12,012 gam. Đun nóng dung dịch thu được thêm 12 gam kết tủa nữa (các phản ứng xảy ra hoàn toàn). Không khí gồm 20% O2 và 80% N2. Giá trị gần nhất của V là:
Ta có mCO2 +mH2O = mdd tăng + m↓ = 12,012 + 3 = 15,012 gam
Do đun nóng dung dịch thu được thêm 12 gam kết tủa nữa nên:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,03 ← 0,03
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,24 ← 0,12
nCO2 = 0,03 + 0,24 = 0,27 mol
Sau khi đốt cháy A:
Bảo toàn O:
Cho sơ đồ phản ứng: styrene + H2 dư ![]() X. Công thức phân tử của X là
X. Công thức phân tử của X là
Phương trình phản ứng:
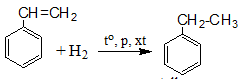
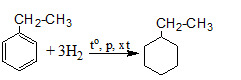
So với benzene, toluene phản ứng với dung dịch HNO3đặc/H2SO4đặc theo tỉ lệ 1:1 thì:
Toluene có sẵn nhóm thế loại 1 (nhóm đẩy electron) nên dễ tham gia phản ứng thế nguyên tử H của vòng benzene hơn benzene và sự thế ưu tiên ở vị trí ortho và para.
Cho các chất :
(1) C6H5–CH3
(2) p-CH3–C6H4–C2H5
(3) C6H5–C2H3
(4) o-CH3–C6H4–CH3
Có bao nhiêu chất là đồng đẳng của benzene?
Chất là đồng đẳng của benzene là: (1); (2) và (4).
(3) không phải vì nhánh –C2H3 không no.
Đốt cháy hoàn toàn 10,6 gam alkybenzene X thu được 17,92 lít CO2 (đktc). Công thức phân tử của X là
Gọi công thức phân tử của X là CnH2n-6:
Ta có nX.n = nCO2
n = 8 (C8H10)
Trong quy trình sản xuất benzene từ hexane, hiệu suất 50%, để sản xuất 19,5 kg benzene cần lượng hexane là:
Sơ đồ phản ứng:
C6H14 → C6H6
86kg → 78kg
Hợp chất nào sau đây không phải là hydrocarbon thơm?
Những phân tử chứa vòng benzene được gọi là hydrocarbon thơm hay arene.
Công thức phân tử của styrene là
Cho benzene tác dụng với lượng dư HNO3 đặc có xúc tác H2SO4 đặc để điều chế nitrobenzene. Khối lượng nitrobenzene điều chế được từ 19,5 tấn benzene (hiệu suất phản ứng 80%) là
nbenzene = 0,25 (mol)
Phương trình hóa học:
C6H6 + HONO2 → C6H5NO2 + H2O
0,25 → 0,25
Khối lượng nitrobenzene điều chế được:
mnitrobenzene = 0,25.80%.123 = 24,6 (gam)
Benzene tác dụng với Br2 theo tỷ lệ mol 1 : 1 (có mặt FeCl3), thu được sẩn phẩm hữu cơ là
Phương trình hóa học:
C6H6 + Br2 C6H5Br + HBr
Đốt cháy hết 9,18 gam 2 đồng đẳng của benzene A, B thu được 8,1 gam H2O và V lít CO2 (đktc). Giá trị của V là:
nH2O = 0,45 (mol)
mhỗn hợp hydrocarbon = mC + mH = 12nCO2 + 2nH2O = 9,18
nCO2 = 0,69 (mol)
V = 0,69.22,4 = 15,456 lít
Cho hỗn hợp A gồm các hơi và khí: 0,1 mol benzene, 0,2 mol toluene, 0,3 mol styrene và 1,4 mol hydrocarbon vào một bình kín, có chất xúc tác Ni. Đun nóng bình kín một thời gian, thu được hỗn hợp B gồm các chất: cyclohexane, methylcyclohexane, ethylcyclohexane, benzene, toluene, và hydrocarbon. Đốt cháy hoàn toàn lượng hỗn hợp B trên, rồi cho hấp thụ hết sản phẩm cháy vào bình đựng dung dịch nước vôi trong dư, để hấp thụ hết sản phẩm cháy. Độ tăng khối lượng bình đựng nước vôi là:
Đốt hỗn hợp khí B cũng như đốt hỗn hợp khí A, ta có:
nCO2 = 6.nC6H6 + 7.nC7H8 + 8.nC8H8 = 4,4 mol
mCO2 = 4,4.44 = 193,6 gam
nH2O = 3nC6H6 + 4nC7H8 + 4nC8H8 + nH2 = 3,7 mol
mH2O = 3,7.18 = 66,6 gam
Vậy độ tăng khối lượng của bình là
m = mCO2 + mHO = 193,6 + 66,6
= 260,2 gam
