Giá trị tuyệt đối của biến thiên enthalpy càng lớn thì
Giá trị tuyệt đối của biến thiên enthalpy càng lớn thì nhiệt lượng tỏa ra hay thu vào của phản ứng càng nhiều
Giá trị tuyệt đối của biến thiên enthalpy càng lớn thì
Giá trị tuyệt đối của biến thiên enthalpy càng lớn thì nhiệt lượng tỏa ra hay thu vào của phản ứng càng nhiều
Trong các phản ứng dưới đây, phản ứng nào tỏa nhiều nhiệt nhất?
Phản ứng tỏa nhiều nhiệt nhất là:
2Al (s) + O2 (g) → Al2O3 (s)
Cho các phản ứng sau:
(a) Nến cháy trong không khí.
(b) Đốt cháy cồn cháy trong không khí.
(c) Phản ứng nung vôi .
(d) Nước lỏng bay hơi.
Số phản ứng thu nhiệt là
a) Nến cháy trong không khí là phản ứng tỏa nhiệt
b) Đốt cháy cồn cháy trong không khí là phản ứng tỏa nhiệt
C2H5OH + O2 → CO2 + H2O
⇒ Phản ứng chỉ cần cung cấp nhiệt vào thời điểm ban đầu và có tỏa nhiệt trong quá trình phản ứng ⇒ Phản ứng tỏa nhiệt.
c) Phản ứng nung vôi là phản ứng thu nhiệt
d) Nước lỏng bay hơi là phản ứng thu nhiệt
Số oxi hóa của Fe trong FexOy là:
Số oxi hóa của O là -2, gọi số oxi hóa của Fe là a, ta có:
x.a + y.(-2) = 0 ⇒ a =
Đốt 6 gam bột Mg trong bình kín chứa V lít O2 thu được chất rắn X. Hòa tan hết X trong dung dịch HCl dư thu được 2,479 lít H2. Biết các phản ứng xảy ra hoàn toàn, các chất khí đo ở điều kiện chuẩn (1bar, 25oC). Tính V?
nH2 = 2,479 : 24,79 = 0,1 mol
nMg = 6 : 24 = 0,25 mol
Đặt số mol của O2 là a mol
Quá trình trao đổi electron
|
Mg0 → Mg2+ + 2e 0,25 → 0,5 |
O2 + 4e → 2 O2- a → 4a |
|
2H+ + 2e → H2 0,2 ← 0,1 |
Áp dụng định luật bảo toàn electron ta có
4a + 0,2 = 0,5 → a = 0,075 mol
Thể tích O2 tham gia phản ứng là:
V = 0,075.24,79 = 1,85925 (lít)
Trong phân tử, khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các
Trong phân tử, khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các lưỡng cực tạm thời.
Dẫn khí H2 đi qua ống sứ đựng bột CuO nung nóng để thực hiện phản ứng hóa học sau:
CuO + H2 ![]() Cu + H2O
Cu + H2O
Trong phản ứng trên, chất đóng vai trò chất oxi hoá là
Chất khử là chất nhường electron (số oxi hóa tăng).
Chất oxi hóa là chất nhận electron (số oxi hóa giảm).
Xét sự thay đổi số oxi hóa
H2 là chất khử
CuO là chất oxi hóa.
Cho phương trình nhiệt hóa học của phản ứng:
C4H9OH(g) + 6O2(g) ![]() CO2(g) + 5H2O(g)
CO2(g) + 5H2O(g) ![]() = -134 kJ. Phản ứng trên là phản ứng:
= -134 kJ. Phản ứng trên là phản ứng:
Phản ứng có = -134 kJ < 0
Phản ứng tỏa nhiệt
Số oxi hóa của đơn chất kim loại là:
Trong đơn chất, số oxi hóa của nguyên tử bằng 0.
⇒ Số oxi hóa của đơn chất kim loại là 0
Cho 4,68 g kim loại M (hóa trị n) tác dụng với dung dịch H2SO4 (đặc, nóng, dư) thu được 6,4454 L khí SO2 (đkc). Kim loại M là:
nSO2 = 6,4454 : 24,79 = 0,26 mol
Sơ đồ phản ứng:
Quá trình trao đổi electron
Phương trình phản ứng: 2M + 2nH2SO4 → M2(SO4)n + nSO2 + 2nH2O
Theo phương trình phản ứng ta có:
Lập bảng xét giá trị ta có:
| n | 1 | 2 | 3 |
| M | 9 | 18 | 27 |
Có các phản ứng hóa học sau:
(1) 2Na(s) + ![]() O2(g)
O2(g) ![]() Na2O(s)
Na2O(s) ![]() = -417,98 kJ
= -417,98 kJ
(2) ![]() H2(g) +
H2(g) + ![]() I2(r)
I2(r) ![]() HI(g)
HI(g) ![]() = 26,48 kJ
= 26,48 kJ
Phát biểu nào sau đây là đúng?
Phản ứng tỏa nhiệt (< 0) thường diễn ra thuận lợi hơn các phản ứng thu nhiệt (
> 0).
Phản ứng (1) là phản ứng tỏa nhiệt; phản ứng (2) là phản ứng thu nhiệt phản ứng (1) diễn ra thuận lợi hơn rất nhiều so với phản ứng (2).
Ở điều kiện chuẩn, phản ứng (2) chỉ xảy ra khi được đốt nóng (cung cấp nhiệt); dừng đốt nóng, phản ứng (2) sẽ dừng lại.
Chọn ý không đúng khi nói về phản ứng tỏa nhiệt
Phản ứng tỏa nhiệt làm tăng nhiệt độ môi trường sau phản ứng.
Phản ứng tỏa nhiệt có thể xảy ra tự phát.
Một số phản ứng tỏa nhiệt cần khơi mào để phản ứng xảy ra.
Phản ứng tỏa nhiệt thường xảy ra nhanh và mãnh liệt hơn phản ứng thu nhiệt.
Phản ứng giữa 2 mol khí hydrogen và 1 mol khí oxygen tạo thành 2 mol H2O lỏng, giải phóng nhiệt lượng 571,68 kJ. Phương trình nhiệt hóa học được biểu diễn là
Phản ứng giữa 2 mol khí hydrogen và 1 mol khí oxygen tạo thành 2 mol H2O lỏng, giải phóng nhiệt lượng 571,68 kJ ⇒ Phương trình nhiệt hóa học được biểu diễn là
Cho 11,2 gam Fe tác dụng hoàn toàn với dung dịch H2SO4 loãng. Thể tích khí H2 thu được ở đkc là
nFe = 0,2 mol
Xét quá trình cho e:
0Fe → Fe+2 + 2e
Xét quá trình nhận e:
2H+1 + 2e → H02
Áp dụng bảo toàn electron
ne nhận = ne cho
⇒ 2.nFe = 2.nH2 ⇒ nH2 = 0,2 mol
⇒ VH2 = 0,2.24,79 = 4,958 L
Để hàn nhanh đường ray tàu hỏa bị hỏng, người ta dùng hỗn hợp tecmit để thực hiện phản ứng nhiệt nhôm sau:
Al + Fe2O3 → Al2O3 + Fe.
Phát biểu nào sau đây sai?
Xác định sự thay đổi số oxi hóa
|
Quá trình oxi hóa : 1x Quá trình khử: 2x |
Al0 → Al+3 + 3e 2Fe+3 + 2.3e → 2Fe0 |
Chất khử: Al
Chất oxi hóa là Fe2O3
2Al + Fe2O3 → Al2O3 + 2Fe.
Tỉ lệ giữa chất bị khử: chất bị oxi hóa là 1:2.
Phản ứng tổng hợp ammonia:
N2(g) + 3H2(g) ![]() 2NH3(g)
2NH3(g) ![]() = -92 kJ
= -92 kJ
Biết năng lượng liên kết (kJ/mol) của N![]() N và H-H lần lượt là 946 và 436. Năng lượng liên kết của N-H trong ammonia là
N và H-H lần lượt là 946 và 436. Năng lượng liên kết của N-H trong ammonia là
Ta có:
= Eb(N
N) + 3Eb(H-H) - 2.3.Eb(N-H)
-92 = 946 + 3.436 - 2.3.Eb(N-H)
Eb(N-H) = 391 kJ/mol
Phản ứng nào sau đây có thể tự xảy ra ở điều kiện thường?
Phản ứng giữa Mg và dung dịch H2SO4 loãng xảy ra ở nhiệt độ thường
Mg + H2SO4 → MgSO4 + H2
Enthalpy tạo thành chuẩn của các đơn chất bền bằng
Enthalpy tạo thành chuẩn của các đơn chất bền bằng 0 kJ/ mol.
Sulfur trong hợp chất nào sau đây có số oxi hoá là +4?
,
,
Cho 2,88 g kim loại R (hóa trị n) tác dụng với dung dịch H2SO4 (đặc, nóng, dư) thu được 2,9748 L SO2 (điều kiện chuẩn). Kim loại R là
nSO2 = 2,9748:24,79 = 0,12 mol
Ta có:
M → M+n + ne
→
S+6 + 2e → S+4
0,12→ 0,12.2
Áp dụng định luật bảo tòan e ta có:
⇒ MR = 12n
Vì R là kim loại, n là số oxi hoá của R ⇒ n = 1,2,3
Xét bảng sau:
|
n |
1 |
2 |
3 |
|
MR |
12 (Loại |
24 (Mg) |
36 (Loại) |
Vậy kim loại R là Mg.
Cho phương trình hóa học: Al + H2SO4 → Al2(SO4)3 + SO2 + H2O. Hệ số cân bằng (là số nguyên, tối giản) của các chất trong sản phẩm lần lượt là
Xác định số oxi hoá của những nguyên tố thay đổi số oxi hoá
Quá trình oxi hoá và quá trình khử
|
2x 3x |
Al0 → Al+3 +3e S+6 + 2e → S+4 |
Đặt hệ số của chất oxi hoá và chất khử vào sơ đồ phản ứng và kiểm tra lại ta được phương trình cân bằng
2Al + 6H2SO4 → Al2(SO4)3 + 3SO2 + 6H2O
Hệ số cân bằng (là số nguyên, tối giản) của các chất trong sản phẩm lần lượt là: 1 : 3 : 6
Ở điều kiện chuẩn, nhiệt lượng tỏa ra của phản ứng sau là 1035,88 kJ
2H2S(g) + 3O2(g) → 2SO2(g) + 2H2O(g)
Tính ΔfHo298 của H2S? Cho biết nhiệt tạo thành của các chất là
Chất | O2(g) | SO2(g) | H2O(g) |
(kJ/mol) | 0 | -296,8 | -241,8 |
Phản ứng
2H2S(g) + 3O2(g) → 2SO2(g) + 2H2O(g)
Tỏa nhiệt nên ΔrHo298 = - 1035,88 kJ
Đặt nhiệt tạo thành của H2S là x ta có:
ΔrHo298 = ΣΔfHo298 (sp) - ΣΔfHo298 (cđ) = -1035,88
⇔ 2.(-296,8) + 2.(-241,8) – 2.x - 3.0 = - 1035,88
→ x = - 20,66 kJ
Số lượng mỗi loại liên kết có trong phân tử CH3OH là
Công thức cấu tạo của CH3OH:
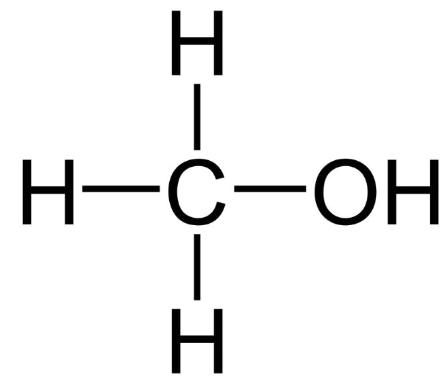
3 liên kết C – H, 1 liên kết C – O và 1 liên kết O – H
Cho phản ứng hydrogen hóa ethylene sau:
H2C=CH2(g) + H2(g) → H3C-CH3(g)
Biết năng lượng trung bình các liên kết trong các chất cho trong bảng sau:
|
Liên kết |
Eb (kJ/mol) |
Liên kết |
Eb (kJ/mol) |
|
C=C |
612 |
C-C |
346 |
|
C-H |
418 |
H-H |
436 |
Biến thiên enthalpy (kJ) của phản ứng có giá trị là:
= EC=C + 4.EC-H + EH-H – EC-C – 6EC-H
= EC=C + EH-H – EC-C – 2EC-H
= 612 + 436 – 346 – 2.418 = -134 (kJ)
Cho phản ứng sau: CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (g). Công thức tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành chuẩn của các chất là
Phản ứng: CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (g)
Biến thiên enthalpy của phản ứng tính theo nhiệt tạo thành chuẩn:
Cho các chất sau, chất nào có ![]() ≠0?
≠0?
Đơn chất không bền Fe (l) có ≠0.
Cho phản ứng sau đây là phản ứng thu nhiệt:
CH4 (g) + H2O (l) → CO (g) + 3H2 (g)
Giá trị ![]() nào sau đây là đúng?
nào sau đây là đúng?
Vì phản ứng thu nhiệt nên > 0 ⇒
= 250 kJ.
Khi nghiên cứu các phản ứng
(1) C(s) + O2(g) → CO2(s)
(2) CaCO3(s) → CaO(s) + CO2(g)
Nhận thấy khi ngừng đun nóng, phản ứng (2) dừng lại còn phản ứng (1) tiếp tục xảy ra, chứng tỏ
Nhận thấy khi ngừng đun nóng, phản ứng (2) dừng lại ⇒ phản ứng (2) là phản ứng thu nhiệt.
Nhận thấy khi ngừng đun nóng, phản ứng (1) tiếp tục xảy ra ⇒ phản ứng (1) là phản ứng tỏa nhiệt.
Cho quá trình Mn+7 + 5e → Mn+2, đây là quá trình
Quá trình oxi hóa (sự oxi hóa) là quá trình nhường electron.
Quá trình khử (sự khử) là quá trình thu electron.
Quá trình Mn+7 + 5e → Mn+2 là quá trình khử
Hòa tan hết 7,44 gam hỗn hợp Al, Mg trong thể tích vừa đủ là 500 mL dung dịch HNO3 loãng thu được dung dịch A và 3,4706 L (đkc) hỗn hợp hai khí đẳng mol có khối lượng 5,18 gam, trong đó có một khí bị hóa nâu trong không khí. Thành phần phần trăm theo khối lượng của kim loại Al trong hỗn hợp là:
nhỗn hợp khí = 3,4706 : 24,79 = 0,14
Khối lượng trung bình của hỗn hợp khí là:
Có 1 khí không màu hóa nâu trong không khí → khí NO ⇒ Khí còn lại là NO2
⇒ nNO = nNO2 = 0,14:2 = 0,07 mol
Gọi số mol Al, Mg trong hỗn hợp lần lượt là x, y
mhỗn hợp = 27x + 24y = 7,44 (g) (1)
|
Al → Al3+ + 3e x → 3x mol Mg → Mg2+ + 2e y → 2x mol |
N+5 + 3e → N+2 (NO) 0,21 ← 0,07 2N+5 + 8e → 2N+1 (N2O) 0,56 ← 0,07 |
Theo định luật bảo toàn e
3x + 2y = 0,21 + 0,56 = 0,77 (2)
Giải hệ phương trình (1) và (2) giải hệ phương trình ta được:
→ x = 0,2; y = 0,085
⇒ mAl = 0,2.27 = 5,4 gam
%mAl = 5,4 : 7,44 .100% = 72,58%
Nguyên tử carbon trong trường hợp nào sau đây vừa thể hiện tính khử, vừa thể hiện tính oxi hoá khi tham gia phản ứng hoá học?
Trong đơn chất C, nguyên tử carbon có số oxi hóa là 0, đây là số oxi hóa trung gian của carbon, do đó trong đơn chất C, nguyên tử carbon vừa có khả năng thể hiện tính oxi hoá, vừa có khả năng thể hiện tính khử.
Một hộ gia đình mua than đá làm nhiên liệu đun nấu và trung bình mỗi ngày dùng hết 1,60 kg
than. Giả thiết loại than đá trên chứa 90% carbon về khối lượng, còn lại là các tạp chất trơ.
Cho phản ứng: C (s) + O2 (g) ![]() CO2 (g)
CO2 (g) ![]()
Nhiệt lượng cung cấp cho hộ gia đình từ quá trình đốt than trong một ngày tương đương bao nhiêu số điện? Biết rằng 1 số điện = 1 kWh = 3600 kJ. Nguyên tử khối của carbon là 12.
Khối lượng carbon trong than đá là:
Nhiệt tỏa ra khi đốt 1,6 kg than đá = 120.393,5 = 47 220 kJ
Cho phản ứng:
NaOH (aq) + HCl (aq) → NaCl (aq) + H2O (l) ![]()
Khẳng định sai là:
< 0 ⇒ Phản ứng tỏa nhiệt
Biến thiên enthalpy chuẩn của phản ứng là -57,9 kJ.
Nhiệt tạo thành chuẩn của NaCl (aq) là -57,9 kJ mol-1. ⇒ Sai vì đây không phải phản ứng tạo thành NaCl từ các đơn chất ở dạng bền nhất.
Phản ứng làm nóng môi trường xung quanh ⇒ đúng vì phản ứng tỏa nhiệt làm nóng môi trường xung quanh.
Methane (CH4) được sử dụng làm nhiên liệu, nguyên nhân chính là do methane
Phản ứng nào sau đây là phản ứng oxi hoá – khử?
Phản ứng tự oxi hóa - khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của ít nhất một nguyên tố hóa học.
Phản ứng sau là phản ứng oxi hóa khử
Trong các hợp chất sau, hợp chất nào chlorine (Cl) có số oxi hóa thấp nhất?
Số oxi hóa của chlorine trong các chất sau: KClO3; Cl2; KClO4; KCl lần lượt là: +5, 0, +7, -1.
Vậy trong hợp chất KCl chlorine (Cl) có số oxi hóa thấp nhất
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
|
Liên kết |
C–H |
C–C |
C=C |
|
E b (kJ/mol) |
418 |
346 |
612 |
Biến thiên enthalpy của phản ứng: C3H8 (g) → CH4 (g) + C2H4 (g) có giá trị là
Phản ứng:
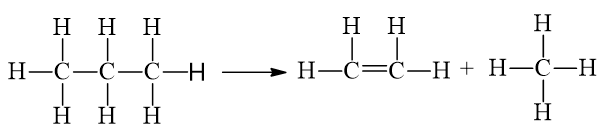
∑Eb(cđ)=2.Eb(C – C) + 8.Eb(C – H) = 2.346 + 8.418 = 4036 kJ
∑Eb(sp)=1.Eb(C = C) + 8.Eb(C – H) = 1.612 + 8.418 = 3956 kJ
⇒ ∑Eb(cd)−∑Eb(sp) = 4036 – 3956 = 80 kJ
Cho thanh zinc vào ống nghiệm chứa 2 ml HCl, zinc phản ứng với HCl theo phương trình hoá học sau: Zn + 2HCl → ZnCl2 + H2. Nhận xét nào sau đây là đúng?
Phản ứng:
Zn nhường electron nên là chất khử.
Ion H+ nhận electron nên là chất oxi hoá.
Quá trình oxi hoá: .
Quá trình khử: .
Cho năng lượng liên kết của một số liên kết như sau:
| Liên kết | H-H | C-H | C-C | C≡C |
| Eb(kJ/mol) | 432 | 413 | 347 | 839 |
Tính biến thiên enthalpy chuẩn của các phản ứng:
H3C-C≡CH (g) + 2H2(g) → CH3-CH2-CH3 (g)
Phản ứng:
H3C-C≡CH(g) + 2H2(g) → CH3-CH2-CH3 (g)
Cho phản ứng sau:
2H2(g) + O2(g) → 2H2O(g) ![]()
Enthalpy tạo thành chuẩn của H2O(g) là
Enthalpy tạo thành chuẩn của H2O(g) là – 241,82 kJ/ mol
