Liên kết cộng hóa trị là liên kết hóa học được hình thành giữa hai nguyên tử bằng
Liên kết cộng hóa trị là liên kết hóa học được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung
Liên kết cộng hóa trị là liên kết hóa học được hình thành giữa hai nguyên tử bằng
Liên kết cộng hóa trị là liên kết hóa học được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung
Liên kết tạo thành do sự góp chung electron thuộc loại liên kết:
Liên kết tạo thành do sự góp chung electron thuộc loại liên kết cộng hóa trị.
Liên kết cộng hóa trị không phân cực thường là liên kết giữa?
Liên kết cộng hóa trị không phân cực thường là liên kết giữa hai phi kim giống nhau.
Hợp chất nào sau đây có liên kết cộng hóa trị không phân cực?
Hiệu độ âm điện trong phân tử N2 bằng 0.
Cho các hợp chất sau: NH3, Al2O3, H2S, NaCl, H2O. Số hợp chất mà phân tử chứa liên kết ion là?
Hợp chất mà phân tử chứa liên kết ion là: Al2O3, NaCl.
Hợp chất nào sau đây có liên kết cộng hóa trị phân cực?
Cl2 và N2 có hiệu độ âm điện bằng 0 ⇒ Có liên kết cộng hóa trị không phân cực.
Hợp chất CHCl3 gồm 1 liên kết C-H và 3 liên kết C-Cl
Hợp chất CH4 gồm 4 liên kết C-H
Δ(C-H) = |2,55 – 2,2| = 0,35 ⇒ Liên kết cộng hóa trị không phân cực
Δ(C-Cl) = |2,55 – 3,16| = 0,61 ⇒ Liên kết cộng hóa trị phân cực.
Vậy hợp chất CHCl3 có liên kết cộng hóa trị không phân cực
Liên kết σ là liên kết hình thành do:
Liên kết σ là liên kết hình thành do sự xen phủ trục của hai orbital
Số liên kết σ và π có trong phân tử C2H2 lần lượt là?
Ta có công thức cấu tạo của C2H2 là: H-C≡C-H
Liên kết 3 gồm 1 liên kết σ và 2 liên kết π.
Vậy tổng số liên kết σ và π có trong phân tử C2H2 lần lượt là: 3 và 2
Hợp chất nào sau đây là hợp chất cộng hóa trị?
Các hợp chất NaCl, K2O, MgO là các hợp chất ion được hình thành từ kim loại điển hình và phi kim điển hình.
HCl là hợp chất cộng hóa trị. Nguyên tử hydrogen liên kết với nguyên tử chlorine bằng cách mỗi nguyên tử góp chung 1 electron tạo thành 1 cặp electron dùng chung trong phân tử HCl.
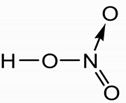
Phân tử chất nào sau đây có liên kết cho - nhận?
Ta có:
Cho các hợp chất sau: Cl2, KCl, HCl, CO2, NaBr. Số hợp chất chứa liên kết cộng hóa trị là?
Các hợp chất chứa liên kết cộng hóa trị là: Cl2, HCl, CO2.
NaCl và NaF được tạo thành bởi kim loại điển hình và phi kim điển hình nên có liên kết ion.
Các chất có chứa liên kết cộng hóa trị có thể tồn tại ở trạng thái nào:
Tính chất chung của hợp chất ion là: Thường là chất rắn, có nhiệt độ nóng chảy và nhiệt độ sôi cao, có khả năng dẫn điện khi tan trong nước hay khi nóng chảy.
Phát biểu nào sau đây sai về các liên kết được tạo thành bởi sự xen phủ các orbital nguyên tử
Liên kết ba gồm một liên kết σ và hai liên kết π
Trong phân tử CO2 có chứa loại liên kết nào (biết độ âm điện của tử C là 2,55 và O là 3,44)
Δ(C-O) = |2,55 – 3,44| = 0,89 ⇒ Liên kết cộng hóa trị phân cực.
Tuy nhiên, do phân tử CO2 có cấu tạo thẳng nên độ phân cực của hai liên kết đôi (C=O) triệt tiêu nhau, dẫn đến toàn bộ phân tử không bị phân cực.
Cho hai nguyên tố X (Z = 20) và Y (Z = 17). Công thức hợp chất tạo thành từ nguyên tố X, Y và liên kết trong phân tử là:
X (Z = 20): 1s22s22p63s23p64s2
Y (Z = 17): 1s22s22p63s23p5
Nguyên tử X là kim loại mạnh, có xu hướng nhường đi 2 electron lớp ngoài cùng tạo thành cation X2+.
Nguyên tử Y là phi kim điển hình, có xu hướng nhận thêm 1 electron và lớp ngoài cùng tạo thành anion Y-.
Ion X2+ và Y- trái dấu hút nhau tạo thành phân tử XY2. Liên kết được tạo thành là liên kết ion.
X2+ + 2Y- → XY2.
Liên kết trong phân tử nào sau đây được hình thành nhờ sự xen phủ orbital p – p:
H (Z = 1): 1s1
Cl (Z = 17): 1s22s22p63s23p5
N (Z = 7): 1s22s22p3
Liên kết trong phân tử H2 được hình thành nhờ sự xem phủ orbital s – s
Liên kết trong phân tử Cl2 được hình thành bởi sự xen phủ orbital p – p
Liên kết trong phân tử NH3 được hình thành bởi sự xen phủ orbital s – p
Liên kết trong phân tử HCl được hình thành bởi sự xen phủ orbital s – p
Dãy hợp chất nào dưới đây chứa liên kết cộng hóa trị
BaCl2 và NaCl, Na2O, CaCl2 chứa liên kết ion.
Vậy dãy hợp chất chứa liên kết cộng hóa trị là SO3, H2S, H2O.
Yếu tố nào đặc trưng cho độ bền của liên kết:
Năng lượng liên kết đặc trưng cho độ bền của liên kết. Năng lượng liên kết càng lớn thì liên kết càng bền và phân tử càng khó bị phân hủy.
Liên kết π là liên kết hình thành do:
Liên kết π là liên kết hình thành do sự xen phủ bên của hai orbital.
Các liên kết trong phân tử oxygen gồm:
Trong phân tử oxygen (O2) hai nguyên tử O liên kết với nhau bằng 1 liên kết đôi (O=O).
1 liên kết đôi gồm 1 liên kết σ, 1 liên kết π.
