Trong điều kiện thích hợp có phản ứng sau: C2H2 + H2O → X. Xác định công thức của X là
Phương trình phản ứng:
C2H2 + H2O CH3CHO
Sản phẩm thu được là: CH3CHO
Trong điều kiện thích hợp có phản ứng sau: C2H2 + H2O → X. Xác định công thức của X là
Phương trình phản ứng:
C2H2 + H2O CH3CHO
Sản phẩm thu được là: CH3CHO
Cho các chất: metane, ethylene, acetylene, pent-1-ene. Số chất làm mất màu dung dịch KMnO4 là
Các alkene phản ứng được với dung dịch KMnO4 ở ngay điều kiện thường
⇒ ethylene, acetylene, pent-1-ene
Để phân biệt alk-1-yne và alkene, ta có thể dùng
Để nhận biết alk-1-yne và alkene ta sử dụng dung dịch AgNO3/NH3.
Chỉ có Alk-1-ene phản ứng sẽ tạo kết tủa màu vàng.
Cụ thể nếu Alk-1-yne ở đây là Acetylene thì ta có phương trình phản ứng hóa học sau:
CH ≡ CH + 2AgNO3 + 2NH3→ CAg ≡ CAg↓vàng + 2NH4NO3
Đốt cháy hoàn toàn 0,2 mol hỗn hợp X gồm 2 alkene là đồng đẳng kế tiếp nhau thu được CO2 và H2O có khối lượng hơn kém nhau 13,52 gam. Công thức của 2 alkene là:
Đốt cháy hoàn toàn alkene thu được số mol CO2 và H2O bằng nhau
⇒ nCO2 = nH2O = x mol
mCO2 – mH2O = 44x – 18x = 13,52
⇒ x = 0,52 mol
⇒ Số C trung bình = nCO2 : nAlkene = 0,52:0,2 = 2,6
⇒ Công thức phân tử của 2 alkene là C2H4 và C3H6
Số đồng phân alkene ứng với công thức C5H10 là:
CH2 = CH – CH2 – CH2 – CH3
CH3 – CH= CH – CH2 – CH3
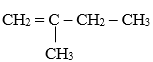
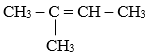
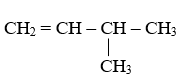
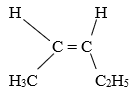
CH3–CH=CH–CH2–CH3: pent-2-ene có đồng phân hình học:
Khí nào sau đây được gọi là khí hồ ao
Methane còn được gọi là khí hồ ao vì methane được tìm thấy trong sự phân huỷ kị khí ở các ao hồ, đầm lầy …
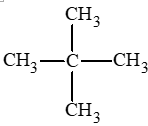
Alkane X có công thức phân tử C5H12. Xác định tên gọi của X, biết X chỉ có thể tạo ra một dẫn xuất monochloro duy nhất.
X chỉ có thể tạo ra một dẫn xuất monochloro duy nhất do đó chỉ có thể là:
2,2 – dimethylpropane.
Oxi hóa ethylene bằng dung dịch KMnO4 thu được sản phẩm gồm:
Phương trình phản ứng minh họa:
3C2H4 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2MnO2↓ + 2KOH
Sản phẩm thu được là: MnO2, C2H4(OH)2, KOH.
Trùng hợp 20,8 gam styrene được hỗn hợp X gồm polistyrene và styrene (dư). Cho X tác dụng với 400 ml dung dịch Br2 0,15M, sau đó cho dung KI dư vào thấy xuất hiện 2,54 gam Iodine. Hiệu suất trùng hợp styrene là:
nStyrene bđ = 20,8 :104 = 0,2 mol
Phương trình phản ứng hóa học xảy ra
(1) C6H5CH=CH2 + Br2 → C6H5CHBr-CH2Br
0,05 ← 0,05
(2) Br2 + 2KI → 2KBr + I2
0,01 ← 0,01
nI2 = 2,54:254 = 0,01 mol
Theo phương trình phản ứng (2) ta có:
nBr2 dư = nI2 = 0,01 mol
nBr2 pư = 0,4.0,15 - 0,01 = 0,05 mol
Theo phương trình (1)
nStiren dư = nBr2 pư = 0,05 mol
nStiren tham gia pứ trùng hợp
= nban đầu - nStiren dư = 0,2 - 0,05 = 0,15 mol.
H = 0,15:0,2.100% = 75%.
Nhận định nào sau đây không đúng tính chất của benzene.
Nhận định không đúng là: Benzene làm mất màu dung dịch nước brom.
Vì Benzene không làm mất màu dung dịch nước brom.
Đốt cháy hoàn toàn hydrocarbon A, sau phản ứng thu được 30,8 gam CO2 và 7,2 gam H2O. Xác định công thức cấu tạo của A.
Gọi công thức Hydrocarbon có công thức phân tử là CxHy.
nCO2 = 30,8 : 44= 0,7 mol;
nH2O = 7,2:18 = 0,4 mol
Phương trình phản ứng cháy:
CxHy + (x + )O2
xCO2 +
yH2O.
Dựa vào phương trình ta có:
nCO2 : nH2O = x : y = 0,7:0,4
⇒
Công thức đơn giản nhất của A: (C7H8)n Với n = 1 thỏa mãn đề bài
Công thức phân tử: C7H8
C6H5 – CH3
Dãy nhận xét nào sau đây đúng khi nói về tính chất vật lí của hydrocarbon thơm:
(1) Các hydrocarbon thơm thường là chất lỏng hoặc chất rắn ở điều kiện thường.
(2) Các hydrocarbon thơm không tan trong nước, tan nhiều trong dung môi hữu cơ
(3) Các hydrocarbon thơm dễ tan trong nước.
(4) Các hydrocarbon thơm có tính độc.
(5) Các hydrocarbon thơm đều là chất khí.
Tính chất vật lí của các hydrocarbon thơm:
Thường là chất lỏng hoặc chất rắn ở điều kiện thường.
Không tan trong nước nhưng tan nhiều trong dung môi hữu cơ.
Thường là các chất độc.
Cho các nhận xét sau:
1) Alkyne là những hydrocarbon không no, mạch hở, có chứa một liên kết ba trong phân tử.
2) Alkyne là những hidrocacbon mạch hở có chứa liên kết ba trong phân tử.
3) Các Alkyne không tan trong nước, hoặc rất ít tan trong nước.
4) Alkyne không có đồng phân hình học.
5) Alkene là hydrocarbon mạch hở có chứa liên kết đôi C=C.
6) Liên kết ba gồm 2 liên kết π và một liên kết σ.
Nhận xét nào là đúng:
Số nhận xét đúng là 1); 3); 4); 6)
2) Alkyne là những hidrocacbon mạch hở có chứa liên kết ba trong phân tử ⇒ sai vì
5) Alkene là hydrocarbon mạch hở có chứa liên kết đôi C=C. sai Alkene là hydrocarbon mạch hở, chỉ có chứa 1 liên kết đôi C=C.
Tiến hành cho hỗn hợp X gồm Al4C3 và CaC2 có số mol lần lượt là x, y vào nước dư thu được dung dịch X; a gam kết tủa Y và hỗn hợp khí Z. Lọc bỏ kết tủa Y. Đốt cháy hoàn toàn khí Z được sản phẩm cháy dẫn vào dung dịch X thu được thêm a gam kết tủa Y nữa. Biết các phản ứng xảy ra hoàn toàn. Xác định tỉ lệ x : y là
Phương trình phản ứng xảy ra:
(1) Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
(2) CaC2 + 2H2O → Ca(OH)2 + C2H2
(3) 2Al(OH)3 + Ca(OH)2 → Ca(AlO2)2 + 4H2O
Kết tủa Y là Al(OH)3 ⇒ trong dung dịch X chỉ chứa Ca(AlO2)2
Bảo toàn nguyên tố Ca: nCa(OH)2= nCa(AlO2)2 = y mol
Bảo toàn nguyên tố Al: 4.nAl4C3= nAl(OH)3 (1) + 2.nCa(AlO2)2 ⇒ nAl(OH)3 (1) = 4x – 2y
Đốt cháy khí Z (C2H2 và CH4) thu được CO2
Bảo toàn nguyên tố C: nCO2 = 3.nAl4C3 + 2.nCaC2 = 3x + 2y
Sục CO2 vào dung dịch X:
Ca(AlO2)2 + 2CO2 + 4H2O → 2Al(OH)3↓ + Ca(HCO3)2
Vì nCa(AlO2)2= ⇒ Phản ứng tính theo Ca(AlO2)2
⇒ nAl(OH)3 (2) = 2.nCa(AlO2)2 = 2y
Vì lượng kết tủa lần 1 thu được bằng lượng kết tủa lần 2
⇒ nAl(OH)3 (1) = nAl(OH)3 (2) ⇒ 4x – 2y = 2y
⇒ x = y
⇒ tỉ lệ x : y = 1 : 1
Đốt cháy hoàn toàn m gam alkyne X thu được m gam nước. Công thức phân tử của X là
Ta có:
nH2O =
Áp dụng bảo toàn khối lượng ta có:
malkyne = mC + mH
⇒ mC = malkyne - mH
⇒ mC = m - 2. =
⇒ Công thức đơn giản nhất của X là C2H3 ⇒ Dựa vào đáp tìm được công thức phân tử của X là C4H6
Cho 5,6 gam alkene A làm mất màu vừa đủ dung dịch chứa 16 gam Br2. Hydrate hóa A chỉ thu được một alcohol duy nhất. Tên gọi của A là:
nBr2 = 0,1 mol
⇒ nalkene = nBr2 = 0,1 mol
⇒ Malkene = 5,6:0,1 = 56 gam/mol
⇒ Alkene có công thức phân tử là C4H8
Vì hydrate hóa A chỉ thu được 1 alcohol duy nhất
⇒ A là CH3-CH=CH-CH3 (but-2-ene).
Thuốc thử dùng để nhận biết 3 dung dịch: hex-1-ene, hex-1-yne, hexane là
Nhận biết 3 dung dịch: hex-1-ene, hex-1-yne, hexane ta dùng dung dịch AgNO3/NH3 và dung dịch bromine.
Ta cho các chất phản ứng lần lượt với AgNO3 /NH3
Xuất hiện kết tủa vàng nhạt xuất hiện → hex-1-yne:
HC≡C-CH2-CH2 -CH2 -CH3 + AgNO3 /NH3 → AgC≡C-CH2 -CH2 -CH2 -CH3 ↓ + NH4NO3
Không có hiện tượng gì là hexane và hex-1-ene.
Cho hai dung dịch còn lại phản ứng với bromine:
Bromine mất màu → hex-1-ene
CH2=CH-CH2-CH2-CH2-CH3 + Br2 → CH2 Br-CHBr-CH2-CH2-CH2-CH3
Nếu không có hiện tượng gì là hexane.
Để làm sạch ethene có lẫn acetylene cần cho hỗn hợp qua dung dịch
Để làm sạch ethene có lẫn acetylene ta cho hỗn hợp đi qua dung dịch dung dịch AgNO3 /NH3 dư vì khi đó chỉ có acetylene phản ứng và bị giữ lại. Còn ethene không phản ứng thoát ra ngoài.
CH≡CH + 2AgNO3 + 2NH3 → AgC≡CAg + 2NH4NO3
Tên gọi 3-ethyl-4-methylhex-1-yne ứng với cấu tạo nào sau đây?
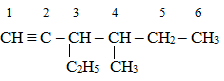
3-ethyl-4-methylhex-1-yne
Chất nào sau đây thuộc dãy đồng đẳng alkene?
Công thức chung của dãy đồng đẳng alkene là
CnH2n (n ≥ 2)
Vậy đồng đẳng alkene là C4H8
Cho 2 – methylbut – 2 – ene tác dụng với hydrogen chloride công thức cấu tạo sản phẩm chính của các phản ứng trên là:
2 – methylbut – 2 – ene có công thức cấu tạo là: CH3 – C(CH3) = CH – CH3
Sản phẩm chính thu được khi cho 2 – methylbut – 2 – ene tác dụng với hydrogen chloride là:
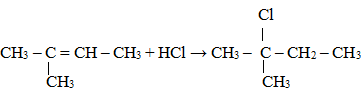
Chất không phản ứng với dung dịch AgNO3/NH3 dư là
Chất không phản ứng được với AgNO3/NH3 là: pent-2-yne (CH3 – C ≡ C – CH3).
Chỉ các alk – 1 – in (các alkyne có liên kết ba đầu mạch) mới tác dụng với AgNO3/ NH3 tạo kết tủa.
Nhận định nào dưới đây không đúng?
Nhận định không đúng là:
Toluene không thể tác dụng với dung dịch KMnO4 ngay khi ở nhiệt độ cao
vì:
Toluene có thể tác dụng với dung dịch KMnO4 ngay khi ở nhiệt độ cao
Phương trình phản ứng:
C6H5CH3 + 2KMnO4 C6H5COOK + KOH + 2MnO2 + H2O
Số đồng phân alkyne có công thức phân tử C5H8 là
Các đồng phân của C5H8 là
CH≡C−CH2−CH2−CH3
CH3−C≡C−CH2−CH3
CH≡C−CH(CH3)−CH3
⇒ Có 3 đồng phân
Benzene là một hydrocarbon thơm đơn giản và điển hình nhất, trong vòng benzene có chứa mấy liên kết đôi:
Vòng benzen có chứa 3 liên kết đôi
Hỗn hợp X gồm propyne và một alkyne Y có tỉ lệ mol 1:1. Lấy 0,15 mol X tác dụng với dung dịch AgNO3/NH3 dư thu được 23,1 gam kết tủa. Tên gọi alkyne Y là
npropyne = nalkyne = 0,075 mol
Phương trình phản ứng
C3H4 + AgNO3 + NH3 → C3H3Ag + NH4NO3
0,075 → 0,075
⇒ mC3H3Ag = 0,075.147 = 11,025 gam
⇒ Y cũng tạo kết tủa với AgNO3/NH3
CnH2n-2 → CnH2n-2-aAga
0,075 → 0,075
mCnH2n-2-aAga = 23,1 - 11,025 = 12,075
nCnH2n-2-aAga= 12,075:0,075 = 161
⇒ Y chứa tối đa 1 liên kết ba đầu mạch ⇒ a = 1
⇒ 14n – 2 + 107 = 161 ⇒ n = 4
Vậy công thức cấu tạo của Y:
CH≡C-CH2-CH3: but - 1 - yne
Cho 4 chất: methane, ethane, propane và butane. Số chất khí ở điều kiện thường là
Ở điều kiện thường, các alkane từ C1 và đến C4 và neophentan ở thế khí, các alkane có nhiều nguyên tử carbon hơn ở thể lỏng hoặc rắn.
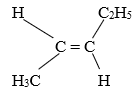
Chất nào sau đây có đồng phân hình học:
Chất có đồng phân hình học là: CH3 – CH = CH – CH3
Nhận định nào sau đây không đúng khi nói về Toluene?
Toluene là đồng đẳng của benzene
Phản ứng đặc trưng của hydrocarbon không no là phản ứng
Phản ứng đặc trưng của các hydrocarbon không no là phản ứng cộng.
Hỗn hợp X gồm acetylene, ethylene và hydrogen có tỉ khối so với H2 là 7,25. Đốt cháy hoàn toàn 0,1 mol hỗn hợp X thu được 0,1 mol CO2. Phần trăm thể tích của acetylene trong hỗn hợp X là
Gọi x, y, z lần lượt là số mol của C2H2, C2H4 và H2.
⇒ x + y + z = 0,1 (1)
Áp dụng bảo toàn nguyên tố C:
nCO2 = 2.nC2H2 + 2.nC2H4
⇒ 2x + 2y = 0,1 (3)
Giải hệ phương trình (1), (2), (3) ⇒ x = 0,025; y = 0,025; z = 0,05
%VC2H2 = 25%.
Tên gọi của hợp chất (CH3)2CH–C6H5 là:
Tên gọi của hợp chất (CH3)2CH–C6H5 là: iso-propylbenzene
Đốt cháy hoàn toàn một alkyne X ở thể khí thu được sản phẩm cháy gồm CO2 và H2O có tổng khối lượng là 34,5 gam. Nếu cho sản phẩm cháy đi qua dung dịch Ca(OH)2 dư thì thu được 60 gam kết tủa. Xác định công thức phân tử của X:
nCaCO3 = 60:100 = 0,6 mol
Áp dụng bảo toàn nguyên tố C:
nCO2 = nCaCO3 = 0,6 mol
Gọi công thức của ankin là CnH2n-2 (n ≥ 2)
Phương trình phản ứng hóa học:
Ta có: mCO2 + mH2O = 34,5
⇒ mH2O = 34,5 - 0,6.44 = 8,1 gam
⇒ nH2O = 8,1:18 = 0,45 mol
Ta có: nCnH2n-2 = nCO2 - nH2O = 0,6 - 0,45 = 0,15 mol
Công thức cần tìm là C4H6.
Hydrocarbon X có công thức phân tử là C5H8 có thể cộng hợp với hydrogen tạo ra alkane mạch nhánh và A có thể tác dụng với AgNO3/NH3 tạo ra kết tủa màu vàng. Hydrocarbon X có tên gọi là:
Hydrocarbon X có công thức phân tử là C5H8 có thể cộng hợp với hydrogen tạo ra alkane mạch nhánh và A có thể tác dụng với AgNO3/NH3 tạo ra kết tủa màu vàng chắc phải là alkyne có nối ba đầu mạch và phân nhánh:
Ta có C5H8 có 3 đồng phân alkyne
CH≡C−CH2−CH2−CH3: loại vì không phân nhánh
CH3−C≡C−CH2−CH3: loại vì không có nối 3 đầu mạch và không phân nhánh.
CH≡C−CH(CH3)−CH3: thỏa mãn.
Cho 2 – methylbutane tác dụng với chlorine trong điều kiện chiếu sáng thu được tối đa bao nhiêu đồng phân cấu tạo dẫn xuất monochloro?
2 – methylbutane có công thức:
CH3– CH(CH3) – CH2 – CH3
Cho 2 – methylbutane tác dụng với chlorine trong điều kiện chiếu sáng thu được tối đa 4 dẫn xuất monochloro là:
CH2Cl – CH(CH3) – CH2 – CH3;
CH3 – CCl(CH3) – CH2 – CH3;
CH3 – CH(CH3) – CHCl – CH3;
CH3 – CH(CH3) – CH2 – CH2Cl.
Chất nào không phải là đồng đẳng của benzene:
Benzene và các đồng đẳng của nó hợp thành dẫy đồng đẳng của benzene có công thức chung là: CnH2n-6 (n ≥ 6).
Vậy chất không phải là đồng đẳng của benzene là: C6H5–C2H3 không phải vì nhánh –C2H3 không no
Cho các chất sau: methane (1); ethylene (2); acetylene (3); benzene (4); styrene (5); toluene (6). Các chất có khả năng làm mất màu dung dịch KMnO4 ở điều kiện thích hợp là
Các chất có khả năng làm mất màu dung dịch KMnO4 ở điều kiện thích hợp là: ethylene (2); acetylene (3); styrene (5); toluene (6).
Dùng nước bromine làm thuốc thử có thể phân biệt cặp chất nào dưới đây?
Vậy ta có thể dùng nước bromine để phân biệt toluene và styrene:
Styrene làm mất màu nước bromine ngay ở điều kiện thường.
Phương trình phản ứng hóa học
C6H5-CH = CH2 + Br2 → C6H5-CHBr-CH2Br
Toluene không làm mất màu nước bromine.
Chất nào sau đây làm mất màu dung dịch Bromine?
But-1-ene làm mất màu dung dịch Bromine
Tiến hành thí nghiệm sau: Dẫn từ từ C2H4 vào dung dịch KMnO4 hiện tượng quan sát được là
Dẫn từ từ C2H4 vào dung dịch KMnO4 hiện tượng quan sát được là Có vẩn đục màu đen
3C2H4 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2MnO2 + 2KOH.
