Giả sử khi kết thúc chuẩn độ, thể tích dung dịch NaOH (tính trung bình sau 3 lần chuẩn độ) đã sử dụng ở burette là 10,27 mL. Tính nồng độ của dung dịch NaOH.
NaOH + HCl → NaCl + H2O
Ta có: VHCl. CHCl = VNaOH. CNaOH
Giả sử khi kết thúc chuẩn độ, thể tích dung dịch NaOH (tính trung bình sau 3 lần chuẩn độ) đã sử dụng ở burette là 10,27 mL. Tính nồng độ của dung dịch NaOH.
NaOH + HCl → NaCl + H2O
Ta có: VHCl. CHCl = VNaOH. CNaOH
Một phản ứng thuận nghịch A(g) + B(g) ⇋ C(g) + D(g). Người ta trộn bốn chất A, B, C, D. mỗi chất 1mol vào bình kín có thể tích V không đổi. Khi cân bằng được thiết lập, lượng chất C trong bình là 1,5 mol. Hằng số cân bằng KC có giá trị là
A(g) + B(g) ⇋ C(g) + D(g)
Ban đầu (M): 1 1 1 1
Phản ứng (M): x x x x
Cân bằng (M): 1 – x 1 – x 1 + x 1 + x
Khi cân bằng được thiết lập [C] = 1,5 (M) 1 + x = 1,5
x = 0,5 (M)
Vậy tại thời điểm cân bằng: [A] = [B] = 1 – x = 1 – 0,5 = 0,5 (M); [C] = 1 + x = 1,5(M)
Hằng số cân bằng:
Đâu không phải nguyên nhân chính gây ra mưa acid
Hoạt động quang hợp của cây không phải nguyên nhân chính gây ra mưa acid.
Cho ba dung dịch có cùng giá trị pH, các dung dịch được sắp xếp theo thứ tự nồng độ mol tăng dần là:
pH bằng nhau => nồng độ mol ion OH- trong các dung dịch bằng nhau
Phương trình phân li:
Ba(OH)2 → 2OH-
NaOH → OH-
NH3 + H2O→ NH4+ + OH-
Mà [OH-] bằng nhau => [Ba(OH)2] < [NaOH] < [NH3].
Công thức hóa học của chất mà khi điện li tạo ra ion Al3+ và SO42- là
Công thức hóa học của chất mà khi điện li tạo ra ion Al3+ và SO42- là Al2(SO4)3.
Trộn V1 lít dung dịch H2SO4 có pH = 3 với V2 lít dung dịch NaOH có pH = 12, thu được dung dịch mới có pH = 4. Tỉ số V1 : V2 có giá trị là
Sau phản ứng ta có: Vdung dịch = V1 + V2 (lít)
- Ban đầu dung dịch H2SO4 có pH = 3
⇒ [H+] = 10-3 ⇒ nH2SO4 = 5.10− 4V1 (mol)
- Dung dịch NaOH có pH = 12
Dung dịch mới thu được có pH = 4 < 7 ⇒ Acid dư
Phương trình phản ứng xảy ra:
2NaOH + H2SO4 → Na2SO4 + 2H2O
0,01V2 → 5.10-3V2 (mol)
Sau phản ứng nồng độ H+ là:
Ở -196oC, nitrogen tồn tại ở dạng nào?
Ở -200oC, nitrogen tồn tại ở dạng lỏng
Ở nhiệt độ nhất định, khí ammonia (NH3) và khí hydrogen chloride (HCl) sẽ phản ứng với nhau để tạo thành chất rắn ammonium chloride (NH4Cl). Cũng tại điều kiện đó, một phần sản phẩm sẽ phân hủy để tạo thành những hợp chất ban đầu. Phương trình hóa học nào sau đây mô tả quá trình diễn ra bên trên?
Phương trình hóa học mô tả quá trình diễn ra là:
NH3(g) + HCl(g) NH4Cl(s).
Số oxi hóa và hoá trị của nitrogen trong hợp chất nitric acid lần lượt là:
Công thức cấu tạo của HNO3 là:

Đặt số oxi hóa của N trong phân tử HNO3 là x
Trong hơp chất, số oxi hóa của H và O là: +1 và -2.
Ta có: +1 + x + (-2.3) = 0 ⇒ x = 5
HNO3 có số oxi hóa là +5 và hóa trị IV
Trung hòa 200 g dung dịch NaOH 10% bằng dung dịch HCl 3,65%. Khối lượng dung dịch HCl cần dùng là:
Phương trình phản ứng trung hòa:
NaOH + HCl → NaCl + H2O
0,5 → 0,5
Thổi tử từ NH3 đến dư vào 400 gam dung dịch CuCl2 6,75%. Khi lượng kết tủa thu được cực đại thì thể tích NH3 (đkc) đã dùng là:
mCuCl2 = (400 . 6,75) : 100 = 27 gam
nCuCl2 = 27 : 135 = 0,2 mol
Phương trình phản ứng:
CuCl2 + 2NH3 + 2H2O → Cu(OH)2 + 2NH4Cl (1)
0,2 → 0,4 (mol)
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2.
Khi lượng kết tủa cực địa thì chỉ xảy ra phản ứng (1)
Nên theo phương trình phản ứng (1) ta có:
nNH3 = 2.nCuCl2 = 0,2.2 = 0,4 mol
→ VNH3 = 0,4.24,79 = 9,916 lít.
Cho các cân bằng sau:
(1) 2SO2 (g) + O 2 (g) ⇌ 2SO 3 (g)
(2) CO (g) + H2O (g) ⇌ H2 (g) + CO2 (g).
(3) H2 (g) + I2 (g) ⇌ 2HI (g)
(4) CaCO3(s) ⇌ CaO(s) + CO2(g)
Nếu tăng áp suất và giữ nguyên nhiệt độ, số cân bằng trên không bị chuyển dịch là:
a) 2SO2(g) + O2(g) ⇌ 2SO3(g)
Nếu tăng áp suất và giữ nguyên nhiệt độ, cân bằng sẽ chuyển dịch theo chiều thuận, tức chiều làm giảm áp suất (hay chiều làm giảm số mol khí).
b) CO(g) + H2O(g) ⇌ H2(g) + CO2(g)
c) H2(g) + I2(g) ⇌ 2HI(g)
Nếu tăng áp suất và giữ nguyên nhiệt độ, cân bằng sẽ không chuyển dịch, do đối với phản ứng thuận nghịch có tổng hệ số tỉ lượng của các chất khí ở hai vế của phương trình hoá học bằng nhau thì trạng thái cân bằng của hệ không bị chuyển dịch khi thay đổi áp suất chung của hệ.
(d) CaCO3(s) ⇌ CaO(s) + CO2 (g)
Nếu tăng áp suất và giữ nguyên nhiệt độ, cân bằng sẽ chuyển dịch theo chiều nghịch , tức chiều làm giảm áp suất (hay chiều làm giảm số mol khí).
Nhiệt phân hoàn toàn hỗn hợp muối NH4HCO3 và (NH4)2CO3, thu được hỗn hợp khí và hơi trong đó CO2 chiếm 30% về thể tích. Tỉ lệ số mol tương ứng của NH4HCO3 và(NH4)2CO3 là
Gọi số mol tương ứng của NH4HCO3 và(NH4)2CO3 là x và y.
Sơ đồ phản ứng:
nCO2 = 30%.n(NH3, CO2, H2O)
Trong các chất sau, chất nào là chất điện li yếu?
Chất điện lí yếu là chất khi tan trong nước chỉ có một phần số phân tử chất tan phân li ra ion, phần còn lại vẫn tồn tại ở dạng phân tử trong dung dịch.
Những chất điện li yếu gồm các acid yếu như CH3COOH, HClO, HF, ... và các base yếu như Cu(OH)2, Fe(OH)3,...
Trong phương trình sau: CH3COOH + H2O ⇌ CH3COO– + H3O+. Theo phản ứng nghịch, ion hay chất nào đóng vai trò base.
Theo phản ứng nghịch CH3COO- có khả năng nhận proton (H+) nên là base.
Tính phân tử khối trung bình của không khí, giả thiết thành phần không khí: 78% nitrogen, 21% oxygen và 1% argon.
= 28,014.0,78 + 31,998.0,21 + 39,948.0,01 = 28,970.
pH của dung dịch nào sau đây có giá trị nhỏ nhất?
Giá trị pH được thể hiện ở bảng sau
|
Dung dịch |
HCl 0,1 M |
CH3COOH 0,1 M |
NaCl 0,1 M |
NaOH 0,01 M |
|
pH |
1 |
> 1 |
7 |
12 |
Phát biểu nào sau đây không phải ảnh hưởng của hiện tượng phú dưỡng
Phát biểu không phải ảnh hưởng của hiện tượng phú dưỡng là:
Làm chất lượng nước tốt hơn.
Cặp kim loại nào sau đây không phản ứng với HNO3 đặc nguội?
Al, Fe là hai kim loại bị thụ động trong nitric acid đặc nguội.
Phân tử nào sau đây có chứa một liên kết cho - nhận?
Trong phân tử HNO3, liên kết O − H phân cực mạnh về phía nguyên tử oxygen, liên kết N → O là liên kết cho – nhận.

Xét cân bằng hóa học: N2(g) + 3H2(g) ⇌ 2NH3(g) ∆H < 0
Hiệu suất phản ứng khi hệ đạt cân bằng ở nhiệt độ 400oC và 500oC lần lượt bằng x% và y%. Mối quan hệ giữa x và y là
Nhiệt độ càng cao cân bằng càng chuyển dịch theo chiều làm giảm nhiệt độ, tức là chiều nghịch. Vậy hiệu suất của phản ứng tại nhiệt độ thấp là cao hơn nhiệt độ cao.
Oxi hóa 6 lít NH3 (tạo ra N2 và NO theo tỉ lệ mol 1 : 4) cần vừa đủ V lít không khí (chứa 20% oxygen về thể tích). Các thể tích đó ở cùng điều kiện. Giá trị của V là
Phương trình phản ứng:
12NH3 + 13O2 8NO + 2N2 + 18H2O
Vkk = 6,5:20% = 32,5 lít
Cân bằng hoá học là cân bằng động, do khi ở trạng thái cân bằng
Cân bằng hóa học là một cân bằng động vì tại trạng thái cân bằng, phản ứng thuận và phản ứng nghịc vẫn xảy ra, nhưng với tốc độ bằng nhau.
Cho một ít tinh thể muối X vào ống nghiệm và đun nóng trên ngon lửa đèn cồn, sau một thời gian thấy không còn chất rắn nào ở đáy ống nghiệm. Muối X có thể là muối nào sau đây?
NaCl không bị nhiệt phân phân.
CaCO3 CaO + CO2
2KClO3 2KCl + 3O2
NH4Cl → NH3 + HCl
Nhiệt phân NH4Cl tạo thành các sản phẩm khí là khí NH3 và khí HCl.
Nên đáp án đúng mà muối NH4Cl
Phát biểu nào sau đây về đơn chất nitrogen (N2) là không đúng?
Phân tử N2 không hoạt động hóa học tốt hơn Cl2 do năng lượng liên kết của N2 rất lớn lớn hơn nhiều so với Cl2.
Cho 100 mL dung dịch NaOH 0,1M vào cốc được 150 mL dung dịch HCl 0,1M. Dung dịch sau phản ứng làm cho
nNaOH = 0,1.0,1 = 0,01 mol.
nHCl = 0,15.0,1 = 0,015 mol.
NaOH + HCl → NaCl + H2O
Dựa vào tỉ lệ mol phản ứng
nNaOH < nHCl sau phản ứng dung dịch chứa HCl dư ⇒ Dung dịch tạo thành sẽ làm cho giấy quỳ tím hóa đỏ.
Trong y học, vì sao nitrogen lỏng được dùng để bảo quản mẫu vật?
Ứng dụng của nitrogen trong y học để bảo quản mẫu vật là do nitrogen hóa lỏng ở nhiệt độ thấp.
Trong quá trình tổng hợp ammonia theo quy trình Haber, khi đạt trạng thái cân bằng, hỗn hợp khí sẽ được:
Thời điểm cân bằng, nồng độ cả chất phản ứng và chất sản phẩm không đổi, hỗn hợp được qua hệ thống làm lạnh để hóa lỏng ammonia
Chất nào sau đây là acid?
Theo thuyết Br∅nsted - Lowry cho rằng acid là chất cho proton (H+)
⇒ HCl chính acid:
HCl + H2O → Cl- + H3O+
Phản ứng nào sau đây là phản ứng thuận nghịch?
Phản ứng thuận nghịch được biểu diễn bằng mũi tên hai chiều:
3H2 + N2 2NH3.
Dãy nào sau đây đều gồm các chất điện li mạnh?
Chất điện li mạnh là chất khi tan trong nước, hầu hết các phân tử chất tan đều phân li ra ion.
Các chất điện li mạnh thường gặp là:
Các acid mạnh: HCl, HNO3, ...
Các base mạnh: NaOH, KOH, Ca(OH)2,...
Hầu hết các muối.
⇒ Dãy gồm chất điện li mạnh là: KOH, CH3COONa, HCl, MgSO4, K2CO3.
Chất nào không là chất điện li?
CH3OH không phải chất điện li.
Hoà tan hết 9,4 gam hỗn hợp Fe; FeO; Fe3O4; Fe2O3 trong dung dịch HNO3 đặc nóng dư được 1,85925 lít khí NO2 (đkc), sản phẩm khử duy nhất) và dung dịch Y. Cô cạn dung dịch Y được m gam muối. Giá trị của m là
Quy đổi hỗn hợp thành ta có theo đề bài
56x + 16y = 9,4 (1)
nNO2 = 1,85925 : 24,79 = 0,075 mol
Quá trình nhường nhận electron.
Fe0 → Fe+3 + 3e x → 3x | N+5 + 1e → N+4 0,075 ← 0,075 O0 + 2e → O-2 y → 2y |
Áp dụng định luật bảo toàn electron ta có:
3x - 2y = 0,075 (2)
Giải hệ phương trình (1) và (2) ta có:
x = 0,125 mol; y = 0,15 mol
Ta có: nNO3- = 3nFe = 0,375 mol
⇒ mFe(NO3)3 = mFe + mNO3- = 0,125.56 + 0,375.62 = 30,25 (gam)
Phân biệt được dung dịch NH4Cl và KCl bằng thuốc thử là dung dịch
Khi cho NaOH tác dụng với NH4Cl và KCl, với NH4Cl có hiện tượng là có khí mùi khai thoát ra, còn NaCl không có hiện tượng gì.
NaOH + NH4Cl → NaCl + NH3 + H2O
Yếu tố nào sau đây không ảnh hưởng đến cân bằng hóa học?
(a) nồng độ.
(b) nhiệt độ.
(c) chất xúc tác.
(d) áp suất.
(e) diện tích bề mặt.
Yếu tố không ảnh hưởng đến cân bằng hóa học là chất xúc tác, diện tích bề mặt.
Phương trình điện li viết đúng là
Phương trình điện li viết đúng là: KOH → K+ + OH-
CuSO4 khi phân li trong nước tạo thành 2 ion là: Cu2+ và SO42-.
CH3OH là chất không điện li.
CH3COOH là acid yếu, phân li không hoàn toàn trong nước, khi biểu diễn phương trình điện li sử dụng mũi tên "".
Dẫn 4,985 lít khí HCl (đkc) vào 2 lít nước thu được 2 lít dung dịch có pH là
⇒ pH = 1.
Cho sơ đồ phản ứng sau:
![]()
Mỗi mũi tên là một phản ứng hóa học. Số phản ứng mà nitrogen đóng vai trò chất khử là
Chất khử là chất cho electron, tức là số oxi hóa tăng.
Các phản ứng N đóng vai trò chất khử là (2), (3), (4).
Pha loãng dung dịch KOH có pH = 13 bao nhiêu lần để được dung dịch có pH = 11?
Gọi V, V’ lần lượt là thể tích dung dịch KOH trước và sau pha loãng.
Trước khi pha loãng có pH = 13
pOH = 1
[OH−] = 10−1 M
nOH− = 10−1V (mol)
Sau khi pha loãng có pH = 11
pOH = 3
[OH−] = 10−3
nOH− = 10−3V' (mol)
Mà số mol OH− không đổi
10−1V = 10−3V'
V'= 100V
Cần pha loãng gấp 100 lần.
Hình ảnh dưới đây mô tả phương pháp nào trong hóa học?
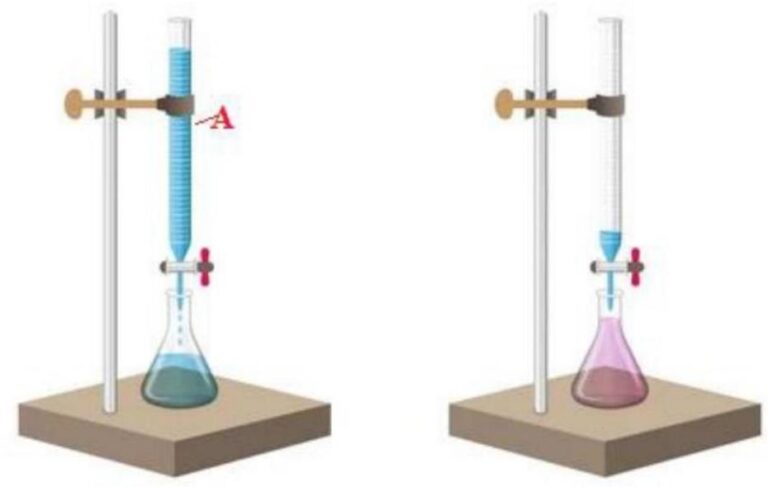
Hình ảnh mô tả phương pháp chuẩn độ trong hóa học.
