Trộn 200 mL dung dịch HCl 0,05M với 200 mL dung dịch H2SO4 0,075M thu được dung dịch có pH bằng
nHCl = 0,2.0,05 = 0,01 mol
nH2SO4 = 0,2.0,075 = 0,015 mol
⇒ nH+ = nHCl + 2nH2SO4 = 0,01 + 2.0,015 = 0,04 mol.
⇒ pH = -log 0,1 = 1.
Trộn 200 mL dung dịch HCl 0,05M với 200 mL dung dịch H2SO4 0,075M thu được dung dịch có pH bằng
nHCl = 0,2.0,05 = 0,01 mol
nH2SO4 = 0,2.0,075 = 0,015 mol
⇒ nH+ = nHCl + 2nH2SO4 = 0,01 + 2.0,015 = 0,04 mol.
⇒ pH = -log 0,1 = 1.
Môi trường base có pH:
Môi trường base có pH lớn hớn 7.
Cho NH3 dư vào 100 ml dung dịch gồm CuSO4 1M ; ZnCl2 0,5M và AlCl3 1M. Khối lượng kết tủa sau phản ứng là
Vì các ion Cu2+, Zn2+, tạo kết tủa với NH3, sau đó kết tủa tan trong NH3 dư tạo phức Cu(NH3)4(OH)2; Zn(NH3)4(OH)2 .
⇒ Kết tủa thu được chỉ gồm Al(OH)3
3NH3 + AlCl3 + 3H2O → Al(OH)3 ↓ + 3NH4Cl
0,1 → 0,1 mol
nAl(OH)3 = nAlCl3 = 0,05 mol
⇒ m = 0,1 . 78 = 3,9 gam.
Trong phản ứng tổng hợp ammonia từ nitrogen và hydrogen, nitrogen đóng vai trò là:
Phương trình hoá học tổng hợp ammonia:
N2 + 3H2 ⇌ 2NH3.
N2 có số oxi hoá là 0. Phản ứng trong hợp chất NH3 nguyên tử N có số oxi hoá là −3.
Vậy số oxi hoá của N giảm nên N2 có vai trò là chất oxi hoá.
Theo thuyết Brønsted-Lowry về acid - base, những chất có khả năng nhận proton là:
Theo thuyết Brønsted-Lowry về acid - base, những chất có khả năng cho proton (H+) là acid và base là chất nhận proton
Nhận định nào sau đây đúng?
Phản ứng nhiệt phân NH4NO3 là phản ứng tự oxi hóa, khử.
N-3H4N+5O3 N-12O + 2H2O
Thể tích không khí (đkc) cần lấy để sản xuất được 1,00 tấn dung dịch NH3 34,0% là bao nhiêu? Biết trong không khí N2 chiếm 80% và hiệu suất quá trình sản xuất là 30,0%.
N2(g) + 3H2(g) 2NH3(g)
mol: 10000 ← 20000
Do hiệu suất quá trình phản ứng là 30% nên:
mol
mol
Phát biểu nào đúng khi một hệ ở trạng thái cân bằng?
Khi một hệ ở trạng thái cân bằng nồng độ của các chất trong hệ không đổi.
Ở trạng thái cơ bản, nguyên tố nitrogen có bao nhiêu electron độc thân?
Cấu hình theo ô orbital của nitrogen là:
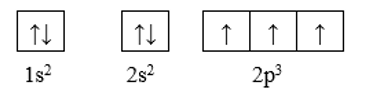
Như vậy, ở trạng thái cơ bản nguyên tử nitrogen có 3 electron độc thân.
Chất nào sau đây không phải chất điện li trong nước?
C6H12O6 không phải chất điện li vì khi tan trong nước không phân li ra các ion.
Nitric acid không có khả năng ăn mòn:
Nitric acid không có khả năng ăn mòn Pt.
Cho 15,3 gam hỗn hợp Cu, Fe, Zn tác dụng với dung dịch HNO3 loãng dư thu được dung dịch chứa 46,3 gam muối khan (không chứa muối ammonium). Nung hỗn hợp muối đến khối lượng không đổi, thu được m gam rắn. Giá trị của m là
Sơ đồ phản ứng:
mNO3- = 46,3 - 15,3 = 31 gam.
⇒ nNO3- = 31 : 62 = 0,5 mol.
Bảo toàn điện tích ta có:
⇒ nO2- = = 0,25 mol
⇒ m = mKL + mO2-
⇒ m = 15,3 + 0,25.16 = 19,3 gam.
Dung dịch chuẩn là gì?
Dung dịch chuẩn là những dung dịch đã biết nồng độ chính xác, thường dùng để xác định nồng độ các dung dịch khác.
Phú dưỡng là hiện tượng ao hồ dư thừa quá nhiều các nguyên tố dinh dưỡng nào sau đây?
Phú dưỡng là hiện tượng ao, hồ dư quá nhiều các nguyên tố dinh dưỡng (nitrogen, phosphorus).
Cho các chất: H2CO3, HCl, CH3COOH, HNO3, HF, HNO2, KNO3, HgCl2, H2S, Ba(OH)2. Số chất thuộc loại điện li yếu là
Chất điện lí yếu là chất khi tan trong nước chỉ có một phần số phân tử chất tan phân li ra ion, phần còn lại vẫn tồn tại ở dạng phân tử trong dung dịch.
Những chất điện li yếu gồm các acid yếu như CH3COOH, HClO, HF, ... và các base yếu như Cu(OH)2, Fe(OH)3,...
Số chất thuộc loại điện li yếu là H2CO3, CH3COOH, HF, HNO2, HgCl2, H2S.
Trong các hợp chất hóa học sau hợp chất nào nitrogen có số oxi hóa thấp nhất?
Số oxi hóa của N trong các hợp chất là:
N-3H4Cl.
N02.
HN+5O3.
N+4O2.
Thêm nước vào 100 mL dung dịch NaOH 1,0 mol/L, thu được 10000 mL dung dịch A. Dung dịch A có pH thay đổi như thế nào so với dung dịch ban đầu?
Khi tăng thể tích lên 100 lần thì nồng độ ion OH- trong dung dịch giảm 100 lần
nồng độ H+ tăng 100 lần pH = -log[H+] pH giảm 2 lần.
Chất nào sau đây thuộc loại chất điện li mạnh?
Chất điện li mạnh là chất khi tan trong nước, hầu hết các phân tử chất tan đều phân li ra ion.
Chất điện li mạnh là HCl. Phương trình điện li minh họa
HCl → H+ + Cl−
Cho phản ứng hóa học sau: Br2 (g) + H2 (g) ![]() 2HBr (g)
2HBr (g)
Biểu thức hằng số cân bằng (KC) của phản ứng trên là:
Phản ứng hóa học sau: Br2 (g) + H2 (g) 2HBr (g)
Biểu thức hằng số cân bằng (KC)
Chuẩn độ 10 ml dung dịch NaOH 0,2M bằng dung dịch HCl 0,1 M tại điểm tương đương thể tích dung dịch HCl là bao nhiêu?
Phương trình phản ứng:
NaOH + HCl → NaCl + H2O
Ta có: nHCl = nNaOH
Chất nào sau đây có tính lưỡng tính?
Hydroxide lương tính có thể phân li theo kiểu acid hoặc base
Chất nào sau đây có tính lưỡng tính là Al(OH)3.
Có thể dùng chất nào dưới đây để trung hòa ammonia?
Dung dịch ammonia có môi trường base yếu do đó ta dùng giấm ăn có tính acid để trung hòa.
Mệnh đề nào sau đây không đúng?
Để điều chế khí NH3 trong công nghiệp bằng cách tổng hợp từ khí nitrogen và khí hydrogen
N2 + 3H2 2NH3
Dựa vào thuyết acid-base của Brønsted-Lowry, xác định cặp base trong phản ứng sau:
(CH3)2NH + H2O ![]() (CH3)2NH2+ + OH-
(CH3)2NH2+ + OH-
Phản ứng thuận: H2O là acid, (CH3)2NH là base; phản ứng nghịch: (CH3)2NH2+ là acid, OH- là base.
Để điều chế 5 lít dung dịch HNO3 21% (D = 1,2g/ml) bằng phương pháp oxi hóa NH3 với hiệu suất toàn quá trình là 80%, thể tích khí NH3 (đkc) tối thiểu cần dùng là
Bảo toàn nguyên tố N:
nNH3 = nHNO3 = = 20 mol
H = 80% ⇒ VNH3 = = 560 lít
Dẫn từ từ 2,479 lít khí NH3 qua ống sứ chứa CuO dư nung nóng. Sau phản ứng hòa tan chất rắn trong ống sứ vào dung dịch HNO3 loãng, dư thu được 1,4874 lít NO (các khí đo ở đkc). Lượng NH3 đã tham gia phản ứng khử CuO là
nNH3 bđ = 0,1 mol
nNO = 0,06 mol
2NH3 + 3CuO 3Cu + N2 + 3H2O
x 1,5x
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
1,5x → x
x = 0,06 mol
Lượng NH3 đã tham gia phản ứng khử CuO là:
Đặc điểm nào sau đây là không đúng khi mô tả về acid mạnh?
Acid là những chất có khả năng cho H+.
Phân li hoàn toàn trong nước.
Dung dịch nước của chúng dẫn điện.
Ứng dụng tính chất nào của khí nitrogen mà được sử dụng để làm hệ thống chữa cháy?
Trong chữa cháy, nitrogen dùng để dập tắt các đám chát do hóa chất, chập điện do tính trơ của nitrogen.
Khí nào sau đây có mùi khai, xốc?
Khí NH3 có mùi khai, xốc.
Trong một bình kín chứa 10 lít nitrogen và 10 lít hydrogen ở nhiệt độ 0oC và 10atm. Sau phản ứng tổng hợp NH3, lại đưa bình về 0oC. Biết rằng có 60% hydrogen tham gia phản ứng, áp suất trong bình sau phản ứng là:
Thể tích H2 phản ứng là:
VH2 = 10.60% = 6 lít.
Phương trình phản ứng hóa học
| N2 + | 3H2 | 2NH3 | ||
| Ban đầu | 10 | 10 | 0 (lít) | |
| Phản ứng | 2 | 6 | 4 (lít) | |
| Sau phản ứng | 8 | 4 | 4 (lít) |
Nhận định nào sau đây không đúng với về mưa acid?
Nhận định nào sau đây không đúng?
Phản ứng 1 chiều là phản ứng xảy ra hoàn toàn.
Cho cân bằng hóa học: 2SO2(g) + O2(g) ![]() 2SO3(l) ΔrHo298 < 0. Khi giảm nhiệt độ và khi giảm áp suất thì cân bằng của phản ứng trên chuyển dịch tương ứng là:
2SO3(l) ΔrHo298 < 0. Khi giảm nhiệt độ và khi giảm áp suất thì cân bằng của phản ứng trên chuyển dịch tương ứng là:
Đây là phản ứng tỏa nhiệt, nên khi giảm nhiệt độ cân bằng phản ứng sẽ chuyển dịch theo chiều thuận.
Vì tổng số mol khí lúc trước phản ứng lớn hơn tổng số mol khí sau khi phản ứng nên khi giảm áp suất cân bằng sẽ chuyển dịch theo chiều nghịch.
Nước cường toan là hỗn hợp của HNO3 đặc và HCl đặc có tỉ lệ thể tích lần lượt là:
Nước cường toan là hỗn hợp của HNO3 đặc và HCl đặc có tỉ lệ thể tích 1 : 3.
Trong các phản ứng dưới đây, ở phản ứng nào nước đóng vai trò là một base?
HCl + H2O → H3O+ + Cl-
H2O nhận proton (H+) là base.
NH3 + H2O NH4+ + OH-.
H2O là acid.
O32- + H2O ⇌ HCO3- + OH-.
H2O là acid.
Cho 100 gam dung dịch NH4HSO4 11,5% vào 100 gam dung dịch Ba(OH)2 13,68% và đun nhẹ. Thể tích khí (đkc) và khối lượng kết tủa thu được là
nNH4HSO4 = (100.11,5%)/115 = 0,1
nBa(OH)2 = (100.13,68%)/171 = 0,08
Phương trình phản ứng:
NH4HSO4 + Ba(OH)2 → BaSO4↓ + NH3↑ + 2H2O
Vì nNH4HSO4 > nBa(OH)2 ⇒ NH4HSO4 còn dư
nBaSO4 = nBa(OH)2 = 0,08 mol ⇒ mBaSO4 = 0,08.233 = 18,64 gam
VNH3 = 0,08.24,79 = 1,9832 lít
Thể tích dung dịch HCl 0,3M cần để trung hòa 200 ml dung dịch hỗn hợp NaOH 0,1M và Ba(OH)2 0,1M là
nNaOH = 0,2.0,1 = 0,02 mol;
nBa(OH)2 = 0,2.0,1 = 0,02 mol
→ nOH− = nNaOH + 2nBa(OH)2 = 0,02 + 2.0,02 = 0,06 mol
Phương trình hóa học
H+ + OH−→ H2O
Theo phương trình:
nH+ = nOH− = 0,06 mol
Ta có:
nHCl = nH+ = 0,06 mol
→VHCl= 0,06 : 0,3 = 0,2 lít = 200 ml
Đối với dung dịch acid yếu CH3COOH 0,10 M, nếu bỏ qua sự điện li của nước thì đánh giá nào về nồng độ mol ion sau đây là đúng?
CH3COOH là acid yếu nên là chất điện li yếu, trong nước không phân li hoàn toàn:
CH3COOH CH3COO- + H+
[H+] = [CH3COO-] < 0,10.
Phản ứng tạo hydrogen iodide xảy ra như sau: H2(g) + I2(g) ⇋ 2HI(g). Tại thời điểm cân bằng, nồng độ các chất thu được lần lượt là: [H2] = 0,105M; [HI] = 0,315; [I2] = 0,12. Biết nhiệt độ không đổi. Giá trị hằng số cân bằng KC của phản ứng là?
Hằng số cân bằng KC của phản ứng là:
Chất nào sau đây là acid?
Thuyết Br∅nsted - Lowry cho rằng acid là chất cho proton (H+)
CH3COOH + H2O CH3COO- + H3O+
