Arene (Hydrocarbon thơm)
I. Khái niệm và danh pháp
1. Khái niệm
Arene hay còn gọi là hydrocarbon thơm là những hydrocarbon trong phân tử có chứa một hay nhiều vòng benzene.
Benzene có công thức C6H6 là một hydrocarbon thơm đơn giản và điển hình nhất.
Benzene và các đồng đẳng của nó hợp thành dãy đồng đẳng của benzene có công thức chung là CnH2n-6 (n≥6).
2. Công thức cấu tạo và danh pháp
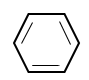
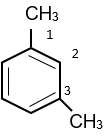
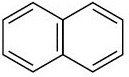
Một số arene, gốc ary thường gặp có công thức cấu tạo và tên gọi như sau:
 |
 |
 |
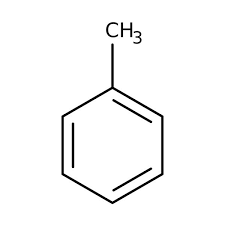 |
| benzene | 1-3-dimethylbenzene | naphthalene |
methylbezene (toluene) |
II. Đặc điểm cấu tạo của benzene
Phân tử benzene có 6 nguyên tử carbon tạo thành hình lục giác đều, tất cả nguyên tử carbon và hydrogen đều nằm trên một mặt phẳng, các góc liên kết đều bằng 120°, độ dài liên kết carbon – carbon đều bằng 139 pm.
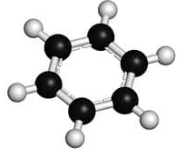 |
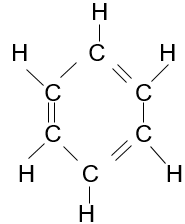 |
| Mô hình phân tử | Công thức cấu tạo |
III. Tính chất vật lí và trạng thái tự nhiên
Benzene, toluene, xylene, styrene ở điều kiện thường là chất lỏng không màu, trong suốt, dễ chảy và có mùi đặc trưng.
Naphthalene là chất rắn màu trắng, có mùi đặc trung (có thể phát hiện được ở nồng độ thấp).
Các arene không phân cực hoặc kém phân cực nên không tan trong nước và thường nhẹ hơn nước, tan được trong các dung môi hữu cơ.
| Arene | Nhiệt độ nóng chảy (oC) | Nhiệt độ sôi (oC) | Khối lương riêng (g/cm3) |
| Benzene | 5,5 | 80,1 | 0,878 |
| Toluene | -95,0 | 110,6 | 0,867 |
| o-Xylene | -25,2 | 144 | 0,880 |
| m-xylene | -47,4 | 139 | 0,864 |
| p-xylene | 13,3 | 138 | 0,861 |
| styrene | -30,0 | 145 | 0,909 |
| Naphthalene | 80,26 | 218 |
1,0253 (20oC) 0,9625 (100oC) |
IV. Tính chất hoá học
1. Phản ứng thế
Arene có thể tham gia phản ứng thể nguyên tử hydrogen ở vòng benzene như phản ứng halogen hoá, nitro hoa,..
Quy tắc thể: Khi benzene có nhóm thể alkyl (–CH3, -C2H5,...), các phản ứng thế nguyên tử hydrogen ở vòng benzene xảy ra dễ dàng hơn so với benzene và ưu tiên thế vào vị trí số 2 hoặc số 4 (vị trí ortho hoặc para) so với nhóm alkyl.
1.1. Phản ứng halogen hoá
Các arene tham gia phản ứng thế nguyên tử hydrogen gắn với vòng thơm bằng halogen (chlorine, bromine) ở nhiệt độ cao khi có xúc tác muỗi Iron(III) halide.
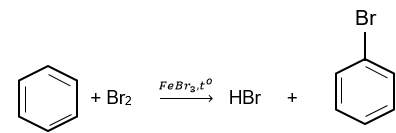
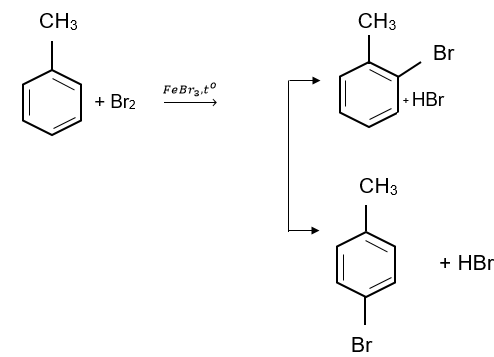
1.2. Phản ứng nitro hóa
Phản ứng nitro hoá là phản ứng trong đó một hay nhiều nguyên tử hydrogen ở vòng benzene được thay thế bằng nhóm nitro (-NO2).
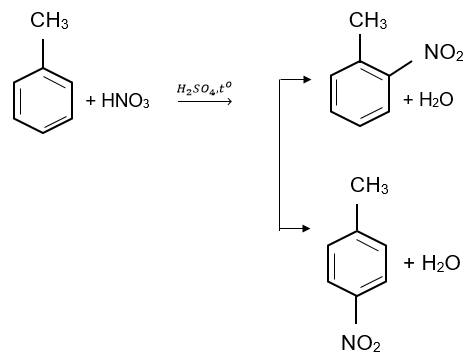
Benzene được nitro hóa bằng hổn hợp HNO3 đặc và H2SO4 đặc ở nhiệt độ không quá 50oC tạo nitrobenzene dạng lỏng, màu vàng nhạt, sánh như dầu:

Tolunene được nitro hóa tạo thành hỗn hợp hai sản phẩm chính ortho và para-nitrotolune.
2. Phản ứng cộng
2.1. Phản ứng cộng chlorine
Phản ứng cộng chlorine vào benzene trong điều kiện có ánh sáng từ ngoại và đun nóng, sản phẩm thu được là 1,2,3,4,5,6 hexachlorocyclohexane.
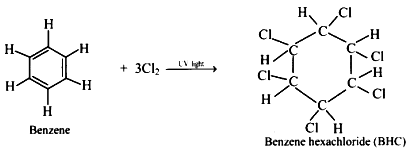
2.2. Phản ứng cộng hydrogen
Phản ứng cộng hydrogen vào benzene tạo thành cyclohexane. Phản ứng xảy ra ở điều kiện áp suất cao và nhiệt độ cao, với sự có mặt của các chất xúc tác dị thể như platinum, nickel.
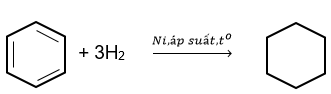
cyclohexane
Phản ứng này được sử dụng trong công nghiệp để sản xuất cyclohexane.
3. Phản ứng oxi hóa
3.1. Phản ứng oxi hóa hoàn toàn (phản ứng cháy)
Các arene như benzene, toluene, xylene dễ cháy và tỏa nhiều nhiệt.
C6H5CH3 + 9O2 ![]() 7CO2 + 4H2O
7CO2 + 4H2O
3.2. Phản ứng oxi hoá nhóm alkyl
Toluene và các alkylbenzene khác có thể bị oxi hoá bởi các tác nhân oxi hoá như dụng dịch KMnO4.
Ví dụ:
C6H5CH3 + 2KMnO4 ![]() C6H5COOK + KOH + 2MnO2 + H2O
C6H5COOK + KOH + 2MnO2 + H2O
C6H5COOK + HCl → C6H5COOH + KCl
V. Ứng dụng
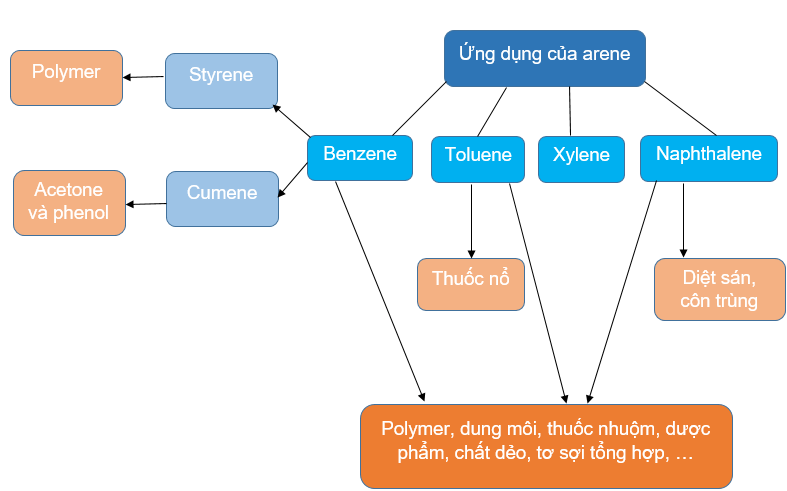
VI. Điều chế
Trong công nghiệp, benzene, toluene được điều chế từ quá trình refoming phân đoạn dầu mỏ chứa các alkane và cydoalkane C6 – C8.
Ví dụ:
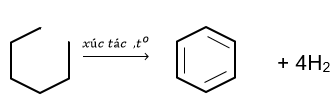
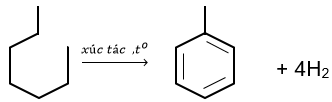
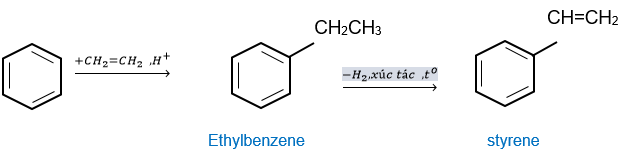
Ethylbenzene được điều chế từ phản ứng giữa benzene và ethylene với xúc tác acid rắn là zeolite.
Naphthalene được điều chế chủ yếu bằng phương pháp chưng cất nhựa than đá.
Nội dung cùng chủ đề
-
Chương 1: Cân bằng hóa học
-
Chương 2: Nitrogen - Sulfur
-
Chương 3: Đại cương về hóa học hữu cơ
-
Chương 4: Hydrocarbon
-
Chương 5: Dẫn xuất halogen - Alcohol - Phenol
-
Chương 6: Hợp chất carbonyl - Carboxylic acid
-
Đề thi Hóa 11 KNTT







