Ethyl alcohol tan vô hạn trong nước là do
Ethyl alcohol tan vô hạn trong nước là do hình thành liên kết hydrogen với nước.
Ethyl alcohol tan vô hạn trong nước là do
Ethyl alcohol tan vô hạn trong nước là do hình thành liên kết hydrogen với nước.
Chất nào sau đây có đồng phân hình học:
Trong phân tử của hai alkenen CH3-CH2-CH=CH-CH 2-CH3, ta thấy nguyên tử C trong liên kết đôi liên kết với hai nhóm thế khác nhau nên chúng có đồng phân hình học.
Cho dãy các chất sau: CH3COOH, CH3CHO, HCOOH, C2H5OH, CH3-C≡CH, CH2=CH-CH3. Số chất trong dãy có thể tham gia phản ứng dung dịch AgNO3/NH3 là:
Chất có thể tham gia phản ứng tráng bạc là: CH3CHO, HCOOH, CH3-C≡CH
Cho 1,97 gam dung dịch Formaldehyde tác dụng với dung dịch AgNO3/NH3 dư thu được 10,8 gam Ag. Nồng độ % của Formaldehyde là:
nAg = 10,8 : 108 = 0,1 mol
Phương trình phản ứng hóa học
HCH=O + 4AgNO3 + 6NH3 + 2H2O → (NH4)2CO3 + 4Ag↓ + 4NH4NO3
nHCHO = 1/4nAg = 0,025 mol
→ mHCHO = 0,025.30 = 0,75 gam
Vậy nồng độ % của Formaldehyde trong dung dịch là:
C%HCHO = 0,75:1,97.100% = 38,07%
Trong số các chất sau, chất tan trong nước ở điều kiện thường là
C2H5OH là chất lỏng, không màu, tan vô hạn trong nước.
Số đồng phân cấu tạo alcohol có công thức phân tử C4H10O là
Các đồng phân cấu tạo alcohol có công thức C4H10O là:
CH3CH2CH2CH2OH;
CH3CH2CHOHCH3;
(CH3)2CHOHCH3;
(CH3)2CHCH2OH.
Trong những cặp chất sau đây, cặp chất nào thuộc loại hợp chất carbonyl?
Trong phân tử hợp chất carbonyl có chứa nhóm >C=O. Vậy hợp chất carbonyl trong các hợp chất trên là HCHO, CH3COCH3.
Cho Na tác dụng vừa đủ với 1,488 gam hỗn hợp 3 alcohol đơn chức X, Y, Z thấy thoát ra 0,44622 lít khí H2 (đkc). Khối lượng muối thu được là
nH2 = 0,44622 : 24,79 = 0,018 mol
Phương trình phản ứng
ROH + Na → RONa + 1/2 H2
nNa = 2.nH2 = 2. 0,018 = 0,036 mol
Áp dụng định luật bảo toàn khối lượng:
mMuối = malcohol + mNa - mH2 = 1,488 + 0,036.23 – 0,018.2 = 2,28 gam
Ethyl alcohol không phản ứng với chất nào sau đây?
Alcohol không phản ứng với Cu
Phương trình phản ứng minh họa
C2H5OH + Na → C2H5ONa + H2
C2H5OH + CuO CH3CHO + Cu↓ + H2O
C2H5OH C2H4 + H2O
Công thức chung của alcohol no, đơn chức, mạch hở là
Alcohol no, đơn chức, mạch hở có công thức chung là CnH2n+1OH (n ≥ 1)
Chất nào sau đây không phải là hydrocarbon
Hydrocarbon: tạo thành từ 2 nguyên tố carbon (C) và hydrogen (H).
Vậy hợp chất CH3-CO-CH3 không phải là hydrocarbon
Thực hiện phản ứng khử hợp chất carbonyl sau:
(CH3)2CH-CH2-CHO + 2[H] ![]() (CH3)2CH-CH2-CH2OH
(CH3)2CH-CH2-CH2OH
Sản phẩm thu được là:
Phương trình phản ứng
(CH3)2CH-CH2-CHO + 2[H] (CH3)2CH-CH2-CH2OH
3-methylbutan-1-ol
Thí nghiệm nào sau đây xảy ra phản ứng tạo sản phẩm chính là alcohol
Các dẫn xuất halogen có thể tham gia phản ứng với dung dịch kiềm, nguyên tử halogen bị thay thế bởi nhóm OH− , tạo thành alcohol.
Đun nóng CH2=CH-CH2Br trong dung dịch NaOH.
CH2=CH-CH2Br + NaOH CH2=CH-CH2OH + NaBr
Còn các thí nghiệm còn lại là phản ứng tách hydrogen halide để tạo thành alkene
Cho sơ đồ phản ứng: C2H2 → X → CH3COOH.
Trong sơ đồ trên, mỗi mũi tên là một phản ứng. X là chất nào sau đây?
X chính là CH3CHO
Phương trình phản ứng minh họa
C2H2 + H2O CH3CHO
Đun nóng m gam hỗn hợp X gồm C2H2, C2H4, và H2 với xúc tác Ni đến phản ứng xảy ra hoàn toàn, thu được 9,916 lít (đkc) hỗn hợp Y (có tỉ khối so với H2 bằng 8). Đốt cháy hoàn toàn cùng lượng hỗn hợp X trên, rồi cho sản phẩm cháy hấp thụ hoàn toàn vào dung dịch Ca(OH)2 dư. Khối lượng kết tủa tạo thành là:
nY = 9,916 : 24,79 = 0,4 mol
MY = 8.2 = 16 ⇒ Y chứa H2 dư
Vì phản ứng xảy ra hoàn toàn nên trong Y chứa C2H6 (x mol) và H2 dư (y mol)
⇒ x + y = 0,4 mol (1)
Từ (1) và (2)
Giải hệ phương trình (1) và (2) ta có:
x = y = 0,2 mol
Đốt cháy X cũng thu được số mol CO2 và H2O như đốt cháy Y
Bảo toàn nguyên tố C:
nCO2 = 2.nC2H6 = 2.0,2 = 0,4 mol
Phương trình hóa học
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
nCO2 = nCaCO3 = 0,4 mol
⇒ mCaCO3 = 0,4.100 = 40 gam
X có công thức phân tử là C3H6O2, có khả năng phản ứng với Na và tham gia được phản ứng tráng gương. Hydrate hóa X thu được Y, Y có khả năng hòa tan được Cu(OH)2 tạo dung dịch xanh lam đặc trưng. Công thức cấu tạo của X là:
X (C3H6O2) có phản ứng tráng gương
⇒ X có CHO
X phản ứng với Na ⇒ X chứa OH
X Y
dung dịch màu xanh lam đặc trưng
⇒ Y có 2 OH kề nhau
⇒ X có công thức cấu tạo CH3CH(OH)CHO
Để nhận biết 3 ống nghiệm riêng biệt ba hóa chất sau: ethanol, glycerol, phenol bằng hóa chất nào sau đây?
Thuốc thử dùng để ethanol, glycerol, phenol dung dịch Br2, Cu(OH)2.
Cho dung dịch Br2 vào 3 ống nghiệm
Xuất hiện kết tủa trắng ⇒ phenol
C6H5OH + 3Br2 → C6H2Br3OH + 3HBr
↓ trắng
Không có hiện tượng gì ⇒ ethanol, glycerol
Sử dùng Cu(OH)2 để nhận biết ethanol, glycerol
Glycerol tạo phức xanh đậm với Cu(OH)2
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
Không có hiện tượng gì là ethanol
Cho dung dịch chứa 5,28 gam CH3CHO tác dụng với dung dịch AgNO3/NH3 (dư). Sau phản ứng thu được m gam bạc. Giá trị m là:
nCH3CHO = 5,28 : 44 = 0,12 mol
Sơ đồ phản ứng:
CH3CHO 2Ag
0,12 → 0,24 mol
mAg = 0,24.108 = 12,96 gam
Cho các phát biểu sau:
(a) Phenol dễ tham gia phản ưng thế bromine và thế nitro hơn benzene do ảnh hưởng của nhóm -OH..
(b) Cho ethane-1,2-diol vào ống nghiệm có Cu(OH)2 và dung dịch NaOH, lắc nhẹ, hiện tượng quan sát được là dung dịch có màu xanh đậm.
(c) Formalin hay formon là dung dịch của methanal trong nước.
(d) Có thể điều chế aldehyde trực tiếp từ bất kì alcohol nào.
(e) Toluene (C6H5CH3) tác dụng được với nước bromine, dung dịch thuốc tím ở điều kiện thường.
Số phát biểu đúng là
(d) sai vì aldehyde không được điều chế trực tiếp từ alcohol
(e) sai vì Toluene (C6H5CH3) không tác dụng được với nước bromine, dung dịch thuốc tím ở điều kiện thường.
Khi cho 6,0 gam chất hữu cơ X có công thức ROH (R là gốc hydrocarbon) tác dụng với natri dư thấy có 1,2395 lít khí thoát ra (đkc). Công thức của X là:
Đặt công thức của X là ROH
nH2 = 1,2395 : 24,79 = 0,05 mol
Phương trình phản ứng:
ROH + Na → RONa + H2
Bảo toàn nguyên tố H ta có:
nROH = 2.nH2 = 0,05.2 = 0,1 mol
⇒ MROH = mROH : nROH = 6 : 0,1 = 60 gam/mol
⇒ MR = 60 - 17 = 43 (C3H7-)
⇒ X: CH3-CH2-CH2-OH
Để phân biệt but-2-yne với but-1-yne có thể dùng thuốc thử nào sau đây?
Chỉ có alk-1-yne mới có phản ứng với dung dịch AgNO3/NH3 để tạo kết tủa.
but-2-yne: (CH3C≡CCH3)
but-1-yne: (CH≡CCH2CH3)
CH≡C-CH2-CH3 + AgNO3 + NH3 → AgC≡C–CH2-CH3 + NH4NO3
Hỗn hợp X gồm hai acid hữu cơ no, đơn chức, mạch hở. Trung hoà 8,3 gam X bằng dung dịch NaOH rồi cô cạn dung dịch sau phản ứng thu được 11,6 gam muối khan. Mặt khác, nếu cho 8,3 gam X tác dụng với lượng dư dung dịch AgNO3 trong NH3 thì thu được 21,6 gam bạc. Công thức của 2 acid là:
Phương trình phản ứng
RCOOH + NaOH → RCOONa + H2O
R + 45 R + 67
8,3 11,6
Áp dụng phương pháp tăng giảm khối lượng ta có
X tác dụng với AgNO3/NH3 ⇒ Có một acid là HCOOH
nAg = 21,6 : 108 = 0,2 mol
HCOOH + 2AgNO3 + 4NH3 + H2O → (NH4)2CO3 + 2NH4NO3 + 2Ag
0,1 ← 0,2
nHCOOH = nAg = 0,1 mol
⇒ nacid = 0,15 – 0,1 = 0,05 mol;
macid = 8,3 – 0,1.46 = 3,7 ⇒ Macid = 74 ⇒ Acid còn lại là C2H5COOH
Hợp chất nào sau đây là một alkene?
Alkene là các hydrocarbon không no, mạch hở, có chứa một liên kết đôi >C = C< trong phân tử
Điều chế Acetic acid bằng phương pháp lên men giấm từ dung dịch chất nào sau đây?
Điều chế Acetic acid bằng phương pháp lên men giấm từ dung dịch ethanol
C2H5OH + O2 CH3COOH + H2O.
Chất nào sau đây không làm mất màu dung dịch thuốc tím ở điều kiện thường?
Naphthalene không làm mất màu dung dịch thuốc tím ở điều kiện thường.
Phương trình phản ứng các chất còn lại
3C6H5-CH=CH2 + 10KMnO4 → 3C6H5COOK + 3K2CO3 + 10MnO2 + KOH + 4H2O
3C2H2 + 8KMnO4 + 4H2O → 3(COOH)2 + 8MnO2 + 8KOH
3C2H4 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2MnO2 + 2KOH
Khi oxi hóa 6,9 gam Ethyl alcohol bởi CuO, to thu được lượng Acetaldehyde với hiệu suất 75%.
nC2H5OH = 6,9 : 46 = 0,15 mol
Phương trình phản ứng:
C2H5OH + CuO CH3CHO + Cu + H2O
⇒ nC2H5OH phản ứng = 0,15.75% = 0,1125 mol
Theo phương trình ta có:
nC2H5OH phản ứng = nCH3CHO = 0,1125 mol
⇒ mCH3CHO = 0,1125.44 = 4,95 gam.
Hỗn hợp X gồm C2H5OH và C6H5OH. Cho m gam X tác dụng hết với Na sinh ra 3,7185 lít H2 (đkc). Cũng lượng m gam hỗn hợp X như trên tác dụng vừa đủ với 100 mL dung dịch NaOH 1M. Giá trị của m là:
nH2 = 3,7185 : 24,79 = 0,15 mol
nNaOH = 0,1.1 = 0,1 mol
Cho hỗn hợp tác dụng với Na, ta có các phương trình hóa học
Cho hỗn hợp tác dụng với NaOH, chỉ có Phenol phản ứng:
Phương trình hóa học
C6H5OH + NaOH → C6H5ONa + H2O
0,1 ← 0,1
Vậy nC6H5OH = 0,1 mol
Theo phương trình hóa học (2), suy ra: nH 2(2)= 0,05 ⇒ nH2(1)= 0,15 − 0,05 = 0,1 mol
Theo phương trình hóa học (1)
⇒ nC2H5OH = 0,2 mol
Vậy m = 0,2.46 + 0,1.94 = 18,6 gam
Phản ứng của benzene với các chất nào sau đây gọi là phản ứng nitro hóa?
Phản ứng của benzene với HNO3 đặc trong H2SO4 đặc được gọi là phản ứng nitro hóa.
Oxi hoá Butan-2-ol bằng CuO nung nóng, thu được sản phẩm nào sau đây?
Oxi hoá alcohol bậc II bằng CuO, thu được ketone.
Butan-2-ol là alcohol bậc 2
CH3-CHOH-CH2-CH3 + CuO CH3-CO-CH2-CH3 + H2O + Cu
Hydrocarbon nào sau đây thuộc dãy đồng đẳng alkyne?
Alkyne là hydrocarbon không no, mạch hở, phân tử có một liên kết ba (C≡C), có công thức chung là CnH2n-2 (n ≥ 2).
Vậy hợp chất C2H2 thuộc dãy đồng đẳng alkyne
Phản ứng với chất/dung dịch nào sau đây của phenol chứng minh phenol có tính acid?
Gốc –C6H5 làm tính acid của phenol mạnh hơn so với alcohol: phenol phản ứng được với NaOH còn alcohol không có phản ứng đó:
C6H5OH + NaOH → C6H5ONa + H2O.
Chất nào sau đây không phải là dẫn xuất halogen của hydrocarbon?
Hợp chất ClCH2COOH ngoài C, H, halogen ra còn chứa nguyên tử O nên không phải là dẫn xuất halogen của hydrocarbon.
Một loại nước uống có cồn, thể tích bình chứa 330 mL dung dịch và trên nhãn ghi độ cồn là 4,5o. Tính thể tích ethanol có trong 350mL dung dịch của loại nước uống này.
Thể tích ethanol có trong 330 mL dung dịch:
Sản phẩm tạo thành chất kết tủa khi cho phenol tác dụng với chất nào sau đây?
Phenol tác dụng với nước bromine sinh ra kết tủa trắng
Cho 13,8 gam hỗn hợp X gồm formic acid và ethanol phản ứng hết với Na dư, thu được V lít khí H2 (đkc). Giá trị của V là:
Phương trình hóa học:
2HCOOH + 2Na → 2HCOONa + H2↑
2C2H5OH + 2Na → 2C2H5ONa + H2↑
Khối lượng phân tử của HCOOH và C2H5OH đều bằng 46 gam/mol
⇒ nhỗn hợp X = 13,8 : 46 = 0,3 mol
Theo phương trình phản ứng:
VH2 = 0,15.24,79 = 3,7185 lít.
Công thức cấu tạo của Propanoic acid là
Propanoic acid là CH3CH2COOH
Số đồng phân có công thức phân tử C4H9Cl khi đun nóng với dung dịch NaOH thu được alcohol bậc I là
Đồng phân C4H9Cl
CH3-CH2-CH2-CH2-Cl
CH3-CH2-CH(Cl)-CH3
CH3-CH(CH3)-CH2-Cl
CH3-CH2-CH(CH3)-Cl
CH3-C(CH3)(Cl)-CH3
Các công thức thỏa mãn khi đun nóng với dung dịch NaOH thu được alcohol bậc I là: CH3CH2CH2CH2Cl; (CH3)2CHCH2Cl.
Phương trình minh họa
CH3CH2CH2CH2Cl + NaOH → CH3CH2CH2CH2OH + NaCl
(CH3)2CHCH2Cl + NaOH → (CH3)2CHCH2OH + NaCl
Trong các chất sau đây, chất nào có nhiệt độ sôi cao nhất?
Với các chất có phân tử khối chênh lệch nhau không nhiều: Nhiệt độ sôi của carboxylic acid > alcohol > aldehyde > alkane.
Vậy CH3COOH có nhiệt độ sôi lớn nhất
Cho công thức cấu tạo sau: (CH3)2CHCH2CH2OH. Tên thay thế của hợp chất này là
Đánh số từ đầu gần nhóm OH hơn
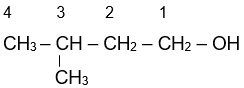
3-methylbutan-1-ol.
Cho các chất: C2H5OH, C2H5Br, C6H5OH, C6H5CH2OH, CH3COOH. Số chất tác dụng được với dung dịch NaOH, đun nóng là
Chất tác dụng được với dung dịch NaOH:
CH3COOH + NaOH → CH3COONa + H2O
C6H5OH + NaOH → C6H5ONa + H2O
C2H5Br + NaOH C2H5OH + NaBr
