Phản ứng hóa học và năng lượng của phản ứng hóa học
I. Phản ứng hóa học là gì
Quá trình biến đổi từ chất này thành chất khác gọi là phản ứng hóa học
Ví dụ: Đốt cháy khí hydrogen trong không khí tạo ra ngọn lửa màu xanh, sau đó đưa ngọn lửa của khí hydrogen đang cháy vào bình đựng khí oxygen thì thấy khí hydrogen cháy mạnh hơn, sáng hơn và trên thành bình xuất hiện những giọt nước nhỏ. Ở đây đã diễn ra sự biến đổi hoá học, trong đó xảy ra quá trình biến đổi hydrogen và oxygen tạo thành nước. Quá trình này đã xảy ra phản ứng hoá học.
Chất ban đầu bị biến đổi trong phản ứng được gọi là chất tham gia phản ứng, chất tạo thành sau phản ứng được gọi là chất sản phẩm.
Ví dụ:
Khi đun nóng hỗn hợp bột sắt (iron) và bột lưu huỳnh (sulfur) ta được hợp chất iron(II) sulfide (FeS).
- Chất tham gia phản ứng là sắt và lưu huỳnh.
- Chất sản phẩm là iron(II) sulfide.
II. Diễn biến của phản ứng hoá học
Các biến đổi hoá học xảy ra khi có sự phá vỡ liên kết trong các chất tham gia phản ứng và hình thành các liên kết mới để tạo ra các chất sản phẩm.
Ví dụ 3:
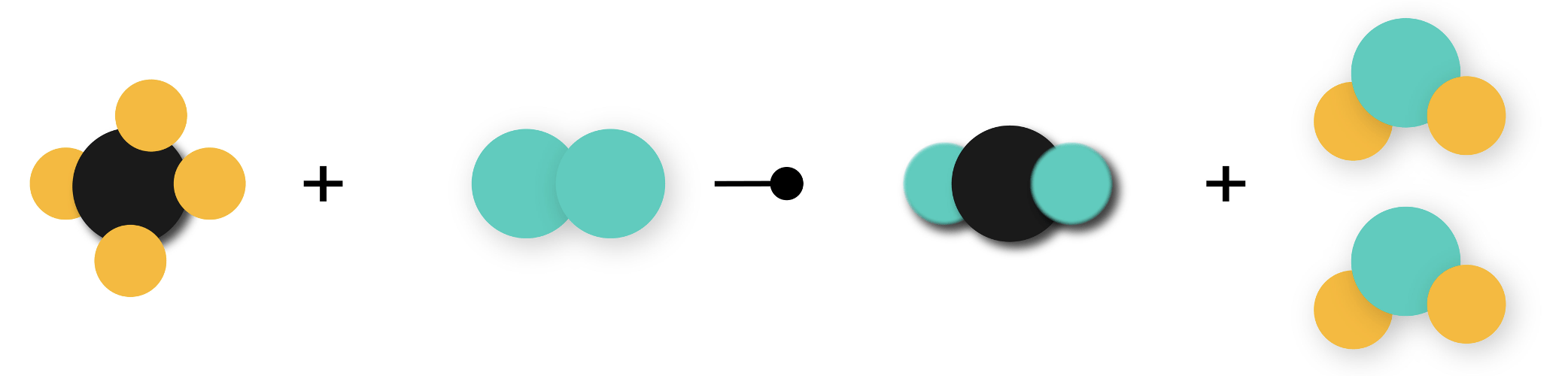
- Phản ứng hóa học xảy ra trong thí nghiệm khí hydrogen cháy trong oxygen tạo thành nước, quá trình đó được mô tả theo sơ đồ sau:
![]() Nguyên tử H
Nguyên tử H ![]() Nguyeen tử O
Nguyeen tử O  Nguyên tử C
Nguyên tử C
Hình 1: Sơ đồ mô tả phản ứng đốt cháy khí methane trong không khí
thu được carbon dioxide và nước
- Trong sơ đồ trên, các liên kết trong phân tử CH4, O2 bị phá vỡ và hình thành liên kết mới giữa 1 nguyên tử C với 2 nguyên tử O (CO2) và một nguyên nguyên tử O với 2 nguyên tử H (H2O).
Trong phản ứng hoá học, chỉ có liên kết giữa các nguyên tử thay đổi làm cho phân tử này biến đổi thành phân tử khác, kết quả là chất này biến đổi thành chất khác. Số nguyên tử của mỗi nguyên tố trước và sau phản ứng không thay đổi.
III. Dấu hiệu có phản ứng hoá học xảy ra
Để nhận biết có phản ứng hoá học xảy ra có thể dựa vào các dấu hiệu sau:
- Có sự thay đổi màu sắc, mùi, … của các chất; tạo ra chất khí hoặc chất không tan (kết tủa); …
Ví dụ: Trong phản ứng của sắt tác dụng với hydrochloric acid, quan sát thấy có bọt khí bay lên.
 Hình 2: Bọt khí thoát ra khi nhúng đinh sắt vào dung dịch hydrochloric acid
Hình 2: Bọt khí thoát ra khi nhúng đinh sắt vào dung dịch hydrochloric acid
- Có sự toả nhiệt và phát sáng: Sự toả nhiệt và phát sáng cũng có thể là dấu hiệu của phản ứng hoá học xảy ra.
Ví dụ: Khi đốt nến, nến cháy có sự toả nhiệt và phát sáng.
 Hình 3: Đốt cháy cây nến
Hình 3: Đốt cháy cây nến
V. Phản ứng toả nhiệt, phản ứng thu nhiệt
1. Khái niệm
Các phản ứng hoá học khi xảy ra luôn kèm theo sự toả ra hoặc thu vào năng lượng (thường dưới dạng nhiệt), năng lượng này được gọi là năng lượng của phản ứng hoá học.
Phản ứng toả ra năng lượng (dưới dạng nhiệt) được gọi là phản ứng toả nhiệt.
Phản ứng toả nhiệt làm nóng môi trường xung quanh.
Ví dụ: Phản ứng đốt cháy than; phản ứng đốt cháy xăng, dầu trong các động cơ; …
Phản ứng thu vào năng lượng (dưới dạng nhiệt) được gọi là phản ứng thu nhiệt.
Phản ứng thu nhiệt làm lạnh môi trường xung quanh.
Ví dụ: Phản ứng nung vôi (phân huỷ CaCO3 thành CaO và CO2).
2. Ứng dụng của phản ứng toả nhiệt
- Trong sản xuất và đời sống, các phản ứng toả nhiệt có ứng dụng chính là cung cấp năng lượng nhiệt cho các ngành công nghiệp, làm cho các động cơ hay máy phát điện hoạt động.
- Nhiệt năng thu được khi đốt cháy các nhiên liệu như than, xăng, dầu,... có thể được dùng để đun nấu, sưởi ấm, thắp sáng,... Than được sử dụng chủ yếu làm nhiên liệu trong công nghiệp. Xăng, dầu được sử dụng chủ yếu trong việc vận hành các máy móc, phương tiện giao thông như xe máy, ô tô, tàu thuỷ,...
Nội dung cùng chủ đề
-
Bài mở đầu: Làm quen với bộ dụng cụ, thiết bị thực hành môn Khoa học tự nhiên 8
-
Chủ đề 1: Phản ứng hóa học
-
Bài 1: Biến đổi vật lí và biến đổi hóa học
-
Bài 2: Phản ứng hóa học và năng lượng của phản ứng hóa học
-
Bài 3: Định luật bảo toàn khối lượng, Phương trình hóa học
-
Bài 4: Mol và tỉ khối của chất khí
-
Bài 5: Tính theo phương trình hóa học
-
Bài 6: Nồng độ dung dịch
-
Bài 7: Tốc độ phản ứng và chất xúc tác
-
Ôn tập & kiểm tra Chủ đề 1
-
-
Chủ đề 2: Acid - Base - pH - Oxide - Muối
-
Đề thi giữa học kì 1 Dạy nối tiếp
-
Đề thi giữa học kì 1 Dạy song song
-
Chủ đề 3: Khối lượng riêng và áp suất
-
Chủ đề 4: Tác dụng làm quay của lực
-
Đề thi cuối học kì 1 Dạy nối tiếp
-
Đề thi cuối học kì 1 Dạy song song
-
Chủ đề 5: Điện
-
Chủ đề 6: Nhiệt
-
Chủ đề 7: Cơ thể người
-
Bài 27: Khái quát về cơ thể người
-
Bài 28: Hệ vận động ở người
-
Bài 29: Dinh dưỡng và tiêu hóa ở người
-
Bài 30: Máu và hệ tuần hoàn ở người
-
Bài 31: Thực hành máu và hệ tuần hoàn
-
Bài 32: Hệ hô hấp ở người
-
Bài 33: Môi trường trong cơ thể và hệ bài tiết ở người
-
Bài 34: Hệ thần kinh và các giác quan ở người
-
Bài 35: Hệ nội tiết ở người
-
Bài 36: Da và điều hòa thân nhiệt ở người
-
Bài 37: Sinh sản ở người
-
Ôn tập & kiểm tra Chủ đề 7
-
-
Đề thi giữa học kì 2 Dạy nối tiếp
-
Đề thi giữa học kì 2 Dạy song song
-
Chủ đề 8: Sinh thái
-
Chủ đề 9: Sinh quyển
-
Đề thi cuối học kì 2 Dạy nối tiếp
-
Đề thi học kì 2 Khoa học tự nhiên 8 - Đề 4







