Ôn tập chủ đề 2
Tóm tắt kiến thức
1. Acid
Khái niệm
- Hợp chất mà phân tử có một hay nhiều nguyên tử H liên kết với gôc acid.
- Tan trong nước, tạo ra ion H+.
Tính chất hóa học:
- Làm quỳ tím hóa đỏ.
- Acid + Kim loại → Muối + H2↑
Ứng dụng:
- CH3COOH: dược phẩm, tơ nhân tạo, chất dẻo, giấm ăn, ...
- HCl, H2SO4: chất tẩy rửa, acquy, tơ sợi, phân bón, giấy, ...
2. Base
Khái niệm
- Hợp chất mà phân tử có một nguyên tử kim loại liên kết với một hay nhiều nhóm OH.
- Base tan trong nước gọi là kiềm, tạo ra ion OH- (NaOH, KOH, ...).
- Base không tan trong nước (Mg(OH)2, Al(OH)3, ...)
Tính chất hóa học
- Làm quỳ tím hóa xanh.
- Làm dung dịch phenolphathalein hóa hồng.
- Base + Acid → Muối + H2O
3. Oxide
Khái niệm
- Hợp chất gồm hai nguyên tố, trong đó có nguyên tố oxygen.
- Oxide được tạo thành từ phản ứng giữa kim loại/phi kim với oxygen.
Phân loại oxide
- Oxide acid: phản ứng được với dung dịch base.
- Oxide base: phản ứng được với dung dịch acid.
- Oxide lưỡng tính: vừa phản ứng được với dung dịch acid, vừa phản ứng được với dung dịch base.
- Oxide trung tính: không phản ứng được với dung dịch acid và dung dịch base.
4. Muối
Khái niệm
- Là hợp chất được tạo ra khi thay thế ion H+ trong acid bằng ion kim loại hoặc ion ammonium.
- Bao gồm muối tan, không tan hoặc ít tan trong nước.
Điều chế muối
- Oxide acid + Base → Muối + H2O
- Oxide base + Acid → Muối + H2O
- Acid + Base → Muối + H2O
- Kim loại (Mg, Al, Zn, Fe,...) + Acid → Muối + H2↑
Tính chất hóa học
- Muối KL(A) + KL(B) → Muối KL(B) + KL(A)
- Muối + Base → Muối mới + Base mới
- Muối + Acid → Muối mới + Acid mới
- Muối (A) + Muối (B) → Muối (C) + Muối (D)
- Điều kiện: sản phẩm có chất kết tủa, chất khí, nước.
5. Thang pH
Khái niệm
- Để xác định được độ acid hay base của dung dịch thì người ta dùng thanh pH.
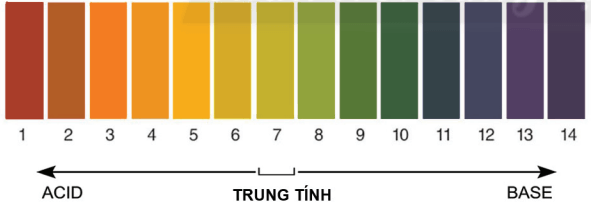
pH và môi trường sống
- pH của môi trường ảnh hưởng đến đời sống của con người và các loài động vật, thực vật. Việc xác định giá trị pH phù hợp sẽ góp phần cải tạo môi trường, xây dựng và phát triển cho cơ thể sống.
6. Phân bón hóa học
Khái niệm
- Phân bón hóa học là hợp chất chứa các nguyên tố dinh dưỡng được dùng để bón cho cây trồng.
- Có 3 loại nguyên tố dinh dưỡng là nguyên tố đa lượng (N, P, K), nguyên tố trung lượng (Ca, Mg, S) và nguyên tố vi lượng (Fe, Cu, Mn, Bo, ...)
Các loại phân bón
- Phân đạm: bổ sung N, kích thích quá trình sinh trưởng, giúp cây phát triển nhanh, tăng năng suất cây trồng.
Gồm: urea, đạm ammonium, đạm nitrate.
- Phân lân: bổ sung P, thúc đẩy quá trình ra rễ, tạo nhánh, phân cành, tăng khả năng chống chịu với những điều kiện bất lợi của môi trường; cải tạo đất chua, bạc màu.
Gồm phân lân nung chảy, phân super phosphate.
- Phân kali: bổ sung K, thúc đẩy quá trình tạo ra chất đường, chất xơ, chất béo, tăng cường sức chống rét, chống sâu bệnh và chịu hạn của cây.
Gồm: phân kali trắng, phân kali đỏ.
- Phân N-P-K: Bổ sung N, P, K, cung cấp các dưỡng chất, kích thích cây phát triển, tăng sức đề kháng cho cây và cải thiện đồ phì nhiêu cho đất.
Gồm: Phân N-P-K hỗn hợp, phân N-P-K phức hợp.
Sử dụng phân bón
- Bón phân không đúng cách sẽ làm ô nhiễm môi trường, ảnh hưởng đến con người,...
- Cần bón phân đúng liều, đúng lúc, đúng loại phân, đúng cách.
Câu trắc nghiệm mã số: 39985,40006,40404,40510,44708
Nội dung cùng chủ đề
Sắp xếp theo
Xóa
Gửi bình luận
-
Chủ đề 1: Phản ứng hóa học
-
Bài 1: Sử dụng hóa chất, dụng cụ và các thiết bị điện an toàn
-
Bài 2: Biến đổi vật lí và biến đổi hóa học
-
Bài 3: Phản ứng hóa học và năng lượng trong các phản ứng hóa học
-
Bài 4: Định luật bảo toàn khối lượng và phương trình hóa học
-
Bài 5: Mol và tỉ khối của chất khí
-
Bài 6: Tính theo phương trình hóa học
-
Bài 7: Nồng độ dung dịch
-
Ôn tập & kiểm tra Chủ đề 1
-
-
Chủ đề 2: Một số hợp chất vô cơ. Thang pH
-
Đề thi giữa học kì 1
-
Đề thi giữa học kì 1 Dạy song song
-
Chủ đề 3: Khối lượng riêng, áp suất và moment lực
-
Chủ đề 4: Điện
-
Đề thi học kì 1 Dạy nối tiếp
-
Đề thi học kì 1 Dạy song song
-
Chủ đề 5: Nhiệt
-
Chủ đề 6: Sinh học cơ thể người
-
Bài 29: Khái quát về cơ thể người
-
Bài 30: Hệ vận động ở người
-
Bài 31: Thực hành: Sơ cứu và băng bó gãy xương. Điều tra tình hình mắc bệnh về hệ vận động trong trường học và khu dân cư
-
Bài 32: Hệ tiêu hóa ở người
-
Bài 33: Dinh dưỡng và an toàn vệ sinh thực phẩm
-
Bài 34: Máu và hệ tuần hoàn của cơ thể người
-
Bài 35: Miễn dịch
-
Bài 36: Thực hành: Cấp cứu, băng bó vết thương, đo huyết áp ở người
-
Bài 37: Hệ hô hấp ở người
-
Bài 38: Thực hành: Hô hấp nhân tạo
-
Bài 39: Hệ bài tiết ở người
-
Bài 40: Điều hòa môi trường trong của cơ thể
-
Bài 41: Hệ thần kinh và các giác quan ở người
-
Bài 42: Hệ nội tiết ở người
-
Bài 43: Da và điều hoà thân nhiệt
-
Bài 44: Hệ sinh dục ở người và bảo vệ sức khỏe sinh sản vị thành niên
-
Ôn tập & kiểm tra Chủ đề 6
-
-
Đề thi giữa học kì 2 Dạy nối tiếp
-
Đề thi giữa học kì 2 Dạy song song
-
Chủ đề 7: Môi trường về hệ sinh thái
-
Đề thi cuối học kì 2 Dạy nối tiếp
-
Đề thi cuối học kì 2 Dạy song song







