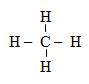Metan
Công thức phân tử metan: CH4
Phân tử khối: 16
I. Trạng thái tự nhiên, tính chất vật lí
Trong tự nhiên, metan có nhiều trong các mỏ khí (khí thiên nhiên), trong mỏ dầu (khí mỏ dầu), trong các mỏ than (khí mỏ than).
Metan là chất khí, không màu, không mùi, nhẹ hơn không khí và tan rất ít trong nước.
II. Cấu tạo phân tử
|
Công thức cấu tạo của metan |
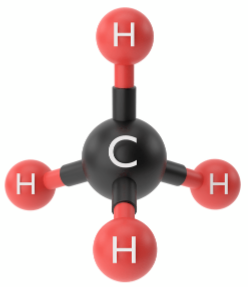
Mô hình phân tử |
- Giữa nguyên tử C và nguyên tử H chỉ có 1 liên kết, đó là liên kết đơn.
- Phân tử metan có 4 liên kết đơn.
III. Tính chất hóa học của Metan
1. Tác dụng với oxi
Khi đốt trong oxi, metan cháy tạo thành khí CO2 và H2O, tỏa nhiều nhiệt.
CH4 + 2O2 ![]() CO2 + 2H2O
CO2 + 2H2O
Hỗn hợp gồm một thể tích metan và hai thể tích oxi là hỗn hợp nổ mạnh.
2. Tác dụng với clo khi có ánh sáng
CH4 + Cl2 ![]() HCl + CH3Cl (metyl clorua)
HCl + CH3Cl (metyl clorua)
Ở phản ứng này, nguyên tử H của metan được thay thế bởi nguyên tử Cl, vì vậy được gọi là phản ứng thế. Đây là phản ứng đặc trưng của liên kết đơn.
IV. Ứng dụng
Metan cháy tỏa nhiều nhiệt nên được đùng làm nhiên liệu.
Metan là nguyên liệu dùng điều chế hiđro theo sơ đồ:
CH4 + H2O → CO2 + H2
Metan còn được dùng để điều chế bột than và nhiều chất khác

Một số ứng dụng của metan trong thực tế
-
Chương 1: Các loại hợp chất vô cơ
-
Bài 1: Tính chất hóa học của oxit. Khái quát về sự phân loại oxit
-
Bài 2: Một số oxit quan trọng
-
Bài 3: Tính chất hóa học của axit
-
Bài 4: Một số axit quan trọng
-
Bài 5: Luyện tập tính chất hóa học oxit và axit
-
Bài 6: Thực hành: Tính chất hóa học của oxit và axit
-
Bài 7: Tính chất hóa học của bazơ
-
Bài 8: Một số bazơ quan trọng
-
Bài 9: Tính chất hóa học của muối
-
Bài 10: Một số muối quan trọng
-
Bài 11: Phân bón hóa học
-
Bài 12: Mối quan hệ giữa các hợp chất vô cơ
-
Thực hành Tính chất hóa học của bazơ và muối
-
Ôn tập & Kiểm tra Chương 1
-
-
Chương 2: Kim loại
-
Bài 15: Tính chất vật lí của kim loại
-
Bài 16: Tính chất hóa học của kim loại
-
Bài 17: Dãy hoạt động hóa học của kim loại
-
Bài 18: Nhôm
-
Bài 19: Sắt
-
Bài 20: Hợp kim sắt Gang, thép
-
Bài 21: Sự ăn mòn kim loại và bảo vệ kim loại không bị ăn mòn
-
Bài 22: Luyện tập chương 2 Kim loại
-
Bài 23: Thực hành tính chất hóa học của nhôm và sắt
-
Ôn tập & Kiểm tra Chương 2
-
-
Chương 3: Phi kim. Sơ lược về bảng tuần hoàn các nguyên tố hóa học
-
Bài 25: Tính chất của phi kim
-
Bài 26: Clo
-
Bài 27: Cacbon
-
Bài 28: Các oxit của cacbon
-
Bài 29: Axit cacbonic và muối cacbonat
-
Bài 30: Silic. Công nghiệp silicat
-
Bài 31: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
-
Bài 33: Thực hành tính chất hóa học của phi kim và hợp chất của chúng
-
Ôn tập & Kiểm tra Chương 3
-
-
Chương 4: Hiđrocacbon. Nhiên liệu
-
Chương 5: Dẫn xuất của Hiđrocacbon. Polime
-
Đề ôn thi Học kì