Pepit và Protein
Peptit và protein đưa ra nội dung lý thuyết tính chất hóa học của peptit, protein, enzim và axit nucleic. Kèm theo các thí dụ, bài tập minh họa cho từng tính chất.
I. Peptit
1. Khái niệm
Peptit là loại hợp chất chứa từ 2 đến 50 gốc α-amino axit liên kết với nhau bởi liên kết peptit.
Những phân tử peptit được tạo lên từ 2, 3, 4,... gốc α-amino axit được gọi là đi-, tri-, tetrapeptit,... Các peptit được tạo lên từ 10 gốc α-amino axit trở lên thì được gọi là polipeptit.
Liên kết peptit là liên kết -CO-NH- giữa hai đơn vị α-amino axit. Nhóm -CO-NH- giữa hai đơn vị α-amino axit được gọi là nhóm peptit.
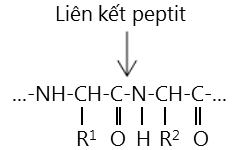
Phân tử peptit được hợp thành từ các gốc α-amino axit bằng liên kết peptit theo 1 trật tự nhất định.
- Amino axit đầu N còn nhóm NH2.
- Amino axit đầu C còn nhóm COOH.
Thí dụ:
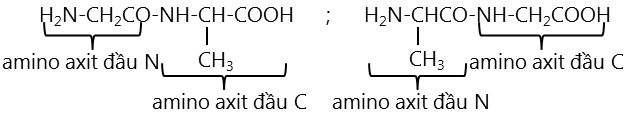
Những phân tử peptit chứa 2, 3, 4,... gốc α -amino axit được gọi là đi-, tri-, tetrapeptit,... Những phân tử peptit chứa nhiều gốc α-amino axit (trên 10) được gọi là polipeptit.
Ta biểu diễn cấu tạo của các peptit bằng cách ghép từ tên viết tắt của các gốc α-amino axit theo trật tự của chúng.
Thí dụ: hai đipeptit từ alanin và glyxin là: Ala-Gly và Gly-Ala.
2. Tính chất hóa học
Peptit có hai phản ứng quan trọng là phản ứng thủy phân và phản ứng màu với Cu(OH)2.
2.1. Phản ứng thủy phân
Ta xét các peptit được tạo thành từ các α-aminoaxit có chứa 1 nhóm NH2 và 1 nhóm COOH.
- Môi trường trung tính
Peptit(n α-aminoaxit) + (n - 1)H2O ![]() nα - aminoaxit
nα - aminoaxit
- Trong môi trường kiềm
Peptit (n α-aminoaxit) + nNaOH → nMuối + H2O
- Trong môi trường axit
Peptit (n α-aminoaxit) + (n - 1)H2O + nHCl → nMuối
Ngoài ra, peptit còn có thể bị thủy phân không hoàn toàn thành các peptit ngắn hơn nhờ xúc tác axit hoặc bazơ và đặc biệt là nhờ các enzim có tác dụng xúc tác đặc hiệu vào một liên kết peptit nhất định nào đó.
2.2. Phản ứng màu biure
Các peptit có từ 2 liên kết peptit trở lên có thể phản ứng với Cu(OH)2 trong môi trường kiềm cho phức chất màu tím. Đây cũng là phản ứng dùng để phân biệt các peptit có từ 2 liên kết peptit trở lên với các đipeptit khác.

II. Protein
1. Khái niệm
Protein là những polipeptit cao phân tử có phân tử khối từ vài chục nghìn đến vài triệu.
Protein được phân thành hai loại:
- Protein đơn giản: Là protein khi thủy phân chỉ thu được hỗn hợp các α-aminoaxit.
Thí dụ: Anbumin của lòng trắng trứng, fiborin của tơ tằm,...
- Protein phức tạp: Là loại protein được tạo thành từ protein đơn giản có thêm thành phần "phi protein".
Thí dụ: Nucleoprotein có chứa axit nucleic, lipoprotein có chứa chất béo...
2. Cấu tạo phân tử
Tương tự peptit, protein được cấu tạo từ nhiều gốc α-aminoaxit nối với nhau bằng liên kết peptit, thường là từ hơn 50 gốc α-aminoaxit trở lên. Khi thay đổi trật tự sắp xếp các gốc α-aminoaxit ta lại thu được các phân tử protein khác nhau. Vì vậy, từ trên 20 α-aminoaxit khác nhau trong tự nhiên có thể tạo ra vô số các protein khác nhau.
Khi thay đổi trật tự sắp xếp các gốc α-aminoaxit ta lại thu được các phân tử protein khác nhau. Vì vậy, từ trên 20 α-aminoaxit khác nhau trong tự nhiên có thể tạo ra vô số các protein khác nhau.
3. Tính chất
3.1. Tính chất vật lí
Protein tồn tại ở hai dạng chính: dạng hình sợi và dạng hình cầu.
- Dạng protein hình sợi như keratin của tóc, móng, sừng; miozin của cơ bắp, fibroin của tơ tằm, mạng nhện.
- Dạng protein hình cầu như anbumin của lòng trắng trứng, hemoglobin của máu.
Tính tan của các loại protein rất khác nhau. Protein hình sợi hoàn toàn không tan trong nước trong khi protein hình cầu tan trong nước tạo thành các dung dịch keo như anbumin (lòng trắng trứng), hemoglobin (máu).
Sự động tụ: Khi đun nóng hoặc cho axit, bazơ hay một số muối vào dung dịch protein, protein sẽ đông tụ lại, tách ra khỏi dung dịch. Ta gọi đó là sự đông tụ của protein.

Trứng sau khi luộc bị biến đổi cấu trúc này gọi là hiện tượng đông tụ của protein
3.2. Tính chất hóa học
Tương tự peptit, protein bị thủy phân nhờ xúc tác axit, bazơ hoặc enzim sinh ra các chuỗi peptit và cuối cùng thành các α-aminoaxit.
Protein cũng có phản ứng màu biure với Cu(OH)2 tạo thành phức màu tím. Đây là một trong các phản ứng dùng để phân biệt protein.
4. Vai trò của protein đối với sự sống
Protein là cơ sở tạo nên sự sống, có protein mới có sự sống.
Ứng dụng chính của protein là làm thức ăn, ngoài ra protein còn có ứng dụng khác trong công nghiệp dệt (len, tơ tằm), da, mĩ nghệ (sừng, ngà) v.v....
 |
 |
III. Khái niệm về enzim và axit nucleic
1. Enzim
1.1. Khái niệm
Enzim là những chất hầu hết có bản chất protein, có khả năng xúc tác cho các quá trình hóa học, đặc biệt trong cơ thể sinh vật.
Tên của các enzim xuất phát từ tên của phản ứng hay chất phản ứng thêm đuôi aza.
1.2. Đặc điểm của xúc tác enzim: có hai đặc điểm
- Hoạt động xúc tác của enzim có tính chọn lọc rất cao.
- Tốc độ phản ứng nhờ xúc tác enzim rất lớn.
2. Axit nucleic
2.1. Khái niệm
- Axit nucleic là polieste của axit photphoric và pentozơ (monosaccarit có 5C); mỗi pentozơ lại liên kết với một bazơ nitơ (đó là các hợp chất dị vòng chứa nitơ được kí hiệu là A, X, G, T, U).
- Axit nucleic là thành phần quan trọng nhất của nhân tế bào và loại polime này có tính axit.
- Axit nucleic thường tồn tại dưới dạng kết hợp với protein gọi là nucleoprotein. Axit nucleic có hai loại được kí hiệu là ADN và ARN.
2.2. Vai trò
- Axit nucleic có vai trò quan trọng bậc nhất trong các hoạt động sống của cơ thể, như sự tổng hợp protein, sự chuyển các thông tin di truyền.
- ADN chứa các thông tin di truyền. Nó là vật liệu di truyền ở cấp độ phân tử mang thông tin di truyền mã hóa cho hoạt động sinh trưởng và phát triển của các cơ thể sống.
- ARN chủ yếu nằm trong tế bào chất, nó tham gia vào quá trình giải mã thông tin di truyền.
-
Chương 1: Este - Lipit
-
Chương 2: Cacbohiđrat
-
Chương 3: Amin, amino axit và protein
-
Chương 4: Polime và vật liệu polime
-
Chương 5: Đại cương về kim loại
-
Bài 17: Vị trí của kim loại trong bảng tuần hoàn và cấu tạo của kim loại
-
Bài 18: Tính chất của kim loại. Dãy điện hóa của kim loại
-
Bài 19: Hợp kim
-
Bài 20: Sự ăn mòn kim loại
-
Bài 21: Điều chế kim loại
-
Bài 22: Luyện tập: Tính chất của kim loại
-
Bài 23: Luyện tập: Điều chế kim loại và sự ăn mòn kim loại
-
Thực hành: Tính chất, điều chế kim loại, sự ăn mòn kim loại
-
Đề Ôn tập Chương 5
-
Đề kiểm tra 15 phút
-
Đề kiểm tra 45 phút
-
-
Chương 6: Kim loại kiềm, kim loại kiềm thổ, nhôm
-
Bài 25: Kim loại kiềm và hợp chất quan trọng của kim loại kiềm
-
Bài 26: Kim loại kiềm thổ và hợp chất quan trọng của kiềm thổ
-
Bài 27: Nhôm và hợp chất của nhôm
-
Bài 28: Luyện tập: Tính chất của kim loại kiềm, kim loại kiềm thổ và hợp chất của chúng
-
Bài 29: Luyện tập: Tính chất của nhôm và hợp chất của nhôm
-
Thực hành: Tính chất của natri, magie, nhôm và hợp chất của chúng
-
Đề Ôn tập Chương 6
-
Đề kiểm tra 15 phút
-
Đề kiểm tra 45 phút
-
-
Chương 7: Sắt và một số kim loại quan trọng
-
Bài 31: Sắt
-
Bài 32: Hợp chất của sắt
-
Bài 33: Hợp kim của sắt
-
Bài 34: Crom và hợp chất của crom
-
Bài 35: Đồng và hợp chất của đồng
-
Bài 36: Sơ lược về niken, kẽm, chì, thiếc
-
Bài 37: Luyện tập: Tính chất hóa học của sắt và hợp chất của sắt
-
Bài 38: Luyện tập: Tính chất hóa học của crom, đồng và hợp chất của chúng
-
Thực hành: Tính chất hóa học của sắt, đồng và những hợp chất của sắt, crom
-
Đề Ôn tập Chương 7
-
Đề kiểm tra 15 phút
-
Đề kiểm tra 45 phút
-
-
Chương 8: Phân biệt một số chất vô cơ
-
Chương 9: Hóa học và vấn đề phát triển kinh tế, xã hội, môi trường
-
Ôn thi Học kì







